
| A. | 钢铁的腐蚀过程中,析氢腐蚀与吸氧腐蚀不可能同时发生 | |
| B. | 镀锌铁制品镀层受损后,铁制品比受损前更容易生锈 | |
| C. | 8NH3(g)+6NO2(g)═7N2(g)+12H2O(g);△H<0,则该反应一定能自发进行 | |
| D. | 原电池反应是导致金属腐蚀的主要原因,故不能用原电池原理来减缓金属的腐蚀 |
分析 A、钢铁腐蚀时若介质为酸性,可能同时发生析氢腐蚀与吸氧腐蚀;
B、镀锌铁制品镀层破损在潮湿的空气中形成原电池,锌做负极被腐蚀,镀锡铁铁做负极被腐蚀;
C、根据反应自发进行的判据:△H-T△S<0反应自发进行来判断;
D、原电池中金属作原电池的正极被保护.
解答 解:A、钢铁腐蚀时若介质为酸性,则可能同时发生析氢腐蚀与吸氧腐蚀,故A错误;
B、镀锌铁制品镀层破损在潮湿的空气中形成原电池,锌做负极被腐蚀,镀锡铁形成原电池,铁做负极被腐蚀,故B错误;
C、8NH3(g)+6NO2(g)═7N2(g)+12H2O(g);△H<0,△S>0,则:△H-T△S<0,该反应一定能自发,故C正确;
D、金属作原电池的正极被保护,所以可以用原电池原理来减缓金属的腐蚀,故D错误;
故选C.
点评 本题综合考察了钢铁的腐蚀、反应能否自发的判断、金属的腐蚀和防护知识,综合性较强,难度适中.


科目:高中化学 来源: 题型:解答题
| 物质 | Cl2 | Br2 | I2 | H2 | HCl | HI | HBr |
| 键能/kJ•mol-1 | 243 | 193 | 151 | 436 | 431 | 298 | 366 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(A)=3 mol•L-1•min-1 | B. | v(B)=6 mol•L-1•min-1 | ||
| C. | v(C)=2.5 mol•L-1•min-1 | D. | v(D)=4 mol•L-1•min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 物质 | A | B | C | D |
| 起始投料/mol | 2 | 2 | 3 | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 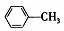 的一溴代物和 的一溴代物和 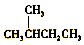 的一溴代物都有4种(不考虑立体异构) 的一溴代物都有4种(不考虑立体异构) | |
| B. | C5H11Cl有3种同分异构体 | |
| C. | 按系统命名法,化合物 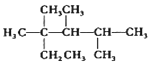 的名称是2,3,4-三甲基-2-乙基戊烷 的名称是2,3,4-三甲基-2-乙基戊烷 | |
| D. | CH3CH═CHCH3分子中的四个碳原子在同一直线上 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
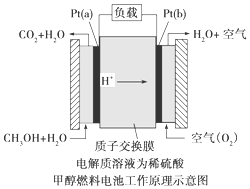
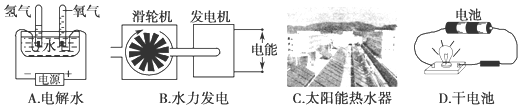
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH溶解后未经冷却,迅速转移到容量瓶中 | |
| B. | 容量瓶未干燥 | |
| C. | 定容时俯视液面 | |
| D. | 洗涤烧杯和玻璃棒的溶液未转移到容量瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
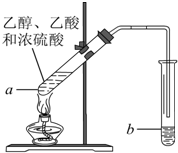 红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了有香味的酯.在实验室也可以用如图所示的装置制取乙酸乙酯,请回答下列问题.
红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了有香味的酯.在实验室也可以用如图所示的装置制取乙酸乙酯,请回答下列问题.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com