
| A. | 0.05mol•L-1的H2SO4 | B. | 0.1mol•L-1的KNO3 | ||
| C. | 0.1mol•L-1的KOH | D. | 0.1mol•L-1的NH4NO3 |
分析 水的电离过程是吸热过程,升高温度促进水的电离,水电离出的氢离子、氢氧根离子浓度会增大,酸、碱抑制水的电离,水解的盐会促进水的电离,据此分析溶液PH变化;
解答 解:A.0.05mol•L-1的H2SO4 溶液中氢离子浓度c(H+)=0.1mol/L,升温促进水的电离,但水电离出氢离子浓度很小和酸电离出的氢离子相比可以忽略,所以溶液的PH基本不发生变化,故A符合;
B.0.1mol•L-1的KNO3 溶液呈中性,升温水电离平衡中性进行,溶液中氢离子浓度增大,溶液PH减小,PH发生变化,故B不符合;
C.0.1mol•L-1的KOH溶液显碱性,升温促进电离离子积常数增大,溶液中氢离子浓度增大,溶液PH减小,故C不符合;
D.0.1mol•L-1的NH4NO3溶液中,铵根离子水解溶液显酸性,水解过程为吸热反应,升温促进水解平衡正向进行,氢离子浓度增大溶液PH减小,酸性增强,故D不符合;
故选A.
点评 本题考查了水的电离平衡影响因素分析,主要是溶液中离子积常数、盐类水解原理的理解应用,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2016-2017学年陕西省高一上第一次月考化学卷(解析版) 题型:计算题
将5.60 g铁投入100 mL某浓度的盐酸中,铁和盐酸恰好完全反应。
求:(1)5.6 0 g铁的物质的量
0 g铁的物质的量
(2)所用盐酸中HCl中的物质的量浓度
(3)反应中生成的H2在标准状况下的体积
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| ① | ② | ③ | ④ | |
| pH | 12 | 12 | 2 | 2 |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
| A. | 在①、②两溶液中分别加入氯化铵晶体,两溶液的pH均增大 | |
| B. | 将等体积的①和②两溶液分别加水稀释100倍,所得溶液的pH:①>② | |
| C. | 把①、④两溶液等体积混合后所得溶液中:[Cl-]>[NH4+]>[OH-]>[H+] | |
| D. | 将溶液②和溶液③等体积混合,混合后所得溶液的pH=7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲中沉淀一定比乙中的多 | B. | 甲中沉淀可能比乙中的多 | ||
| C. | 甲中沉淀一定比乙中的少 | D. | 甲中和乙中的沉淀不可能一样多 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
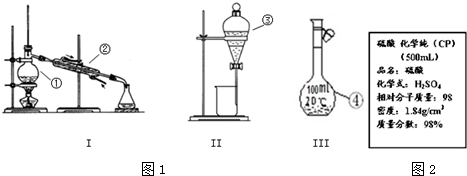
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某学生用0.1000 mol•L-1KOH液滴定未知浓度的醋酸,其操作分解为如下几步:
某学生用0.1000 mol•L-1KOH液滴定未知浓度的醋酸,其操作分解为如下几步:| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗NaOH溶液的体积(mL) | 20.05 | 20.00 | 18.80 | 19.95 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| Cu(OH)2 | CuOH | CuCl | Cu2O | |
| 颜色 | 蓝色 | 黄色 | 白色 | 砖红色 |
| Ksp(25℃) | 1.6×10-19 | 1.0×10-14 | 1.2×10-6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
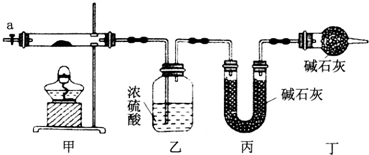
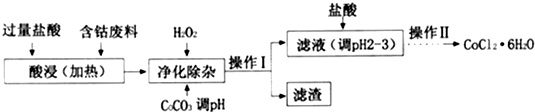
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | CO(OH)2 | Al(OH)3 |
| 开始沉淀(pH) | 2.3 | 7.5 | 7.6 | 3.4 |
| 完全沉淀(pH) | 4.1 | 9.7 | 9.2 | 5.2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com