
| A. | 减小压强 | B. | 升高温度 | C. | 增加SO2浓度 | D. | 加入催化剂 |
分析 A.减小压强,平衡向气体分子数目增大的方向移动;
B.升高温度,平衡向吸热反应方向移动;
C.增大反应物浓度,平衡正向移动;
D.使用催化剂不影响平衡移动.
解答 解:正反应为气体分子数目减小的放热反应.
A.减小压强,平衡向气体分子数目增大的方向移动,正反应为气体分子数目减小,即向逆反应方向移动,故A错误;
B.升高温度,平衡向吸热反应方向移动,正反应为放热反应,故平衡逆向移动,故B错误;
C.增大反应物浓度,平衡正向移动,故C正确;
D.使用催化剂加快反应速率,但不影响平衡移动,故D错误,
故选:C.
点评 本题考查化学平衡影响因素,比较基础,注意对平衡移动原理的理解,注意平衡移动是减弱“这种改变”,不是消除“改变”.


 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案科目:高中化学 来源: 题型:选择题
| A. | 放热反应在任意条件下都能自发进行 | |
| B. | 已知热化学方程式2A(g)+B(g)?2C (g)△H=-QkJ/mol (Q>0)将2molA(g)和1molB(g)置于一密闭容器中充分反应后放出QkJ的热量 | |
| C. | 1mol/L的盐酸与1mol/L的氨水、11mol/L的NaOH溶液等体积混合,充分反应,后者比前者放出的热量多 | |
| D. | BaCl2溶液中加过量H2SO4,溶液中一定不存在Ba2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol金属钠含有的电子数 | |
| B. | 0.012 kg 12C中含有的碳原子数 | |
| C. | 1 mol H2SO4完全溶于水后电离出的H+的个数 | |
| D. | 27 g Al与足量稀硫酸反应后生成H2的分子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.0gH2O与D2O的混合物中所含中子数为NA | |
| B. | 标准状况下1.4 g乙烯所含共用电子对数为0.25NA | |
| C. | 3 mol单质Fe完全转变为Fe3O4,失去8 NA个电子 | |
| D. | 50ml 12 mol•L-1盐酸与足量MnO2共热,转移的电子数为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,脱落酸(如图)可用作植物生长抑制剂,下
,脱落酸(如图)可用作植物生长抑制剂,下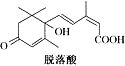 列对该物质的叙述正确的是( )
列对该物质的叙述正确的是( )| A. | 其分子式为C15H22O4 | |
| B. | 其属于芳香族化合物 | |
| C. | 能与氢氧化钠溶液反应,但不能与碳酸氢钠溶液反应 | |
| D. | 该物质在一定条件下可发生自身取代反应生成含七元环的物质. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
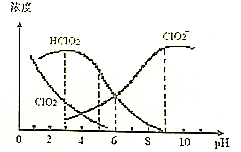
| A. | 向亚氯酸钠溶液加水稀释,溶液中n(ClO2)增大 | |
| B. | HClO2的电离平衡常数Ka=1.0×10-6 | |
| C. | NaClO2溶液中:c(Na+)+c(H+)>c(ClO2-)+c(Cl-) | |
| D. | pH=5时含氯元素的微粒浓度大小关系为:c(HClO2)>c(ClO2-)>c(Cl-)>c(ClO2) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
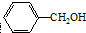 ,可用于制作香料和调味剂,还可以用作明胶、虫胶、酪蛋白及醋酸纤维等的溶剂,则苯甲醇的含苯环同分异构体有( )
,可用于制作香料和调味剂,还可以用作明胶、虫胶、酪蛋白及醋酸纤维等的溶剂,则苯甲醇的含苯环同分异构体有( )| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com