
 而与具体反应进行的途径无关。物质A在一定条件下可发生一系列转化,由右图判断下列
而与具体反应进行的途径无关。物质A在一定条件下可发生一系列转化,由右图判断下列
关系错误的是
A.A→F,△H = - △H 6
B.△H1+△H 2+△H 3+△H 4+△H 5+△H 6=1
C.C→F,|△H| = |△H 1+△H 2+△H 6 |
D.△H 1+△H 2+△H 3 = -△H 4-△H5-△H 6
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源: 题型:
某温度下,将Cl2通入KOH溶液中,反应得到KCl、KClO、KClO3的混合物,经测定c(ClO—): c(ClO3—)=1:3,则此反应中被还原氯元素与被氧化氯元素的质量比为( )
A.21:5 B.11:3 C.3:1 D.4:1
查看答案和解析>>
科目:高中化学 来源: 题型:
某氧化铁样品中含有少量的FeCl2杂质.现要测定其中铁元素的质量分数,按以下步骤进行实验:
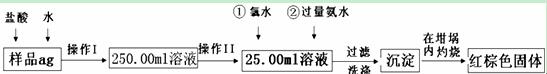
请根据图的流程,回答下列问题:
(1)操作I所用到玻璃仪器除烧杯、玻璃棒、胶头滴管以外,还必须有 ;
(填仪器名称)操作II必须用到的仪器是 。(填字母)
A.50ml烧杯 B.50ml量筒 C.100ml量筒 D.25ml滴定管
⑵再加入氨水的离子方程式为 。
⑶检验沉淀是否洗涤干净的操作是 。
⑷将沉淀物加热,冷却至室温,用天平称量其质量为b1g,再次加热并冷却至室温称量其质
量为b2g,若b1—b2=0.3,则接下来还应进行的操作是
。
⑸若坩埚的质量为W1g,坩埚与加热后固体的总质量为W2g,则样品中铁元素的质量分数
是 。
⑹有学生认为上述实验步骤太繁琐,他认为,将样品溶于水后充分搅拌,在空气中加热蒸干
燃烧称量即可,请你评价是否可行? 。(填“可行”或“不可行”)
查看答案和解析>>
科目:高中化学 来源: 题型:
反应3A(g)+B(g)  2C(g)+2D(g),在不同情况下测得反应速率如下,其中反应速率最快的是
2C(g)+2D(g),在不同情况下测得反应速率如下,其中反应速率最快的是
A.v (A)=0.15 mol·L-1·s-1 B.v (B)=0.3 mol·L-1·s-1
C.v (C)=0.5 mol·L-1·s-1 D.v (D)=0.4 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应A(g)+B C(g)+D,A和C均为无色气体,B和D的聚集状态未知,当反应到
C(g)+D,A和C均为无色气体,B和D的聚集状态未知,当反应到
达平衡时,下列叙述不正确的是
A.若保持恒容,充入C气体后混合气体颜色加深,则说明B是有颜色的气体
B.若升高温度,发现C的物质的量减少,则说明正反应为放热反应
C.若压缩容器,平衡不移动,则说明B和D一定都是气体
D.保持恒容,到达平衡后继续充入A会使B的转化率增大,A的转化率减少
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)已知某反应的平衡常数表达式为:K=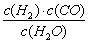 ,则它所对应反应的化学方程式是 ▲ 。
,则它所对应反应的化学方程式是 ▲ 。
(2) 合成甲醇的主要反应是:2H2(g)+CO(g) CH3OH(g) △H=-90.8 kJ·mol-1,t℃下此反应的平衡常数为160。此温度下,在密闭容器中开始只加入CO、H2,反应l0min后测得各组分的浓度如下:
CH3OH(g) △H=-90.8 kJ·mol-1,t℃下此反应的平衡常数为160。此温度下,在密闭容器中开始只加入CO、H2,反应l0min后测得各组分的浓度如下:
| 物质 | H2 | CO | CH3OH |
| 浓度(mol/L) | 0.2 | 0.1 | 0.4 |
(A)该时间段内反应速率v(H2)= ▲
(B)比较此时正、逆反应速率的大小:v正 ▲ v逆(填“>”、“<”或“=”)
(C)反应达到平衡后,保持其它条件不变,若只把容器的体积缩小一半,平衡向 ▲
(填“逆向”、“正向”或“不”)移动,平衡常数K ▲ (填“增大”、“减小” 或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
用10 mL的0.1 mol·L-1 BaCl2溶液恰好可使相同体积的硫酸铁(Fe2(SO4)3)、硫酸锌(ZnSO4)和硫酸钾(K2SO4)三种溶液中的硫酸根离子完全转化为硫酸钡沉淀,则三种硫酸盐溶液的物质的量浓度之比是
A.3∶2∶2 B 1∶2∶3 C 1∶3∶3 D 3∶1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
某工厂废水中含游离态氯,通过下列实验测定其浓度。①取水样10.0ml于锥形瓶中,加入10.0ml的K I溶液(足量),发生的反应为:Cl2+2KI=2KCl+I2,滴入指示剂2~3滴。②取一滴定管依次用自来水、蒸馏水洗净后,马上注入0.01mol·L-1Na2S2O3溶液,调整液面,记下读数。③将锥形瓶置于滴定管下进行滴定,发生的反应为:I2+2Na2S2O3=2NaI+ 2Na2S4O6 试回答下列问答:
⑴步骤①加入的指示剂是 。
⑵步骤②应使用 式滴定管。
⑶判断达到滴定终点的实验现象是 ;
⑷氯的实际浓度比所测浓度会偏小,造成误差的原因是
(5)用0.1032mol/L HCl溶液滴定未知浓度的NaOH溶液,下列情况对实验结果无影响的是
A、酸式滴定管未用标准盐酸溶液润洗 B、锥形瓶未用待测液润洗
C、滴定前滴定管尖嘴中有一气泡,滴定后气泡消失了
D、滴定时将标准液溅出锥形瓶外
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com