
【题目】某化学研究小组探究外界条件(催化剂、压强、温度)对化学反应mA(g)+nB(g)![]() qC(g)的速率和平衡的影响图像如图所示,下列判断正确的是
qC(g)的速率和平衡的影响图像如图所示,下列判断正确的是
A.由图可知,T1<T2,该反应的正反应为吸热反应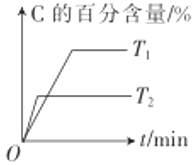
B.由图可知,该反应m+n<q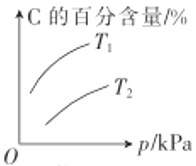
C.图中,点3的反应速率:v正>v逆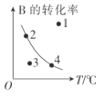
D.图中,若m+n=q,则曲线a一定使用了催化剂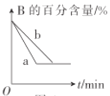
科目:高中化学 来源: 题型:
【题目】某小组以4H++4I-+O2=2I2+2H2O为研究对象,探究影响氧化还原反应因素。
实验 | 气体a | 编号及现象 |
| HCl | Ⅰ.溶液迅速呈黄色 |
SO2 | Ⅱ.溶液较快呈亮黄色 | |
CO2 | Ⅲ.长时间后,溶液呈很浅的黄色 | |
空气 | Ⅳ.长时间后,溶液无明显变化 |
(1)实验Ⅳ的作用是______________。用CCl4萃取Ⅰ、Ⅱ、Ⅲ、Ⅳ的溶液,萃取后下层CCl4的颜色均无明显变化。
(2)取萃取后上层溶液,用淀粉检验:Ⅰ、Ⅲ的溶液变蓝;Ⅱ、Ⅳ的溶液未变蓝。溶液变蓝说明Ⅰ、Ⅲ中生成了______________。
(3)查阅资料:I2易溶于KI溶液。下列实验证实了该结论并解释Ⅰ、Ⅲ的萃取现象。
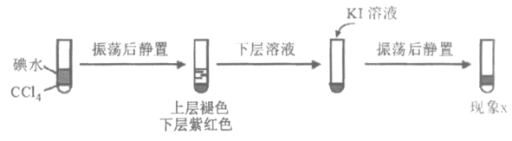
现象x是______________。
(4)针对Ⅱ中溶液未检出I2的原因,提出三种假设:
假设1:溶液中c(H+)较小。小组同学认为此假设不成立,依据是______________。
假设2:O2只氧化了SO2,化学方程式是______________。
假设3:I2不能在此溶液中存在。
(5)设计下列实验,验证了假设3,并继续探究影响氧化还原反应的因素。
i.取Ⅱ中亮黄色溶液,滴入品红,红色褪去。
ii.取Ⅱ中亮黄色溶液,加热,黄色褪去,经品红检验无SO2。加入酸化的AgNO3溶液,产生大量AgI沉淀,长时间静置,沉淀无明显变化。
iii.取Ⅱ中亮黄色溶液,控制一定电压和时间进行电解,结果如下。
电解时间/min | 溶液 | 阳极 | 阴极 |
t1 | 黄色变浅、有少量SO42- | 检出I2,振荡后消失 | H2 |
| 溶液无色、有大量SO42- | 检出I2,振荡后消失 | H2 |
结合化学反应,解释上表中的现象:______________。
(6)综合实验证据说明影响I-被氧化的因素及对应关系______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~G各物质间的关系如图,其中B、D为气态单质。

请回答下列问题。
(1)物质C和E的名称分别为_______、_______;
(2)可选用不同的A进行反应①,若能在常温下进行,其化学方程式为___________________;若只能在加热情况下进行,则反应物A应为_______;
(3)MnO2在反应①和反应②中的作用分别是_______、_______;
(4)新配制的F溶液应加入_______以防止其转化为G。检验G溶液中阳离子的常用试剂是_______,实验现象为_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示操作能实现实验目的的是( )
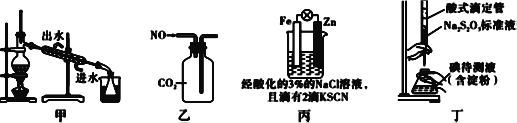
A. 用图甲装置分离碘和四氯化碳,在锥形瓶中收集到碘单质
B. 用图乙装置收集NO气体
C. 用图丙装置验证牺牲阳极的阴极保护法
D. 用图丁装置测定待测液中I2的含量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生为测定未知浓度的硫酸溶液,实验如下:用1.00mnL待测硫酸溶液配制100mL稀H2SO4,取上述配好的稀H2SO425.00mL,用0.1400mol/L的NaOH溶液滴定,滴定终止时消耗NaOH溶液150mL。
(1)该学生用标准0.1400mol/LNaOH溶液滴定硫酸的实验操作如下:
A.用酸式滴定管取25.00mL稀H2SO4,注入锥形瓶中,加入指示剂
B.用待测定的溶液润洗酸式滴定管
C.用蒸馏水洗干净滴定管
D.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管刻度“0”以上2-3cm处,再把碱式滴定管固定好,调节液面至刻度“0”或“0”刻度以下
E.检查滴定管是否漏水
F.另取锥形瓶,再重复操作一次
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度
①滴定操作的正确顺序是(用序号填写):___→___→D→B→___→___→___。
②在G操作中如何确定终点?___。
(2)碱式滴定管用蒸馏水洗涤后,未用标准液润洗导致滴定结果偏大,原因是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是
A.工业上用熔融的金属钠制取金属钾:KCl(l)+Na(l)![]() NaCl(l)+K(g)
NaCl(l)+K(g)
B.对于反应2HI(g)![]() H2(g)+I2 (g),达到平衡后缩小容器体积可使体系颜色变深
H2(g)+I2 (g),达到平衡后缩小容器体积可使体系颜色变深
C.氨水中加入NaOH固体有利于氨气的溢出
D.实验室用排饱和食盐水的方法来收集氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NH3和CuO高温时反应能生成Cu和N2,某实验小组欲利用如图所示实验装置测定某5 g CuO(含Cu)样品的纯度
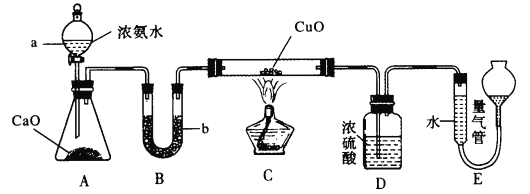
请回答下列问题:
(1)锥形瓶中的生石灰可用试剂____代替,仪器b中所盛试剂为______(填名称)。
(2)装置C中硬质玻璃管中发生反应的化学方程式为___________
(3)装置D的作用为________
(4)读取装置E中量气管中的气体体积时应注意的事项为_______
若装置E中所得气体体积在标准状况下时为336 mL,则样品中CuO的含量为___%。若读数时左边液面高于右边液面,则测得CuO含量将____(填“偏高”“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依折麦布(Ezetimibe)是一种高效的的胆固醇吸收抑制剂,合成它的一种重要中间体M的结构如图所示。某兴趣小组以甲苯和戊二酸酐为原料,设计了以下合成路线,部分条件和产物已略去。
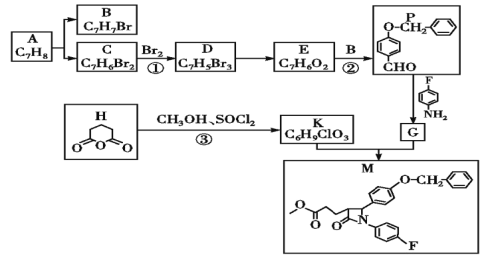
已知:Ⅰ.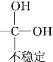
![]()
![]()
Ⅱ.![]() +RNH2
+RNH2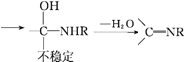
Ⅲ.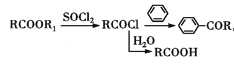 (R1为H或烃基)
(R1为H或烃基)
请回答:
(1)物质A的结构简式为______。
(2)下列说法正确的是______。
A.由甲苯制B需用Fe作催化剂
B.物质H水解后产物的最简单同系物为乙二酸
C.反应①②③均为取代反应
D.1mol物质C最多能与2molNaOH反应
(3)写出反应②的化学方程式:_____。
(4)写出同时符合下列条件的比![]() 多2个碳的同系物N的所有同分异构体的结构简式:______。
多2个碳的同系物N的所有同分异构体的结构简式:______。
①属芳香族化合物②能与酸反应③1H—NMR谱中出现3个峰
(5)设计以苯和乙烯为原料制备另一种医药中间体二苯甲酮(![]() )的合成路线:_____(用流程图表示,无机试剂任选)。
)的合成路线:_____(用流程图表示,无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案中,能达到相应实验目的的是
实验方案 |
|
|
|
|
目的 | A.比较乙醇分子中羟基氢原子和水分子中氢原子的活泼性 | B.除去乙烯中的二氧化硫 | C.制银氨溶液 | D.证明碳酸酸性强于苯酚 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com