
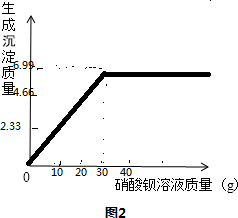
| 加入硝酸钡溶液质量/g | 10 | 20 | 45 | 55 |
| 产生白色沉淀质量/g | 2.33 | 4.66 | 6.99 | 6.99 |

| ||
| ||
 ,故答案为:
,故答案为: ;
;| 2.33g |
| 233g/mol |
| 2.61g |
| 10g |


科目:高中化学 来源: 题型:
| A、Ca2+、H+、Cl-、HCO3- |
| B、H+、K+、S2-、ClO- |
| C、Fe2+、Na+、SO42-、NO3- |
| D、Cu2+、Ag+、SO42-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向某无色溶液中滴加酚酞试液,溶液变红;结论:该溶液一定呈碱性 |
| B、向某溶液中加入盐酸,放出不能使品红溶液褪色的气体;结论:溶液中一定含有CO32- |
| C、某无色溶液焰色反应呈黄色;结论:溶液中一定含有Na+、没有K+ |
| D、向某无色溶液中加入碳酸钠溶液,产色白色沉淀;结论:溶液中一定含有Ca2+或Ba2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | A | B | C | D |
| 原子半径/nm | 0.102 | 0.077 | 0.117 | 0.075 |
| 单质沸点/℃ | 444.6 | 4827 | 2355 | -195.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 稀溶液中含有Fe(NO2)3、Cu(NO2)2、HNO3,向其中逐渐加入铁粉,溶液中Fe2+的浓度(纵坐标/mol?L-1)与加入铁粉的物质的量(横坐标/mol)之间的关系如图所示.则溶液中Fe(NO2)3、Cu(NO2)2、HN03物质的量浓度之比为( )
稀溶液中含有Fe(NO2)3、Cu(NO2)2、HNO3,向其中逐渐加入铁粉,溶液中Fe2+的浓度(纵坐标/mol?L-1)与加入铁粉的物质的量(横坐标/mol)之间的关系如图所示.则溶液中Fe(NO2)3、Cu(NO2)2、HN03物质的量浓度之比为( )| A、1:1:1 |
| B、1:3:1 |
| C、3:3:8 |
| D、1:1:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、卤素单质的熔点和沸点随核电荷数的增加逐渐升高 |
| B、碱金属单质与水反应生成碱和氢气 |
| C、碱金属单质在空气中燃烧都可生成过氧化物 |
| D、卤素的氢化物的还原性性随核电荷数的增加逐渐增强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com