
科目:高中化学 来源:湖南省长郡中学2012届高三第五次月考化学试题 题型:043
| |||||||||||
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:058
人的纯净胃液是一种无色而呈酸性反应的液体,PH在0.9~1.5之间,
液中含有大量盐酸,其中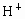 浓度比血液高几百万倍.试回答下列问题:
浓度比血液高几百万倍.试回答下列问题:
(1)若胃液酸度增高就患胃酸过多症,下列物质不适宜用来治疗胃酸过多症药物的主要成分是________
|
A.小苏打粉 |
B.氢氧化铝粉 |
|
C.氧化钙粉 |
D.纯碳酸钙粉 |
(2)胃镜检查发现胃有少量出血,说明胃溃疡已深及__________(胃结构).胃溃疡病患者胃酸过多可考虑选用(1)中的______________.
(3)三硅酸镁晶体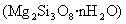 是一种常见的用来治疗胃溃疡的药物,该药物不溶于水,但能中和胃酸,且作用持久.写出该药物中和胃
是一种常见的用来治疗胃溃疡的药物,该药物不溶于水,但能中和胃酸,且作用持久.写出该药物中和胃
酸的化学方程式:_____________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com