
【题目】化合物C是一种合成药品的中间体,其合成路线为:
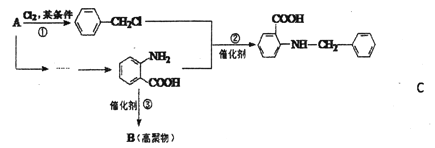
已知:
(1)写出![]() 中宮能团的名称_____________。
中宮能团的名称_____________。
(2)写出反应①的化学方程式_________________。
(3)反成②属于_______反应(填有机反应类型)。
(4)D是比![]() 多一个碳的同系物,则满足下列条件的D的间分异构体共有______种,写出一种满足条件且含4种不同氢原+的同分异构体的结构简式 __________。
多一个碳的同系物,则满足下列条件的D的间分异构体共有______种,写出一种满足条件且含4种不同氢原+的同分异构体的结构简式 __________。
①显弱碱性,易被氧化 ②分子内含有苯环 ③能发生水解反应
(5)请你设计由A合成B的合成路线。 __________
提示:①合成过程中无机试剂任选;②合成路线表示方法示例如下:
![]()
【答案】(1)氨基、羧基(每个1分,共2分)
(2)![]() +Cl2
+Cl2![]()
![]() +HCl(共2分,无“条件”扣1分,其它错不得分)
+HCl(共2分,无“条件”扣1分,其它错不得分)
(3)取代 (1分) (4)19(2分),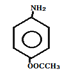 (2分)(5)(共5分)
(2分)(5)(共5分)

(答对一步得1分,出现错误后面不得分。合成顺序不能颠倒,无“条件”有一处扣1分。)
【解析】试题分析:(1)根据有机物![]() 的结构简式可知,分子中官能团的名称为氨基和羧基。
的结构简式可知,分子中官能团的名称为氨基和羧基。
(2)反应②是甲苯分子中甲基上氢原子被氯原子取代,反应的化学方程式为![]() +Cl2
+Cl2![]()
![]() +HCl。
+HCl。
(3)根据反应前后有机物结构简式的变化可知,该反应是氨基中的氢原子被![]() 取代,因此该反应是取代反应。
取代,因此该反应是取代反应。
(4)D是比![]() 多一个碳的同系物,则D比
多一个碳的同系物,则D比![]() 多1个CH2原子团。①显弱碱性,易被氧化,说明含有氨基;②分子内含有苯环;③能发生水解反应,说明含有酯基。因此如果苯环上有2个取代基,则可以是-CH2OOCH和-NH2,分为邻、间、对三种;也可以是-OOCCH3和-NH2,分为邻、间、对三种;还可以是-COOCH3和-NH2,分为邻、间、对三种;如果含有三个取代基,则分别为-NH2、-CH3和-OOCH,又有10种,所以共计是19种;又因为含4种不同氢原子,所以满足条件的D的同分异构体的结构简式可以是
多1个CH2原子团。①显弱碱性,易被氧化,说明含有氨基;②分子内含有苯环;③能发生水解反应,说明含有酯基。因此如果苯环上有2个取代基,则可以是-CH2OOCH和-NH2,分为邻、间、对三种;也可以是-OOCCH3和-NH2,分为邻、间、对三种;还可以是-COOCH3和-NH2,分为邻、间、对三种;如果含有三个取代基,则分别为-NH2、-CH3和-OOCH,又有10种,所以共计是19种;又因为含4种不同氢原子,所以满足条件的D的同分异构体的结构简式可以是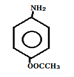 ,氨基对位的取代基也可以是-COOCH3。
,氨基对位的取代基也可以是-COOCH3。
(5)由于氨基易被氧化,所以首先引入硝基后先氧化甲基,最后再还原硝基为氨基,所以正确的合成路线为 。
。


科目:高中化学 来源: 题型:
【题目】能源的开发、利用与人类社会的可持续发展息息相关,充分利用好能源是摆在人类面前的重大课题。
Ⅰ.已知:①Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) ΔH=a kJ·mol-1
②CO(g)+l/2O2(g)=CO2(g) ΔH=b kJ·mol-1
③C(石墨)+O2(g)=CO2(g) ΔH=c kJ·mol-1
则反应4Fe(s)+3O2(g)=2Fe2O3(s)的焓变ΔH=______________kJ·mol-1。
Ⅱ.依据原电池的构成原理,下列化学反应在理论上可以设计成原电池的是_____(填序号)。
C(s)+CO2(g)=2CO(g) ΔH>0
B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH<0
C.2H2O(l)=2H2(g)+O2(g) ΔH>0
D.CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH<0
若以稀硫酸为电解质溶液,则该原电池的正极反应式为______________________。
Ⅲ.金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,充分燃烧时生成二氧化碳,反应中放出的热量如下图所示。

①在通常状况下,金刚石和石墨中________(填“金刚石”或“石墨”)更稳定,石墨的燃烧热为________。
②12 g石墨在一定量空气中燃烧,生成气体36 g,该过程放出的热量________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)一定温度下,向1 L 0.1 mol·L-1CH3COOH溶液中加入0.1 mol CH3COONa固体,则醋酸的电离平衡 向________(填“正”或“逆”)反应方向移动;溶液中![]() 的值________(填“增大”、“减小”或“不变”)。
的值________(填“增大”、“减小”或“不变”)。
(2)氨气的水溶液称为氨水,其中存在的主要溶质微粒是NH3·H2O。
已知:a.常温下,醋酸和NH3·H2O的电离平衡常数均为1.74×10-5 mol·L-1;
b.CH3COOH+NaHCO3===CH3COONa+CO2↑+H2O。
则CH3COONH4溶液呈________性(填“酸”、“碱”或“中”,下同),NH4HCO3溶液呈________性,NH4HCO3溶液中物质的量浓度最大的离子是________(填化学式)。
(3)99 ℃时,KW=1.0×10-12 mol2·L-2,该温度下测得0.1 mol·L-1Na2A溶液的pH=6。
①H2A在水溶液中的电离方程式为________________。
②该温度下,将0.01 mol·L-1H2A溶液稀释到20倍后,溶液的pH=__________。
③体积相等、pH=1的盐酸与H2A溶液分别与足量的Zn反应,产生的氢气____________。
A.盐酸多 B.H2A多 C.一样多 D.无法确定
④将0.1 mol·L-1H2A溶液与0.2 mol·L-1氨水等体积混合,完全反应后溶液中各离子浓度从大到小的顺序为___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,用0.0500 mol·L-1H2C2O4(二元弱酸)溶液滴定 25.00 mL 0.100 0 mol L-1NaOH溶液所得滴定曲线如右图。下列说法正确的是( )

A. 点①所示溶液中:c(H+)+c(H2C2O4)+ c(HC2O4-)=c(OH-)
B. 点②所示溶液中:c(HC2O4-)+c(C2O42-)=c(Na+)
C. 点③所示溶液中:c(Na+)>c(HC2O4-)>c(H2C2O4)>c(C2O42-)
D. 滴定过程中可能出现:c(Na+) > c(C2O42-) =c(HC2O4-)>C(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有甲、乙两位同学,他们一起做了如图所示的水果电池实验,测得数据如下表:
实验次数 | 电极材料 | 水果品种 | 电极间距/cm | 电压/mV | |
1 | 锌 | 铜 | 菠萝 | 3 | 900 |
2 | 锌 | 铜 | 苹果 | 3 | 650 |
3 | 锌 | 铜 | 柑橘 | 3 | 850 |
4 | 锌 | 铜 | 西红柿 | 3 | 750 |
5 | 锌 | 铝 | 菠萝 | 3 | 650 |
6 | 锌 | 铝 | 苹果 | 3 | 450 |
甲同学提出的问题,乙同学解释不正确的是
①甲:实验6中的负极反应如何写? 乙:铝为负极:Al-3e-===Al3+
②甲:实验1、5电流方向为什么相反? 乙:实验1中锌为负极,电流由铜经导线流向锌;实验5中铝为负极,铝失去电子,电流由锌经导线流向铝
③甲:水果电池的电压与哪些因素有关? 乙:只跟水果的品种有关。
A. ③ B. ① C. ①②③ D. ②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某短周期元素原子的第三电子层排布有5个电子,该元素在周期表中位于
A. 第二周期ⅣA族 B. 第二周期ⅤA族
C. 第三周期ⅣA族 D. 第三周期ⅤA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,在25 mL 0.1 mol·L-1的NaOH溶液中逐渐加入0.2 mol·L-1 CH3COOH溶液,混合溶液pH的变化曲线如图所示,下列分析结论正确的是( )
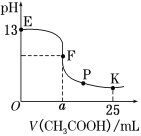
A.a=12.5,且混合溶液pH=7
B.对应曲线上E、F之间的任何一点,溶液中都有 c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
C.K点时,c(CH3COO-)+c(CH3COOH)=2c(Na+)
D.P点时,c(CH3COO-)>c(Na+)>c(H+)=c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中需要2mol/L的NaCl溶液950mL,配制时应选用的容量瓶的规格和称取NaCl质量分别是( )
A. 950mL,111.2g B. 950mL,117.0g
C. 1000mL,117.0g D. 1000mL,111.2g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com