
【题目】取三份浓度均为0.1 mol/L,体积均为1 L 的CH3COONa 溶液中分别加入NH4Cl 固体、CH3COONH4固体、HCl 气体后所得溶液pH 变化曲线如图(溶液体积变化忽略不计)下列说法不正确的是
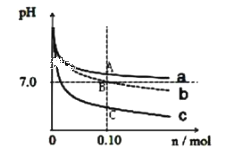
A.曲线 a、b、c 分别代表加入 CH3COONH4、NH4Cl、HCl
B.由图可知 Ka(CH3COOH)=Kb(NH3﹒H2O)=1×10-7
C.A点处 c(CH3COO-)>c(Na+)> c(NH4+)> c(OH-)> c(H+)
D.C点处 c(CH3COO-)+c(Cl-)+c(OH-)>0.1mol/L
【答案】B
【解析】
醋酸钠为强碱弱酸盐,因醋酸根离子水解,溶液呈碱性。往溶液中加入氯化铵固体,由于铵根离子水解呈酸性,故随着氯化铵的加入,溶液将由碱性逐渐变为酸性,由于水解微弱,所得溶液酸性较弱,符合的曲线为b;往溶液中通入氢化氯气体,随着气体的通入溶液由碱性转变为酸性,由于氯化氢为强酸,通入量较大时,溶液的酸性较强,符合的曲线为c;加入醋酸铵固体所对应的变化曲线为a,据此结合电荷守恒及盐的水解原理分析。
A.根据分析可知,曲线a代表醋酸铵、曲线b代表氯化铵、曲线c代表氯化氢,故A正确;
B.当加入固体的物质的量为0.1mol时,曲线b对应的pH值等于7,说明等浓度的醋酸根离子的水解程度与铵根离子相同,即Ka(CH3COOH)=Kb(NH3﹒H2O),但无法计算其电离平衡常数,故B错误;
C.A点含有的溶质为0.1molCH3COONa与0.1molCH3COONH4,溶液的pH>7,则c(OH)>c(H+),醋酸根离子的水解程度较小,则c(CH3COO)>c(Na+),铵根离子部分水解,则c(Na+)>c(NH4+),溶液中离子浓度的大小关系为:c(CH3COO-)>c(Na+)> c(NH4+)> c(OH-)> c(H+),故C正确;
D.C点通入0.1molHCl,与0.1mol醋酸钠反应得到0.1molCH3COOH与0.1molNaCl,c(Cl)=c(Na+)=0.1mol/L,则c(CH3COO)+c(Cl)+c(OH)>0.1mol/L,故D正确;
故选:B。


 名题金卷系列答案
名题金卷系列答案科目:高中化学 来源: 题型:
【题目】实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是

选项 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
A | 浓氨水 | CaO | NH3 | H2O |
B | 稀硫酸 | Na2SO3 | SO2 | NaOH溶液 |
C | 稀硝酸 | Cu | NO2 | H2O |
D | 浓盐酸 | KMnO4 | Cl2 | NaOH溶液 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是电解CuCl2溶液的装置,其中c、d为石墨电极。则下列有关的判断正确的是( )
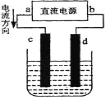
A. 电解过程中,d电极质量增大
B. a为阳极、b为阴极
C. a为负极、b为正极
D. 电解过程中,氯离子浓度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池是将化学能转化为电能的装置。
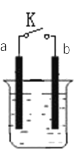
I. a为铜片,b为铁片,烧杯中是稀硫酸溶液
(1)当开关K断开时产生的现象为_______ ;当开关K闭合时,产生的现象为_________。
A.a不断溶解 B.b不断溶解 C.a上产生气泡 D.b上产生气泡 E.溶液逐渐变蓝
(2)闭合开关K,反应一段时间后断开开关K,经过一段时间后,下列叙述不正确的是___________ 。
A.溶液中H+浓度减小 B.正极附近![]() 浓度逐渐增大
浓度逐渐增大
C.溶液中含有FeSO4 D.溶液中![]() 浓度基本不变
浓度基本不变
II.FeCl3常用于腐蚀印刷电路铜板,反应过程的离子方程式为 ________ ,若将此反应设计成原电池,请写出该原电池负极电极反应为_______,正极电极反应为______。
III.如图是氢氧燃料电池构造示意图。
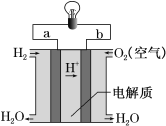
下列说法不正确的是______
A.a极是负极
B.电子由b通过溶液流向a
C.该电池总反应是2H2+O2=2H2O
D.氢氧燃料电池是环保电池
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组的同学为了制取NO并探究其性质,进行了如下实验。
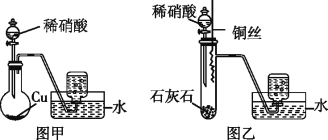
试回答下列问题:
(1)某同学用图甲装置进行实验,收集到无色气体,由此确定铜和稀硝酸反应生成NO气体。该同学的推断不合理的理由是__________ (用化学方程式表示)。
(2)另一名同学设计了图乙装置进行实验,步骤如下:①在大试管中放入适量石灰石,加入过量稀硝酸;②待石灰石反应完全,将铜丝浸入过量的稀硝酸中;③一段时间后,观察到大试管中气体始终为无色,收集反应产生的气体。其中步骤①的作用是___________。
(3)当过量的铜与稀硝酸完全反应后,再加20%的稀硫酸,铜片上又有气泡产生,稀硫酸的作用是___(填选项编号),反应的离子方程式为__________。
a.还原剂 b.氧化剂 c.提供氢离子 d.提供热能
(4)某些资料认为NO不能与Na2O2反应。有同学提出质疑,他认为NO易与O2发生反应,应该更容易被Na2O2氧化。
查阅资料:a.2NO+Na2O2=2NaNO2
b.6NaNO2+3H2SO4(稀)=3Na2SO4+2HNO3+4NO↑+2H2O
c.酸性条件下,NO能被MnO![]() 氧化成NO
氧化成NO![]()
该同学利用图中装置来探究NO与Na2O2的反应(装置可重复使用)。
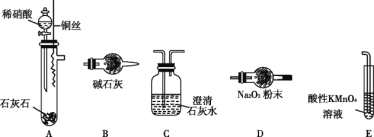
①装置的连接顺序为A→_________,装置E的作用是 __________。
②充分反应后,欲检验装置D中是否生成了NaNO2,请简述实验方案_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属及其化合物在生产生活等各个领域有着广泛的应用。
(1)钛具有良好的金属性能。钛基态原子中电子占据能级个数为______。与钛同周期的元素中,基态原子的未成对电子数与钛相同的还有______种。钛比钢轻、比铝硬,是一种新兴的结构材料,钛硬度比铝大的可能原因是________。
(2)有一种氮化钛晶体的晶胞与NaCl晶胞相似,该晶胞中N、Ti之间的最近距离为a×10-10cm,则该氮化钛的密度为_________g·cm-3(NA为阿伏加德罗常数的值,只列计算式)。
(3)Li是最轻的固体金属,采用Li作为负极材料的电池具有小而轻、能量密度大等优良性能,得到广泛应用。Li2O是尚子晶体,其晶格能可通过图(a)的Bom-Haber循环计算得到。

Li原子的第一电离能为______kJ·mol-1,O==O键键能为______kJ·mol-1,Li2O晶格能为_______kJ·mol-1。
(4)Zn可形成多种化合物,其中立方ZnS晶胞结构如下图,其阴离子(S2-)按面心立方密堆积排布,立方ZnS的配位数与NaCl不同,这是由__________因素决定的。
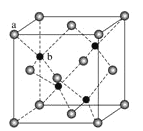
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表示物质结构的化学用语正确的是( )
A. 乙烯的结构简式:CH2CH2 B. 异丙基的结构简式:-CH(CH3)2
C. 羟基的电子式: ![]() D. 新戊烷的结构简式:
D. 新戊烷的结构简式:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是氯化铯晶体的晶胞(晶体中的最小重复单元),已知晶体中两个最近的Cs+离子核间距离为a cm,氯化铯的相对分子质量为M,NA为阿伏加德罗常数,则氯化铯晶体密度是( )

A. ![]() g/cm3 B.
g/cm3 B. ![]() g/cm3 C.
g/cm3 C. ![]() g/cm3 D.
g/cm3 D. ![]() g/cm3
g/cm3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.足量的KI溶液与FeCl3溶液反应后,用CCl4萃取其中的I2,分液,在水溶液中滴加KSCN溶液仍呈血红色,说明该反应有一定的限度
B.在一定条件下,一份双氧水样品经过2h,H2O2的浓度从0.05molL-1下降到0.03molL-1,H2O2在这2h中分解的平均反应速率约为0.015molL-1h-1
C.其他条件相同时,升高温度,对于吸热反应,反应速率加快,对于放热反应,反应速率减慢
D.一定条件下,固定体积的密闭容器中发生反应A(g)+B(g)2C(g),当容器内A、B、C的浓度之比为1:1:2时,该反应处于平衡状态
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com