
(6分)在标准状况下,CO和CO2的混合气体共33.6L,质量为50g。请回答下列三个问题:
(1)两种气体总的物质的量为多少?
(2)CO的质量为多少?
(3)C与O原子个数比为多少?
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:
| 醇 |
| △ |
| 醇 |
| △ |
| 水 |
| △ |
| 水 |
| △ |


查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
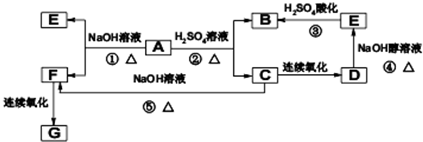
| ||
| ||
| 1 |
| 3 |
| 3 |
| 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(9分)(1)在标准状况下,①6.72 L CH4气体;②3.01×1023个 HCl气体分子;③13.6 g H2S气体;④0.2 mol NH3,下列对这四种气体所含分子物质的量的关系从小到大的排列是(用上述数字序号表示)_______ ______________________________。
(2)粗盐经提纯后得到NaCl溶液,再经蒸发、结晶、烘干得精盐。
①蒸发操作中使用到的仪器除铁架台(带铁圈)外,还需要的仪器名称为(写出三种)_________________。
②该同学将所得精盐配成溶液,用于另一实验:实验中需要用60 mL 2 mol/L的NaCl溶液,配制过程中用托盘天平称取的精盐质量为________,该同学将精盐放在天平的右盘中称量好后,配制成溶液,则该溶液的浓度________2mol·L-1(填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年云南省保山曙光中学高一上学期期末考试化学试卷 题型:填空题
(9分)(1)在标准状况下,①6.72 L CH4气体;②3.01×1023个 HCl气体分子;③13.6 g H2S气体;④0.2 mol NH3,下列对这四种气体所含分子物质的量的关系从小到大的排列是(用上述数字序号表示)_______ ______________________________。
(2)粗盐经提纯后得到NaCl溶液,再经蒸发、结晶、烘干得精盐。
①蒸发操作中使用到的仪器除铁架台(带铁圈)外,还需要的仪器名称为(写出三种)_________________。
②该同学将所得精盐配成溶液,用于另一实验:实验中需要用60 mL 2 mol/L的NaCl溶液,配制过程中用托盘天平称取的精盐质量为________,该同学将精盐放在天平的右盘中称量好后,配制成溶液,则该溶液的浓度________2 mol·L-1(填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源:2014届云南省高一上学期期末考试化学试卷 题型:填空题
(9分)(1)在标准状况下,①6.72 L CH4气体;②3.01×1023个 HCl气体分子;③13.6 g H2S气体;④0.2 mol NH3,下列对这四种气体所含分子物质的量的关系从小到大的排列是(用上述数字序号表示)_______ ______________________________。
(2)粗盐经提纯后得到NaCl溶液,再经蒸发、结晶、烘干得精盐。
①蒸发操作中使用到的仪器除铁架台(带铁圈)外,还需要的仪器名称为(写出三种)_________________。
②该同学将所得精盐配成溶液,用于另一实验:实验中需要用60 mL 2 mol/L的NaCl溶液,配制过程中用托盘天平称取的精盐质量为________,该同学将精盐放在天平的右盘中称量好后,配制成溶液,则该溶液的浓度________2 mol·L-1(填“>”、“<”或“=”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com