
c(Co(H2O
| ||
c(CoC
|
c2(Cr
| ||
c(Cr2
|
c2(Cr
| ||
c(Cr2
|
c(Co(H2O
| ||
c(CoC
|


 学业测评一课一测系列答案
学业测评一课一测系列答案科目:高中化学 来源: 题型:
| A、化石燃料的液化与气化技术非常成熟且大量应用时,就无需开发新能源 |
| B、绿色化学的核心是应用化学原理对环境污染进行治理 |
| C、在食用盐中添加适量的碘酸钾(KIO3)不符合食品的安全要求 |
| D、垃圾是放错地方的资源,应当分类处理和回收利用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
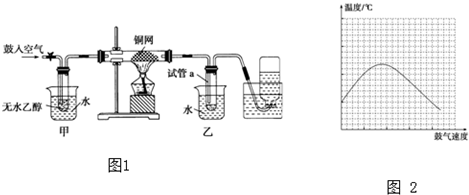
查看答案和解析>>
科目:高中化学 来源: 题型:
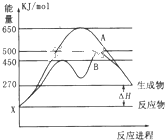 (1)某可逆反应在不同条件下的反应历程分别为A、B,如图所示.
(1)某可逆反应在不同条件下的反应历程分别为A、B,如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
| 高温 |
| 序号 | 碳粉的质量/g | 氮气的物质的量/mol | 二氧化硅的质量/g | 二氧化硅的形状 | 反应温度/℃ | 达到平衡所用的时间/s | 平衡时氮化硅的质量/g |
| 1 | 7.2 | 3.0 | 12.0 | 大颗粒 | 1500 | 300 | m1 |
| 2 | 7.2 | 3.0 | 12.0 | 大颗粒 | 1550 | 200 | m2 |
| 3 | 7.2 | 3.0 | 12.0 | 小颗粒 | 1550 | 120 | m3 |
| 4 | 7.2 | 3.0 | 12.0 | 小颗粒 | 1600 | 80 | 6.3 |
| 5 | 7.2 | 3.0 | 12.0 | 粉末 | 1550 | t1 | 7.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
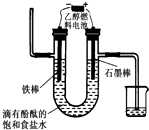 据报道,一定条件下由二氧化碳和氢气合成乙醇已成为现实.
据报道,一定条件下由二氧化碳和氢气合成乙醇已成为现实.查看答案和解析>>
科目:高中化学 来源: 题型:
 如图所示为某化学兴趣小组设计的乙醇催化氧化及其产物检验的实验装置(图中加热仪器、铁架台、铁夹等均未画出).
如图所示为某化学兴趣小组设计的乙醇催化氧化及其产物检验的实验装置(图中加热仪器、铁架台、铁夹等均未画出).查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4++H2O?NH3?H2O+H+ |
| B、HS-+H2O?H3O++S2- |
| C、HS-+H2O?H2S+OHˉ |
| D、NH4++2H2O?NH3?H2O+H3O+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com