
【题目】氮化锶(Sr3N2)在工业上有广泛应用。已知氮化锶遇水剧烈反应产生氢氧化锶和氨气。
锶和镁位于同主族且锶比镁活泼, 锶与氮气在加热条件下反应产生氮化锶。某学习小组拟设计两套方案制备氮化锶:
方案Ⅰ:根据下列装置制备氮化锶。
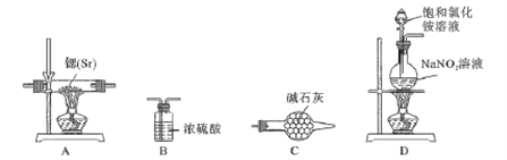
已知:实验室用饱和氯化铵溶液和亚硝酸钠溶液共热制备氮气。
回答下列问题:
(1)气流从左至右,选择装置并排序为___________(填字母表示)。
(2)写出实验室制备N2的化学方程式____________
(3)实验时先点燃_____处酒精灯(填“A”或“D”),一段时间后,点燃另一只酒精灯。
(4)氮化锶遇水发生反应的化学方程式为____________
方案Ⅱ:某氮气样品可能含有少量的CO、CO2、O2等气体杂质,某同学设计如下装置制备氮化锶(各装置盛装足量试剂)。已知:醋酸二氨合亚铜CH3COO[Cu(NH3)2]溶液能定量吸收CO,但易被O2氧化,失去吸牧CO能力;连苯三酚鹹性溶液能定量吸收O2.
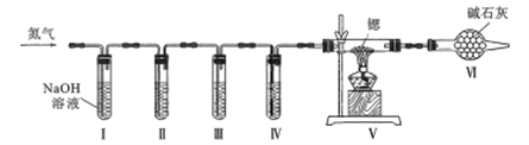
(5)试管Ⅱ盛装的试剂是__________填代号)。
a.连苯三酚碱性溶液b.醋酸二氨合亚铜溶液 C.浓巯酸d.赤热铜粉
装置Ⅵ的作用是_______________
(6)测定产品纯度:取wg产品,向其中加入适量的水。将产生的气体全部通人到依硫酸中,依硫酸增重mg,则产品纯度为__(用代数式表示)。有同学认为上述方法使测得产品纯度偏高,其原因是___________
【答案】 D、B、A、C NH4Cl+NaNO2![]() NaCl+N2↑+2H2O D Sr3N2+6H2O=3Sr(OH)3+2NH3↑ a 吸收空气中CO和H2O(g) 146m/(17w)×100% 氨气中混有水蒸气
NaCl+N2↑+2H2O D Sr3N2+6H2O=3Sr(OH)3+2NH3↑ a 吸收空气中CO和H2O(g) 146m/(17w)×100% 氨气中混有水蒸气
【解析】(1)气流从左至右,先制取氮气,再用浓硫酸干燥,与锶反应,用碱石灰防止空气中水和二氧化碳气体进入A中,选择装置并排序为 D、B、A、C 。(2)实验室用饱和氯化铵溶液和亚硝酸钠溶液共热制备氮气,实验室制备N2的化学方程式 NH4Cl+NaNO2![]() NaCl+N2↑+2H2O;(3)实验时先点燃D处酒精灯(填“A”或“D”),赶走装置中的空气,一段时间后,点燃另一只酒精灯。(4)氮化锶遇水发生反应的化学方程式为 Sr3N2+6H2O=3Sr(OH)3+2NH3↑。
NaCl+N2↑+2H2O;(3)实验时先点燃D处酒精灯(填“A”或“D”),赶走装置中的空气,一段时间后,点燃另一只酒精灯。(4)氮化锶遇水发生反应的化学方程式为 Sr3N2+6H2O=3Sr(OH)3+2NH3↑。
方案Ⅱ:某氮气样品可能含有少量的CO、CO2、O2等气体杂质,某同学设计如下装置制备氮化锶(各装置盛装足量试剂)。I用碱吸收二氧化碳,试管Ⅱ用连苯三酚鹹性溶液能定量吸收O2,Ⅲ中醋酸二氨合亚铜CH3COO[Cu(NH3)2]溶液能定量吸收CO;(5)试管Ⅱ盛装的试剂是a,吸收氧气。装置Ⅵ的作用是吸收空气中CO和H2O(g);(6)测定产品纯度:取wg产品,向其中加入适量的水。将产生的气体全部通人到依硫酸中,依硫酸增重mg,
2NH3~~~Sr3N2
34 292
mg x
x=146m/17g,则产品纯度为146m/(17w)×100%。有同学认为上述方法使测得产品纯度偏高,其原因是 氨气中混有水蒸气。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】一定条件下,CH4与H2O(g)发生反应:CH4(g)+H2O(g)![]() CO(g)+3H2(g),设起始
CO(g)+3H2(g),设起始![]() =Z,在恒压下,平衡时
=Z,在恒压下,平衡时![]() (CH4)的体积分数与Z和T(温度)的关系如图所示。下列说法正确的是
(CH4)的体积分数与Z和T(温度)的关系如图所示。下列说法正确的是
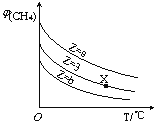
A.该反应的焓变△H>0
B.图中Z的大小为a>3>b
C.图中X点对应的平衡混合物中![]() =3
=3
D.温度不变时,图中X点对应的平衡在加压后![]() (CH4)减小
(CH4)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,有关物质的电离平衡常数如下:
化学式 | CH3COOH | H2CO3 | H2SO3 |
电离平衡常数 | K=1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=1.5×10-2 K2=1.02×10-7 |
(1)请写出H2SO3的电离平衡常数K1的表达式:________________。
(2) 常温下,将体积为10mL pH=2的醋酸溶液与亚硫酸溶液分别加蒸馏水稀释至1000mL,稀释后溶液的pH,前者_____后者(填“>”、“<”或“=”)。
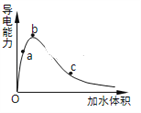
(3)一定条件下,冰醋酸加水稀释过程中溶液导电能力I随加水体积V变化曲线如右图所示,则a、b、c三点溶液醋酸的电离程度由大到小为____________________。
(4)下列离子CH3COO-、CO32-、HSO3-、SO32-在溶液中结合H+的能力由大到小的关系为___________。
(5)体积相同、c(H+)相同的①CH3COOH;②HCl;③H2SO4 三种酸溶液分别与同浓度的NaOH溶液完全中和时,消耗NaOH溶液的体积由大到小的排列顺序是_____(填序号)。
(6)已知,H+(aq) + OH-(aq) == H2O(l) ΔH =-57.3 kJ/mol。实验测得稀醋酸与稀NaOH溶液反应生成1 mol H2O时放出57 kJ的热,则醋酸溶液中,醋酸电离的热化学方程式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一瓶无色澄清的溶液,溶质由NH4NO3、KCl、CuCl2、K2CO3、Na2CO3中的一种或几种配制而成。为了确定其中的溶质,用该溶液做如下实验:
(1)取少许溶液,加入足量的盐酸有气泡产生
(2)再向(1)的溶液中滴加硝酸银溶液有白色沉淀生成
(3)取原溶液少量,加入NaOH溶液并加热,产生刺激性气味的气体,并用湿润的红色石蕊试纸检验气体,试纸变蓝
(4)用铂丝蘸取原溶液于煤气灯上灼烧,火焰呈黄色
根据以上事实判断:肯定存在的溶质是___________________________;肯定不存在的溶质是_______; 不能确定是否存在的溶质是________________。写出上述实验(3)中产生刺激性气味气体的反应的化学方程式:_____________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,CH4与H2O(g)发生反应:CH4(g)+H2O(g)![]() CO(g)+3H2(g),设起始
CO(g)+3H2(g),设起始![]() =Z,在恒压下,平衡时
=Z,在恒压下,平衡时![]() (CH4)的体积分数与Z和T(温度)的关系如图所示。下列说法正确的是
(CH4)的体积分数与Z和T(温度)的关系如图所示。下列说法正确的是

A.该反应的焓变△H>0
B.图中Z的大小为a>3>b
C.图中X点对应的平衡混合物中![]() =3
=3
D.温度不变时,图中X点对应的平衡在加压后![]() (CH4)减小
(CH4)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,将4molA和3molB充入体积为1L的密闭容器中,发生如下反应:aA(g)+2B(g)![]() 3C(g)+D(g)。反应达到平衡后,C的浓度为3mol/L.压缩容器体积,使容器的体积减小一半,建立新的平衡时,B的浓度为2mol/L.则方程式中a的数值为
3C(g)+D(g)。反应达到平衡后,C的浓度为3mol/L.压缩容器体积,使容器的体积减小一半,建立新的平衡时,B的浓度为2mol/L.则方程式中a的数值为
A. 1 B. 2 C. 3 D. 4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠-氯化镍电池以 β-Al2O3(Al2O3x Na2O)作为固体电解质构成的一种新型电池(2Na+NiCl2![]() Ni+2NaCl ), 其结构如图所示。下列关于该电池的叙述错误的是
Ni+2NaCl ), 其结构如图所示。下列关于该电池的叙述错误的是
A. 放电时 NaCl在熔融电解质中生成
B. 充电时阴极反应: Na+ + e- ═ Na
C. 氯离子通过β-Al2O3(s)在两电极间移动
D. 如果电池过度放电, AlCl4-可能被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以熔融Li2CO3和K2CO3为电解质,天然气经重整催化作用提供反应气的燃料电池如右图。下列说法正确的是
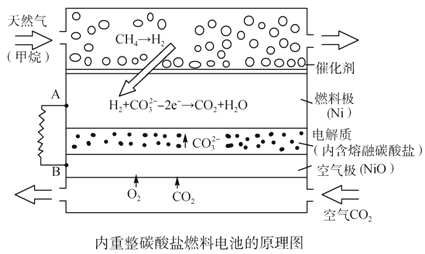
A. 以此电池为电源电解精炼铜,当有0.1 mol e- 转移时,有3.2 g铜溶解
B. 若以甲烷为燃料气时负极电极反应式:CH4+5O2--8e-=CO32-+2H2O
C. 该电池使用过程中需补充Li2CO3和K2CO3
D. 空气极发生的电极反应式为O2+4e-+2CO2===2CO32-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com