
����Ŀ��ԭ����ǻ�ѧ�������һ���ش��ס�
(1)ij��ȤС��Ϊ�о����ԭ���������ͼAװ�á�
|
|
A | B |
��a��b������ʱ���ձ��з�����Ӧ�����ӷ���ʽ��___________________��
��a��b�õ������ӣ�Cu��Ϊԭ���________(����������������)�����õ缫��Ӧʽ��____________________________��
������a��b�Ƿ����ӣ�ZnƬ������ʴ����ת����0.4 mol���ӣ���������ZnƬ��������________ g��
(2)��ͼB�Ǽ���ȼ�ϵ��ԭ��ʾ��ͼ���ش��������⣺
�ٵ�صĸ�����________(����a������b��)�缫���ü��ĵ缫��ӦʽΪ________________��
�ڵ�ع���һ��ʱ���������Һ��pH________(��������������С������������)��
���𰸡�Zn+2H+=H2��+Zn 2+ ���� 2H++2e-=H2�� 13.0 a CH4+10OH--8e-===CO32-+7H2O ��С
��������
(1)��a��b������ʱ����װ�ò�����ԭ��أ�п�������ӷ����û���Ӧ��
��a��b�õ������ӣ���װ�ù���ԭ��أ�пʧ���ӷ���������Ӧ����������ͭ�������������������ӵõ��ӷ�����ԭ��Ӧ��
�۸���п��ת�Ƶ���֮��Ĺ�ϵʽ���㣻
(2)�ټ��Լ���ȼ�ϵ����ͨ������һ��Ϊԭ��صĸ�����ͨ��������һ��Ϊԭ��ص���������������ȼ�Ϸ���ʧ���ӵ�������Ӧ��
�ڸ���ȼ�ϵ�ص��ܷ�Ӧ����ʽ�ж�pH�ı仯��
(1)��a��b������ʱ����װ�ò�����ԭ��أ�п�������ӷ����û���Ӧ�����ӷ�Ӧ����ʽΪ��Zn+2H+=Zn2++H2����
��a��b�õ������ӣ���װ�ù���ԭ��أ�ͭ�������������������ӵõ��ӷ�����ԭ��Ӧ���缫��ӦʽΪ2H++2e-=H2����
����ת����0.4mol���ӣ�Zn-2e-=Zn2+��пƬ���ٵ�����=![]() ��65g/mol=13.0g��
��65g/mol=13.0g��
(2)�ټ��Լ���ȼ�ϵ����ͨ������һ��Ϊԭ��صĸ������ü�����ȼ�Ϸ���ʧ���ӵ�������Ӧ����CH4+10OH--8e-�TCO32-+7H2O��
���ڼ�����Һ�У�����ȼ�ϵ�ص��ܷ�ӦʽΪCH4+2O2+2OH-=CO32-+3H2O����ع���һ��ʱ����������������ӱ����ģ����Ե������Һ��pH���С��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ˮ����(N2H4��H2O)����ɫ����ǿ��ԭ�Ե�Һ�壬ʵ�����Ʊ�ˮ���µ�ԭ��Ϊ��CO(NH2)2+2NaOH+NaClO=Na2CO3+N2H4��H2O+NaCl�ݴˣ�ijѧ�����������ʵ�顣
���Ʊ�NaClO��Һ��ʵ��װ������ͼͼ����ʾ�����ּг�װ����ʡ�ԣ�
��֪��3NaClO![]() 2NaCl+NaClO3
2NaCl+NaClO3
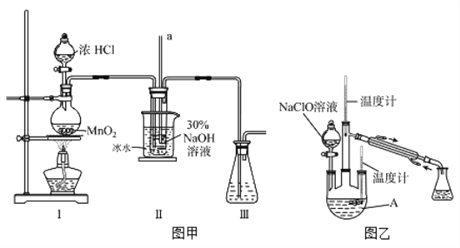
��1������30 %NaOH��Һʱ�����貣����������Ͳ���__________������ĸ����
A.����ƿ B���ձ� C����Һ�� D.������
��2��װ��I�з��������ӷ�Ӧ����ʽ��_______________�����в�����a������Ϊ____________�������ñ�ˮԡ�����¶���30�����£�����ҪĿ��___________________
����ȡˮ���¡�ʵ��װ������ͼͼ����ʾ
��3����Ӧ�����У������Һ©������Һ�ĵ��ٹ��죬 ����N2H4��H2O����A�з�Ӧ������������������Ʒ������˽��ͣ���д�����Ͳ��ʵ���ػ�ѧ��Ӧ����ʽ____________________����ַ�Ӧ��������A�ڵ���Һ���ɵõ�ˮ���µĴֲ�Ʒ��
���ⶨ�µĺ�����
��4����ȡ���0.3000 g����ˮ���20.0 mL��Һ��һ����������0.1500 mol��L-1��I2��Һ�ζ�����֪: N2H4��H2O + 2I2 = N2��+ 4HI + H2O��
�ٵζ�ʱ������ѡ�õ�ָʾ��Ϊ____________��
��ʵ��������I2��Һ��ƽ��ֵΪ20. 00 mL�������N2H4��H2O����������Ϊ____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧʵ��������ͼ��ʾװ����ȡ�����屽������д���пհס�
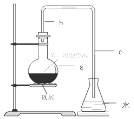
��1������ƿa��װ���Լ��DZ��������м������b��������������һ�ǵ��������Ǽ���__________�����á�
��2����Ӧ�������ڵ���c���¿ڸ������Թ۲쵽�������֣��������ڷ�Ӧ���ɵ�________��ˮ�������γɵġ�
��3����Ӧ��Ϻ�����ƿd�е���AgNO3��Һ����__________���ɡ�
��4����Ӧ��Ϻ���ƿa�е�Һ�嵹��ʢ����ˮ���ձ�����Թ۲쵽�ձ��ײ���__________ɫ������ˮ��Һ�塣�����ܽ���__________�Ĵ��屽��
��5��д����ƿa�з�����Ӧ�Ļ�ѧ����ʽ��____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ɫ�����ĩ������Fe2O3��Cu2O�������Ϊ̽������ɣ���ȡmg�ù����ĩ��Ʒ����������ϡH2SO4��ַ�Ӧ�Ƶù�������Ϊag��
��֪��Cu2O+2H+ = Cu+Cu2++H2O
(1)��a=____________(�ú�m�����ʽ��ʾ)�����ɫ�����ĩΪ�����
(2)��a=m/9�����ɫ�����ĩ��Fe2O3�����ʵ���Ϊ____________mol(�ú�m�����ʽ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����.���Ʊ������ǻ�ѧʵ���һ�ֳ��÷������±���ijѧϰС���о������ʵ���Ũ�ȵ�ϡ�����п��Ӧ��ʵ�����ݣ������������ݣ��ش��������⣺
��� | ��������/mL | п������/g | п����״ | �¶�/�� | ��ȫ�������ʱ��/s | ��������п������/g |
1 | 50.0 | 2.0 | ��Ƭ | 25 | 100 | m1 |
2 | 50.0 | 2.0 | ���� | 25 | 70 | m2 |
3 | 50.0 | 2.0 | ���� | 35 | 35 | m3 |
4 | 50.0 | 2.0 | ��ĩ | 25 | 45 | 5.0 |
5 | 50.0 | 6.0 | ��ĩ | 35 | 30 | m5 |
6 | 50.0 | 8.0 | ��ĩ | 25 | t6 | 16.1 |
7 | 50.0 | 10.0 | ��ĩ | 25 | t7 | 16.1 |
(1)��ѧ��Ӧ���ʱ������������ʵ����ʾ����ģ����������Ҳ��Ӱ�췴Ӧ���ʵĴ�С����ʵ����ʵ��2��ʵ��3�Աȵó��Ľ�����______________________________��
(2)�������ѡȡʵ��________(��3��ʵ�����)�о�п����״�Է�Ӧ���ʵ�Ӱ�졣
(3)��������ʵ��1��ȫ��ͬ������������Ӧ�����еμ���������ͭ��Һ�����ַ�Ӧ�������Լӿ졣ԭ����______________________________��
(4)���ñ������ݣ�������ã���������ʵ���Ũ����________mol/L��
��.ij�¶�ʱ����5 L�������У�X��Y��Z������������ʵ�����ʱ��ı仯������ͼ��ʾ����ͨ������ش��������⣺
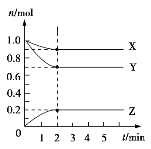
(5)��Ӧ��ʼ��2 min��Y��ƽ����Ӧ����______________________��
(6)�����й����ݣ�д��X��Y��Z�ķ�Ӧ����ʽ_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������(Ni��Cd)�ɳ�������ִ��������й㷺Ӧ�á���֪ij���ӵ�صĵ������ҺΪKOH��Һ����䡢�ŵ簴��ʽ���У�Cd��2NiOOH��2H2O![]() Cd(OH)2��2Ni(OH)2���йظõ�ص�˵����ȷ����( )
Cd(OH)2��2Ni(OH)2���йظõ�ص�˵����ȷ����( )
A. �ŵ�ʱ����ʧȥ���ӣ�������ԭ��Ӧ
B. �ŵ�ʱ�������Һ�е�OH���������ƶ�
C. ���ʱ����������Һ��pH��С
D. ���ʱ������Ӧ��Ni(OH)2��e����OH��===NiOOH��H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��Һ�У�������IO3��>I2>SO32-����3 mol NaHSO3����Һ����μ���KIO3��Һ�������KIO3��������I2�����ʵ����Ĺ�ϵ��������ͼ��ʾ������˵����ȷ����
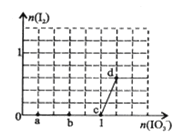
A. a�㷴Ӧ�Ļ�ԭ����NaHSO3����������Ԫ���ǵ�Ԫ��
B. b�㷴Ӧ�����ӷ���ʽ�ǣ�3HSO3-+IO3-+3OH-=3SO42-+I-+3H2O
C. c�㵽d��ķ�Ӧ�й�ת��0.6mol����
D. ��200mL 1 mol/L��KIO3��Һ�еμ�NaHSO3��Һ����Ӧ��ʼʱ�����ӷ���ʽ�ǣ�5 HSO3- + 2IO3- == I2+ 5SO42-+ 3H++ H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��NH3��һϵ�з�Ӧ���Եõ�HNO3��NH4NO3����ͼ��ʾ��

�����У�NH3��O2�ڴ��������·�Ӧ���仯ѧ����ʽ�ǣ�__________________________��

��2�����У�2NO��g��+ O2��g�� 2NO2��g����������������ͬʱ���ֱ���NO��ƽ��ת�����ڲ�ͬѹǿ��p1��p2�����¶ȱ仯�����ߣ���ͼ����
��p1��p2�Ĵ�С��ϵp1 ________ p2������ڡ����ڡ�С�ڣ�����
�����¶����ߣ��÷�Ӧƽ�ⳣ���仯��������_________________________
��3�����У������¶ȣ���NO2��g��ת��ΪN2O4��1�����Ʊ�Ũ���ᣮ
N2O4��O2�� H2O���ϵĻ�ѧ����ʽ��______________________________
��4�����У����NO�Ʊ�NH4NO3����ԭ��ԭ������ͼ��ʾ��Ϊʹ������ȫ��ת��ΪNH4NO3�� �貹������___________ ��˵�����ɣ�___________________��
 .
.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����Ϊ��Ԫ���H2C2O4![]() HC2O��H����Ka1��HC2O
HC2O��H����Ka1��HC2O![]() C2O
C2O![]() ��H����Ka2�������£���ijŨ�ȵ�H2C2O4��Һ����μ���һ��Ũ�ȵ�KOH��Һ��������Һ��H2C2O4��HC2O��C2O
��H����Ka2�������£���ijŨ�ȵ�H2C2O4��Һ����μ���һ��Ũ�ȵ�KOH��Һ��������Һ��H2C2O4��HC2O��C2O![]() �����������ʵ�������(��)����ҺpH�Ĺ�ϵ��ͼ��ʾ��������˵���в���ȷ����(����)
�����������ʵ�������(��)����ҺpH�Ĺ�ϵ��ͼ��ʾ��������˵���в���ȷ����(����)

A. Ka1=10��1.2
B. pH��2.7ʱ��Һ�У�![]() ��1000
��1000
C. ����ͬ���ʵ�����KHC2O4��K2C2O4������ȫ����ˮ�������pHΪ4.2�Ļ��Һ
D. ��pH��1.2����Һ�м�KOH��Һ����pH������4.2�Ĺ�����ˮ�ĵ���̶�һֱ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com