
 碳酸钙可以降低胃酸的浓度而被用作胃药的抗酸剂.某中学研究性学习小组为测定一胃药中碳酸钙的含量,设计了如下的实验操作:
碳酸钙可以降低胃酸的浓度而被用作胃药的抗酸剂.某中学研究性学习小组为测定一胃药中碳酸钙的含量,设计了如下的实验操作:分析 (1)用中和滴定法胃药中碳酸钙的含量,先把药片磨碎溶于水,配制0.1 mol•L-1的HCl溶液和0.1 mol•L-1的NaOH溶液,加过量的盐酸溶解碳酸钙,再用氢氧化钠滴定剩余的盐酸;
(2)配制溶液的主要操作为:称量或量取、在烧杯中溶解、转移到容量瓶、定容;
(3)根据配制的溶液体积选择容量瓶;
(4)步骤④中为盐酸与碳酸钙反应;
(5)以酚酞作指示剂,用氢氧化钠滴定盐酸,溶液由无色变为浅红色;
(6)根据氢氧化钠的量求出盐酸的量,用总的盐酸的物质的量减去与氢氧化钠反应的盐酸的量即是与碳酸钙反应的盐酸的量,根据方程式计算出碳酸钙的物质的量,再求质量.
解答 解:(1)用中和滴定法胃药中碳酸钙的含量,先把药片磨碎溶于水,配制0.1 mol•L-1的HCl溶液和0.1 mol•L-1的NaOH溶液,加过量的盐酸溶解碳酸钙,再用氢氧化钠滴定剩余的盐酸,则实验操作顺序为②①④③,
故答案为:②①④③;
(2)配制溶液的主要操作为:称量或量取用到天平或量筒、在烧杯中溶解用到烧饼和玻璃棒、转移到容量瓶用到容量瓶和玻璃棒、定容用到胶头滴管,所以没有用到的仪器是烧瓶和分液漏斗,即AC;除了图中所给的仪器还需要烧杯和玻璃棒;
故答案为:AC;烧杯、玻璃棒;
(3)要配制100ml盐酸和氢氧化钠溶液,所以选用100ml的容量瓶;
故答案为:100;
(4)步骤④中为盐酸与碳酸钙反应生成氯化钙、二氧化碳和水,其反应的离子方程式为CaCO3+2H+═Ca2++CO2↑+H2O;
故答案为:CaCO3+2H+═Ca2++CO2↑+H2O;
(5)以酚酞作指示剂,用氢氧化钠滴定盐酸,溶液由无色变为浅红色,则滴入最后一滴NaOH溶液时,使溶液由无色变为浅红色,且半分钟内不褪色即是滴定终点;
故答案为:滴入最后一滴NaOH溶液时,使溶液由无色变为浅红色,且半分钟内不褪色;
(6)与氢氧化钠反应的盐酸为n(HCl)=n(NaOH)=0.1 mol•L-1×10-3VL=10-4Vmol;
与碳酸钙反应的盐酸为n′(HCl)=0.1 mol•L-1×0.025L-10-4Vmol=(0.0025-10-4V)mol,
已知碳酸钙与盐酸的反应为:CaCO3+2H+═Ca2++CO2↑+H2O,则n(CaCO3)=$\frac{1}{2}$×(0.0025-10-4V)mol,
则每粒该胃药中含碳酸钙的质量是$\frac{1}{2}$×(0.0025-10-4V)mol×100g/mol=(0.125-0.005V)g;
故答案为:(0.125-0.005V)g.
点评 本题考查溶液的配制、中和滴定、物质含量的测定,题目难度中等,侧重于学生的分析能力和实验能力的考查,注意把握实验原理、步骤和操作注意事项等.


 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:选择题
| 一定状态的分子 | H2(g) | Br2(l) | HBr(g) |
| 1mol该分子中的化学键断裂吸收的能量/kJ | 436 | a | 369 |
| A. | 404 | B. | 344 | C. | 260 | D. | 200 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 FeCl3具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3 高效,且腐蚀性小.请回答下列问题:
FeCl3具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3 高效,且腐蚀性小.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 光导纤维 | B. | 硅橡胶 | C. | 合成纤维 | D. | 黏合剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
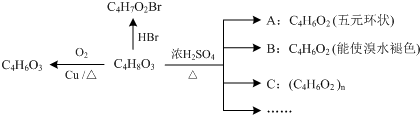
 .
. +H2O.
+H2O. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | 2Na+2H2O=2NaOH+H2↑ 2Al+2H2O+2NaOH=2NaAlO2+3H2↑ | 均为水做氧化剂的氧化还原反应 |
| B | Fe+CuSO4=FeSO4+Cu 点燃 2Mg+CO22MgO+C | 均为固体质量增大的置换反应 |
| C | NaAlO2+SO2+2H2O=Al(OH)3+NaHSO3 NaClO+CO2+H2O=HClO+NaHCO3 | 均为较强酸制较弱酸的复分解反应 |
| D | H2O2+SO2=H2SO4 CaO+SO3=CaSO4 | 均为非氧化还原反应的化合反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “碳铵”的化学式:(NH4)2CO3 | |
| B. | 二氧化碳的结构式:O=C=O | |
| C. | 钾原子的结构示意图: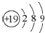 | |
| D. | 中子数为138、质子数为88的镭(Ra)原子:${\;}_{88}^{138}$Ra |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
. .
. $→_{②Zn/H_{2}O}^{①O_{3}}$
$→_{②Zn/H_{2}O}^{①O_{3}}$ +R3CHO,
+R3CHO, 为原料制备
为原料制备 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH$→_{浓H_{2}SO_{4}△}^{CH_{3}COOH}$CH3COOCH2CH3.
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH$→_{浓H_{2}SO_{4}△}^{CH_{3}COOH}$CH3COOCH2CH3.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com