
·ÖĪö ŅĄ¾Żn=$\frac{N}{{N}_{A}}$=$\frac{m}{M}$£¬½įŗĻ¶žŃõ»ÆĮņÖŠŗ¬ÓŠ2øöŃõŌ×Ó£¬ČżŃõ»ÆĮņÖŠŗ¬ÓŠ3øöŃõŌ×Ó½ā“š£®
½ā“š ½ā£ŗŅĄ¾Żn=$\frac{N}{{N}_{A}}$æÉÖŖ£¬ŗ¬ÓŠĻąĶ¬·Ö×ÓøöŹżµÄSO2ŗĶSO3£¬ĪļÖŹµÄĮæÖ®±ČĪŖ£ŗ1£ŗ1£»
ŅĄ¾Żn=$\frac{m}{M}$æÉÖŖ£¬ĻąĶ¬ĪļÖŹµÄĮæµÄĪļÖŹÖŹĮæÖ®±ČµČӌĦ¶ūÖŹĮæÖ®±Č£¬ĖłŅŌĪļÖŹµÄĮæÖ®±ČĪŖ£ŗ1£ŗ1µÄSO2ŗĶSO3£¬ÖŹĮæÖ®±ČĪŖ£ŗ64£ŗ80=4£ŗ5£»
¶žŃõ»ÆĮņÖŠŗ¬ÓŠ2øöŃõŌ×Ó£¬ČżŃõ»ÆĮņÖŠŗ¬ÓŠ3øöŃõŌ×Ó£¬ŌņĻąĶ¬ĪļÖŹµÄĮæµÄSO2ŗĶSO3£¬ĘäÖŠĖłŗ¬ŃõŌ×ÓøöŹż±ČĪŖ2£ŗ3£»
¹Ź“š°øĪŖ£ŗ4£ŗ5£» 1£ŗ1£»2£ŗ3£®
µćĘĄ ±¾Ģāæ¼²éĮĖŅŌĪļÖŹµÄĮæĪŖŗĖŠÄµÄÓŠ¹Ų¼ĘĖć£¬Ć÷Č·ŅŌĪļÖŹµÄĮæĪŖŗĖŠÄµÄĻą¹Ų¼ĘĖć¹«Ź½£¬ŹģĻ¤¶žŃõ»ÆĮņ”¢ČżŃõ»ÆĮņ·Ö×Ó¹¹³ÉŹĒ½āĢā¹Ų¼ü£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
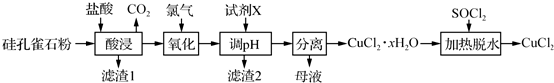
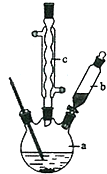 ±½ŅŅĖįĶŹĒŗĻ³ÉÓÅĮ¼“߻ƼĮ”¢“«øŠ²ÄĮĻ--ÄÉĆ×Ńõ»ÆĶµÄÖŲŅŖĒ°ĒżĢåÖ®Ņ»£®ĻĀĆęŹĒĖüµÄŅ»ÖÖŹµŃéŹŅŗĻ³ÉĀ·Ļߣŗ
±½ŅŅĖįĶŹĒŗĻ³ÉÓÅĮ¼“߻ƼĮ”¢“«øŠ²ÄĮĻ--ÄÉĆ×Ńõ»ÆĶµÄÖŲŅŖĒ°ĒżĢåÖ®Ņ»£®ĻĀĆęŹĒĖüµÄŅ»ÖÖŹµŃéŹŅŗĻ³ÉĀ·Ļߣŗ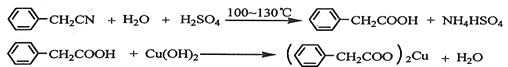
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ę½ŗāŗóCOµÄĢå»ż·ÖŹżĪŖ40% | |
| B£® | Ę½ŗāŗóCOµÄ×Ŗ»ÆĀŹĪŖ25% | |
| C£® | Ę½ŗāŗóĖ®µÄ×Ŗ»ÆĀŹĪŖ50% | |
| D£® | Ę½ŗāŗó»ģŗĻĘųĢåµÄĘ½¾łĻą¶Ō·Ö×ÓÖŹĮæĪŖ24 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NH4+”¢C1-”¢Mg2+”¢SO42- | B£® | A13+”¢Cu2+”¢SO42-”¢C1- | ||
| C£® | Ba2+”¢K+”¢NO3-”¢OH- | D£® | Ca2+”¢Na+”¢C1-”¢A1O2- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ū¢Ż | B£® | ¢Ł¢Ü¢Ż | C£® | ¢Ś¢Ū¢Ü | D£® | ¢Ś¢Ü¢Ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | ĖüµÄŅ»ĀČ“śĪļÖ»ÓŠŅ»ÖÖĶ¬·ÖŅģ¹¹Ģå | |
| B£® | ĖüµÄ¶žĀČ“śĪļÓŠĮ½ÖÖĶ¬·ÖŅģ¹¹Ģå | |
| C£® | ĖüµÄ·Ö×ÓŹ½ĪŖC8H8 | |
| D£® | ĖüÓė±½ŅŅĻ©£ØC6H5-CH=CH2£©»„ĪŖĶ¬·ÖŅģ¹¹Ģå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĻąĶ¬Ģõ¼žĻĀ£¬Ę½ŗāŹ±Čō³äČėĻ”ÓŠĘųĢ壬SO2µÄ×Ŗ»ÆĀŹŌö“ó | |
| B£® | 0”«6 minµÄĘ½ŗā·“Ó¦ĖŁĀŹ£ŗv£ØO2£©=0.105 mol/£ØL•min£© | |
| C£® | ±£³ÖĘäĖūĢõ¼ž²»±ä£¬½ö½µµĶĪĀ¶Č£¬Õż·“Ó¦ĖŁĀŹ¼õŠ”³Ģ¶Č±ČÄę·“Ó¦ĖŁĀŹ¼õŠ”³Ģ¶Č“ó | |
| D£® | ·“Ó¦æŖŹ¼Ź±£¬ĻņČŻĘ÷ÖŠĶØČėµÄSO2µÄĪļÖŹµÄĮæŹĒ1.4 mol |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com