
| A. | 苯乙烯 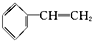 | B. | 苯甲醛 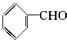 | C. | 苯乙酮 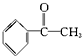 | D. | 苯酚 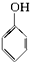 |
分析 在常见的有机化合物中甲烷是正四面体结构,乙烯和苯是平面型结构,乙炔是直线型结构,其它有机物可在此基础上进行判断,注意结合信息中甲醛的平面结构.
解答 解:A.苯为平面结构,乙烯为平面结构,通过旋转乙烯基连接苯环的单键,可以使两个平面共面,故 中所有的原子可能处于同一平面,故A错误;
中所有的原子可能处于同一平面,故A错误;
B.苯环为平面结构,醛基为平面结构,通过旋转醛基连接苯环的单键,可以使两个平面共面,故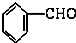 中所有的原子可能处于同一平面,故B错误;
中所有的原子可能处于同一平面,故B错误;
C.分子中存在甲基,具有甲烷的四面体结构,故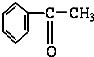 所有原子不可能处于同一平面,故C正确;
所有原子不可能处于同一平面,故C正确;
D.苯环为平面结构,氧原子取代氢原子的位置,氢原子通过旋转,所有的原子可能处于同一平面,故D错误.
故选C.
点评 本题主要考查有机化合物的结构特点,做题时注意从甲烷、乙烯、苯和乙炔的结构特点判断有机分子的空间结构,其中单键可以旋转.


 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石墨比金刚石稳定 | B. | 金刚石比石墨稳定 | ||
| C. | 石墨转化为金刚石是一个物理变化 | D. | 石墨和金刚石是同一种物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO的燃烧热为566kJ•mol-1 | |
| B. | 2 mol CO和1 mol O2的总能量比2 mol CO2的总能量低 | |
| C. | 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=-1453.28 kJ•mol-1 | |
| D. | 完全燃烧16g甲醇,生成一氧化碳和水时放出的热量为221.82 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
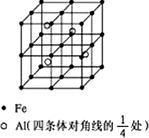 第四周期过渡元素Fe、Ti可与C、H、N、O形成多种化合物.
第四周期过渡元素Fe、Ti可与C、H、N、O形成多种化合物.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 每一个水分子内含有两个氢键 | |
| B. | 氢键只能存在于分子之间 | |
| C. | DNA中的碱基互补配对是通过氢键来实现的 | |
| D. | HF是一种非常稳定的化合物,这是由氢键所致 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
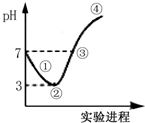 常温下,将Cl2缓缓通入水中至饱和,然后向所得饱和溶液中滴加0.1mol•L-1 NaOH溶液,整个过程中pH的变化如图所示.下列有关叙述正确的是( )
常温下,将Cl2缓缓通入水中至饱和,然后向所得饱和溶液中滴加0.1mol•L-1 NaOH溶液,整个过程中pH的变化如图所示.下列有关叙述正确的是( )| A. | 从反应开始至②点,发生反应的离子方程式为:Cl2+H2O═ClO-+2H++Cl- | |
| B. | ③处表示氯气和NaOH溶液恰好完全反应 | |
| C. | ②点所表示的溶液中所存在的具有氧化性的含氯元素的微粒主要有:Cl2、HClO、ClO- | |
| D. | 从反应开始至②点可用pH试纸测定溶液的pH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com