
在Cu+2H2SO4(浓)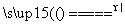 CuSO4+SO2↑+2H2O反应中:
CuSO4+SO2↑+2H2O反应中:
(1)________元素被氧化,________是氧化剂。
(2)用双线桥法标出该反应中电子转移的方向和数目。
Cu+2H2SO4(浓)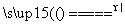 CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
(3)某一反应中有反应物和生成物的粒子共6种:SO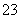 、I2、H+、SO
、I2、H+、SO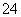 、I-、H2O,已知该反应中I2只发生如下过程:I2→I-,请回答:
、I-、H2O,已知该反应中I2只发生如下过程:I2→I-,请回答:
①该反应的还原剂是________(填分子或离子符号)。
②反应过程中,每有1molI2发生反应,转移的电子为____mol。
③写出该反应的离子方程式____________________________。
科目:高中化学 来源: 题型:
溴及其化合物广泛应用于医药、农药、纤维、塑料组燃剂等,回答下列问题:
(1)海水提溴过程中,向浓缩的海水中通入 ,将其中的Br-氧化,再用空气吹出溴;然后用碳酸钠溶液吸收溴,溴歧化为Br-和BrO3-,其离子方程式为 。
(2)溴与氯能以共价键结合形成BrCl。BrCl分子中, 显正电性。BrCl与水发生反应的化学方程式为 。
(3)CuBr2分解的热化学方程式为:
2CuBr2(s)=2 CuBr(s)+ Br2(g) △H=+105.4kJ/mol
在密闭容器中将过量CuBr2于487K下加热分解,平衡时p(Br2)为4.66×103Pa。
①如反应体系的体积不变,提高反应温度,则p(Br2)将会 (填“增大”、“不变”或“减小”)。
②如反应温度不变,将反应体系的体积增加一倍,则p(Br2)的变化范围为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
乙醇在实际生产生活中有广泛用途。
(1)下列选项中属于乙醇作为燃料的优点的是________。
①燃烧时发生氧化反应
②充分燃烧的产物不污染环境
③乙醇是一种可再生能源
④燃烧时放出大量热量
A.①②③ B.①②④
C.①③④ D.②③④
(2)在焊接铜漆包线的线头时,通常先把线头放在火上烧一下除去漆层,并立即在酒精中蘸一下再进行焊接操作,这是因为(用反应方程式表示):
①________________________________________________________________________;
②________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子在溶液中能够大量共存的是( )
A.K+、Cl-、NO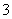 、Ag+
、Ag+
B.H+、HCO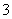 、Na+、Cl-
、Na+、Cl-
C.Na+、OH-、Ba2+、CO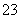
D.Mg2+、Cl-、H+、SO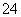
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应的离子方程式正确的是( )
A.向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:
Fe3++3H2O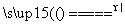 Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
B.用小苏打治疗胃酸过多:
HCO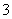 +H+===H2O+CO2↑
+H+===H2O+CO2↑
C.实验室用浓盐酸与MnO2反应制Cl2:
MnO2+2H++2Cl-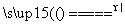 Cl2↑+Mn2++H2O
Cl2↑+Mn2++H2O
D.用FeCl3溶液腐蚀印刷电路板:
Fe3++Cu===Fe2++Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中不属于水解反应的是( )
A.纤维素在稀硫酸作用下转化为葡萄糖
B.葡萄糖在酒化酶作用下转化为乙醇和二氧化碳
C.乙酸乙酯在氢氧化钠溶液中加热反应
D.淀粉在一定条件下转化为葡萄糖
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ、已知将浓盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去。现有一个氧化还原反
应的体系中共有KCl.Cl2.H2SO4.H2O.KMnO4.MnSO4.K2SO4七种物质:
(1)该反应中,化合价升高的反应物是 。
(2)写出一个包含上述七种物质的氧化还原反应方程式:
(3)上述反应中,氧化剂是 ,1 mol氧化剂在反应中得到 mol电子。
Ⅱ、某研究性学习小组利用下列装置制备漂白粉,并进行漂白粉有效成分的质量分数测定
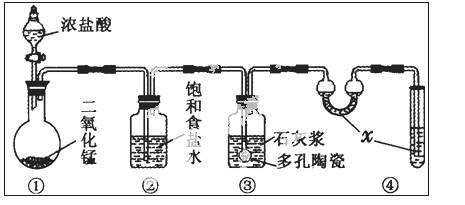
(1)装置④中的x试剂为 。
(2)装置③中发生反应的化学方程式为 。该反应是放热反应,反应温度较高时有副反应发生。改进该实验装置以减少副反应发生的方法是 _______________。
(3)测定漂白粉有效成分的质量分数
称取1.000 g漂白粉于锥形瓶中,加水溶解,调节溶液的pH,以淀粉为指示剂,用0.1000 mol·L-1 KI溶液进行滴定,溶液出现稳定浅蓝色时为滴定终点。反应原理为:
3ClO-+ I- = 3Cl-+ IO3- IO3- + 5I- + 3H2O = 6OH- + 3I2
实验测得数据如下表所示。
| 滴定次数 | 1 | 2 | 3 |
| KI溶液体积/mL | 19.98 | 20.02 | 20.00 |
该漂白粉中有效成分的质量分数为 。若滴定过程中未充分振荡溶液局部变浅蓝色时就停止滴定,则测定结果将 (填“偏高”、“偏低”或“无影响”)
查看答案和解析>>
科目:高中化学 来源: 题型:
硒(Se)被科学家称之为人体微量元素中的“防癌之王”,同时也是“心脏的守护神”“肝病的天敌”,对人体具有良好的保健作用。已知硒为第四周期、与氧同一族,根据它在周期表中的位置推测,硒不可能具有的性质为( )
A.硒也有两种氧化物,分别为SeO2和SeO3两种
B.硒化氢属于共价化合物,比硫化氢稳定
C.硒化氢的水溶液显弱酸性
D.硒单质的非金属性比氧弱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com