
| ||
| △ |
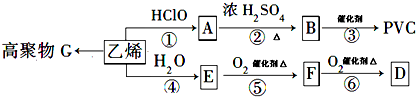
 ,乙烯与水发生加成反应生成E为CH3CH2OH,乙醇在催化剂条件下发生氧化反应生成F为CH3CHO,CH3CHO可进一步氧化得到D为CH3COOH,反应①为乙烯与次氯酸发生加成反应生成A为HOCH2CH2Cl,A发生消去反应生成B为CH2=CHCl,B再发生加聚反应得到PVC为
,乙烯与水发生加成反应生成E为CH3CH2OH,乙醇在催化剂条件下发生氧化反应生成F为CH3CHO,CH3CHO可进一步氧化得到D为CH3COOH,反应①为乙烯与次氯酸发生加成反应生成A为HOCH2CH2Cl,A发生消去反应生成B为CH2=CHCl,B再发生加聚反应得到PVC为 ,据此解答.
,据此解答. ,乙烯与水发生加成反应生成E为CH3CH2OH,乙醇在催化剂条件下发生氧化反应生成F为CH3CHO,CH3CHO可进一步氧化得到D为CH3COOH,反应①为乙烯与次氯酸发生加成反应生成A为HOCH2CH2Cl,A发生消去反应生成B为CH2=CHCl,B再发生加聚反应得到PVC为
,乙烯与水发生加成反应生成E为CH3CH2OH,乙醇在催化剂条件下发生氧化反应生成F为CH3CHO,CH3CHO可进一步氧化得到D为CH3COOH,反应①为乙烯与次氯酸发生加成反应生成A为HOCH2CH2Cl,A发生消去反应生成B为CH2=CHCl,B再发生加聚反应得到PVC为 ,
, ;
;| Cu |
| △ |
| Cu |
| △ |


科目:高中化学 来源: 题型:
| A、生成物具有的总能量减去反应物具有的总能量等于该反应的焓变 |
| B、因为该反应为吸热反应,故一定要加热反应才能进行 |
| C、破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量 |
| D、1 mol X和1 molY的总能量一定低于1 mol M和1 molN的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| NaOH溶液 |
| Cu/Ag |
| △ |
| ①HCN/OH- |
| ②H2O/H+△ |
乳酸 C3H6O3 |
| 浓H2SO4 |
| △ |
| 一定条件 |
F 加聚物 |
| ①HCN/OH- |
| ②H2O/H+△ |

查看答案和解析>>
科目:高中化学 来源: 题型:
 元素X位于第四周期,其基态原子的内层轨道全部排满电子,最外层电子数为2.元素Y基态原子的3p轨道有4个电子.元素Z的原子最外层电子数是内层的3倍.
元素X位于第四周期,其基态原子的内层轨道全部排满电子,最外层电子数为2.元素Y基态原子的3p轨道有4个电子.元素Z的原子最外层电子数是内层的3倍.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.08mol |
| B、0.10mol |
| C、0.12mol |
| D、0.18mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
 学校实验室现有含少量NaCl杂质的Na2CO3固体样品,某化学兴趣小组的同学决定测定样品Na2CO3的质量分数,甲、乙两位同学分别设计出下列两种实验方案:
学校实验室现有含少量NaCl杂质的Na2CO3固体样品,某化学兴趣小组的同学决定测定样品Na2CO3的质量分数,甲、乙两位同学分别设计出下列两种实验方案:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com