
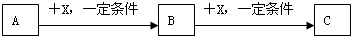
已知A是非金属单质,B是纯净物或其溶液,二者之间的反应可表示为:A+B![]() C+D(若生成物中除C、D外还有水的话,则水被略去)
C+D(若生成物中除C、D外还有水的话,则水被略去)
(1)若①在常温下能反应,C与D在酸性条件下又能转化为固体A,则A可能是_________,当C、D两物质的溶液均呈碱性时,写出①的离子方程式为__________________。
(2)若C、D既是两种重要气态燃料与原料,则用方程式表示出反应①________________
(3)若①中涉及的四种物质有三种的晶体均具有立体网状结构,则这三种晶体熔点由高到低的顺序为(写名称)___________________________
(4) 若①在常温下能剧烈反应,C、D中有一种物质的溶液能腐蚀玻璃,则反应①的方程式可表示为____________________________
(5)若A、C、D含有相同的元素,且这三种物质混合后能形成一种新物质E,E与B能发生化合反应生成F,则A的结构式为__________,0.01mol/L F的溶液中,各微粒浓度由大到小的顺序为________________________。
(1) Cl2或S ,3S+6OH-=2S2-+SO32—+3H2O (2)C+H2O(g)![]() H2+CO
H2+CO
(3) 金刚石>二氧化硅>硅 (4) 2F2+2H2O=4HF+O2
(5)O=O,c(NO3-)>c(NH4+)>c(H+)>c(OH-)
反应①可表示为A(单质)+B(化合物)→C+D(+H2O),中学化学中,满足此种形式的常见反应有很多,具体情况如下(部分)。
| A | Cl2、S | C | O2 | F2 | C、S | C、H2 | Cl2 |
| B | NaOH | SiO2、H2O | H2S、NH3 、CH4 | H2O | 浓硫酸、HNO3 | CuO | NaBr、H2S |
(1)C、D在酸性条件下能反应生成A,说明这是一个价态归中型氧化还原反应,A为氯气或单质硫;当C、D的溶液呈碱性,则它们分别是Na2S、Na2SO3。
(2)C、D为气态燃料时,一种是H2、一种是CO,此时A是单质碳,B是水
(3)符合此种条件的物质是金刚石、二氧化硅、晶体硅,由于键的长度是Si-Si>Si-O>C-C,故熔点高低顺序为金刚石>二氧化硅>硅。
(4)对照上表中各组物质,此时A为单质氟、B为水
(5)此时A为氧气,B为氨气,F是NH4NO3,NH4+水解,溶液呈酸性。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
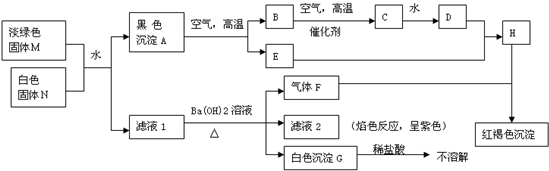
 (2011?山西模拟)A、B、C、D、E、F六种物质的相互转化关系如图所示(反应条件未标出),其中反应①是置换反应.
(2011?山西模拟)A、B、C、D、E、F六种物质的相互转化关系如图所示(反应条件未标出),其中反应①是置换反应.
| ||
| ||


| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:

| ||
| ||

查看答案和解析>>
科目:高中化学 来源:2012-2013学年浙江省杭州市西湖高级中学高一5月月考理科化学试卷(带解析) 题型:填空题
有A、B、C、D、E五种元素,它们均为短周期元素。已知A是非金属性最强的元素,且E与A同族;金属B的原子核内质子数比前一周期的同族元素多8,其单质不能从CuSO4溶液中置换出Cu;C元素有三种同位素,Cl、C2、C3,C1的质量数分别为C2、C3的1/2和1/3;D的气态氢化物溶于水后显碱性。
(1)写出B元素的离子结构示意图 ;C2粒子的符号: ;
(2)B、E两种元素形成化合物的电子式:
(3)A、E两种元素形成的氢化物沸点较高的是: (用化学式表示),
其原因是 。
(4)写出D的气态氢化物与其最高价氧化物的水化物反应的离子方程式
(5)写出D的氢化物(过量)与E的单质发生氧化还原反应生成一种单质和一种盐的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com