
【题目】在无色透明溶液中,能大量共存的离子组是
A. Mg2+、Na+、SO42-、Cl- B. Al3+、Ag+、NO3-、Cl-
C. Cu2+、Cl-、NO3-、OH- D. K+、H+、Cl-、CO32-
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】设汁下列实验方案鉴别Na2CO3和NaHC03两种白色粉末,不能达到预期目的是( ) 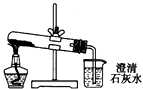
A.分别向等量的白色粉末中加等体积、等浓度的稀盐酸,比较生成气体的快慢
B.分别向等量的白色粉末中加等体积适量的水,比较固体溶解量的多少
C.分别将等量的白色粉末配成溶液,然后加入澄清石灰水,比较是否有沉淀生成
D.分别将等量的白色粉末用如图所示装置进行实验,比较澄清石灰水是否变浑浊
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯乙烯(C6H5CH=CH2)2是合成橡胶和塑料的单体,用来生产丁苯橡胶、聚苯乙烯等.工业上以乙苯C6H5CH2CH3为原料,采用催化脱氢的方法制取苯乙烯,反应方程式为:C6H5CH2CH3(g)C6H5CH=CH2(g)+H2(g)△H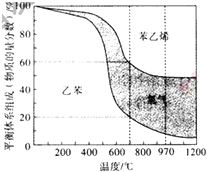
(1)已知:H2和CO的燃烧热(△H)分别为﹣285.8kJ.molL﹣1和﹣283.0kJ.molL﹣1;
C6H5CH2CH3(g)+CO2(g)C6H5CH=CH2(g)+CO(g)+H2O(I)△H=+114.8kJmol﹣1
则制取苯乙烯反应的△H为
(2)向密闭容器中加入1mol乙苯,在恒温恒容条件下合成苯乙烯,达平衡时,反应的能量变化为QkJ.下列说法正确的是 .
A.升高温度,正反应速率减小,逆反应速率增大
B.若继续加入1mol乙苯,苯乙烯转化率增大
C.压缩体积,平衡逆向移动,反应物浓度增大,生成物浓度减小
D.相同条件下若起始加入1mol苯乙烯和1mol氢气,达平衡时反应能量变化为(△H﹣Q)kJ
(3)向2L密闭容器中加入1mol乙苯发生反应,达到平衡状态时,平衡体系组成(物质的量分数)与温度的关系如图所示.700℃时,乙苯的平衡转化率为 , 此温度下该反应的平衡常数为;温度高于970℃时,苯乙烯的产率不再增加,其原因可能是 .
(4)含苯乙烯的废水排放会对环境造成严重污染,可采用电解法去除废水中的苯乙烯,基本原理是在阳极材料MOx上生成自由基MOx(OH),其进一步氧化有机物生成CO2 , 该阳极的电极反应式为 , 若去除0.5mol苯乙烯,两极共收集气体mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 碱性氧化物均为金属氧化物
B. 河海交汇处可沉积成沙洲是胶体的聚沉
C. Fe(OH)3胶体无色透明,能产生丁达尔效应
D. 我国试采可燃冰获得成功,可燃冰的主要成分是甲烷,甲烷属于有机物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】日常生活中的许多现象与化学反应有关,下列现象与氧化还原反应无关的是
A. 铜器出现铜绿[Cu2(OH)2CO3]
B. 铁制菜刀生锈
C. 铝锅表面生成致密的薄膜
D. 大理石雕像被酸雨腐蚀毁坏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确 的是( )
A.利用太阳能在催化剂参与下分解水制氢是把光能转化为化学能的绿色化学方法
B.蔗糖、淀粉、油脂及其水解产物均为非电解质
C.通过红外光谱分析可以区分乙醇与乙酸乙酯
D.石油催化裂化的主要目的是提高汽油等轻质油的产量与质量;石油裂解的主要目的是得到更多的乙烯、丙烯等气态短链烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列方法中不能证明2HI(g)![]() H2(g)+I2(g)已达到平衡状态的是
H2(g)+I2(g)已达到平衡状态的是
A. 温度和体积一定时,某一生成物浓度不再变化
B. 一个H-H键断裂的同时有两个H-I键断裂
C. 单位时间内生成nmolH2的同时生成nmolHI
D. 温度和体积一定时混合气体的颜色不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为四种短周期主族元素,它们在周期表中的相对位置如下图所示,Z元素原子核外K层与M层电子数相等。下列说法中正确的

A. Y元素最高价氧化物对应的水化物化学式为H3YO4
B. 原子半径由小到大的顺序为:X<Y<W<Z
C. 与同浓度的盐酸反应,Z比W更剧烈
D. X的气态氢化物的稳定性比Y的高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com