
| A. | 淀粉和纤维素都是纯净物 | |
| B. | 油脂不是高分子化合物 | |
| C. | 植物油不能使溴的四氯化碳溶液褪色 | |
| D. | 糖类物质均有甜味 |
分析 A.淀粉、纤维素都是有机高分子,都是混合物;
B.高分子化合物相对分子质量特别大一般达1万以上、一般具有重复结构单元;
C.植物油中含有不饱和的碳碳双键;
D.糖类不一定有甜味.
解答 解:A.它们的通式都是(C6H10O5)n,但聚合物的n不同个体数不确定,长短不一定,也就是说淀粉、纤维素都分别是由长短不一的聚合物混合在一起的,所以都是混合物,故A错误;
B.油脂相对分子质量较小,不属于高分子化合物,故B正确;
C.植物油中含有不饱和的碳碳双键,能与溴发生加成反应,使溴的四氯化碳溶液褪色,故C错误;
D.糖类不一定有甜味如多糖,故D错误;
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握常见有机物的组成、官能团与性质的关系等为解答的关键,注重糖类、油脂基础知识的考查,题目难度不大.


 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L己烷分子数约为NA | |
| B. | 1 mol甲基含10 NA个电子 | |
| C. | 在人体内,180g葡萄糖完全被生理氧化所消耗的氧气的分子数为6NA | |
| D. | 0.5mol 1,3-丁二烯(CH2=CHCH=CH2)分子中含有碳碳双键数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 是非金属元素 | B. | 单质是分子晶体 | ||
| C. | R(OH)4-结合H+的能力小于Al(OH)4- | D. | R2H6中R为-3价 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
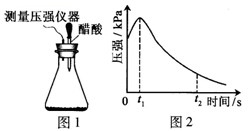
| A. | t2时容器中压强明显小于起始压强原因是铁发生了吸氧腐蚀 | |
| B. | 0~t2时压强变大的原因可能是铁发生了析氢腐蚀 | |
| C. | 0~t1时压强变大的原因可能是腐蚀过程为放热反应,锥形瓶内气体温度升高 | |
| D. | 钢铁在酸性条件下一定发生析氢腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
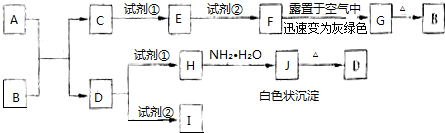
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 反应 | 大气固氮N2(g)+O2(g)?2NO(g) | |
| 温度/℃ | 27 | 2260 |
| K | 3.84×10-31 | 1 |
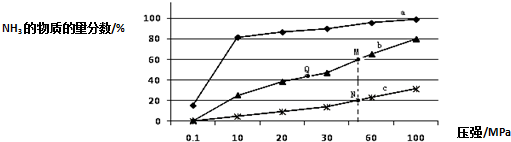
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
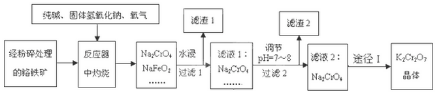
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

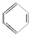 ;④HCHO等,其中碳原子采取sp2杂化的分子有①③④(填序号);HCHO分子的空间构型为平面三角形.
;④HCHO等,其中碳原子采取sp2杂化的分子有①③④(填序号);HCHO分子的空间构型为平面三角形.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com