
 Fe��Cu�����������ʹ�õĽ�����ijУ��ѧ�о���ѧϰС���ͬѧ����ʵ����ֶ��о�Fe��Cu�Լ��������������ʣ���������о����ش��������⣺
Fe��Cu�����������ʹ�õĽ�����ijУ��ѧ�о���ѧϰС���ͬѧ����ʵ����ֶ��о�Fe��Cu�Լ��������������ʣ���������о����ش��������⣺���� ��1��Fe��Cl2��Ӧ����FeCl3��Cu��Cl2��Ӧ����CuCl2��Fe��S��Ӧ����FeS��
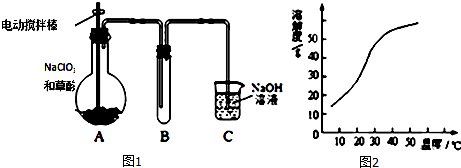
��2��Fe�ܺ��ȵ�ŨHNO3��Ӧ���ɶ������������������ܺ�ˮ��Ӧ����A��Cֱ�����ӣ�C��Һ���ܵ�����A�У�����װ��B���л������á����������ã���ʼ����ǰ����������
��3���ٸ��ݶ������������ʷ��������������ܺ�ˮ��Ӧ�������ᣬ����Һ���������ʱ������������ʣ�࣬����ʺ���ɫ���������ʱ���������ᷴӦ���������������������������ʷ�����
���ȸ���Fe3+��������Ӧ���������������Һ�ж���Һ����Fe3+��Ȼ��������������������Fe2+��Fe2+��������������Fe3+��Һ��ɺ�ɫ���Դ�֤��Fe2+�Ĵ��ڣ�
�۸���Nԭ���غ��֪����Һ��NO3-�����ʵ���n��NO3-��=2n��Fe2+��+2n��Cu2+��������ֻ����ԭ��NO��NO2��0.02mol�����ݵ�ʧ�����غ��������NO�����ʵ�����
��4������Ũ�����ӷ����ֽ�����ʷ������
��� �⣺��1��Cl2�����Խ�ǿ�����۽������ɸ۵Ľ����Ȼ��Fe��Cl2�ķ�Ӧ����FeCl3��Cu��Cl2��Ӧ����CuCl2��S�����Խ��������۽������ɵͼ۵Ľ������Fe��S�ķ�Ӧ����FeS��
�ʴ�Ϊ��B��
��2��Fe�ܺ��ȵ�ŨHNO3��Ӧ��Fe+6HNO3��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$Fe��NO3��3+3NO2��+3H2O�����ɵĶ��������ܺ�ˮ��Ӧ3NO2+H2O=2HNO3+NO����A��Cֱ�����ӣ�C��Һ���ܵ�����A�У�����װ��B���л������á����������ã���ʼ����ǰ��Ӧ������������������
�ʴ�Ϊ���������ã����������ã��ޣ�
��3���ٶ��������ܺ�ˮ��Ӧ���������һ������������Һ���������ʱ�����ƶ����������ܽ⣬����CuƬ�ܽ��ԭ������Ǻ�����HNO3������Ӧ���ɿ���������ɫ���壬�Թ��ϲ����ֺ���ɫ���壬�÷�Ӧ�����ӷ���ʽΪ3Cu+2NO3-+8H+=3Cu2++2NO��+4H2O���������ʱ���������ᷴӦ��������������������ͭ�ܷ�Ӧ���ɶ��������Ӻ�ͭ���ӣ��Ӷ�ʹͭƬ�ܽ⣬������ӦΪ2Fe��NO3��3+Cu=Cu��NO3��2+2Fe��NO3��2��
�ʴ�Ϊ��������ɫ���壻�Թ��ϲ����ֺ���ɫ���壻3Cu+2NO3-+8H+=3Cu2++2NO��+4H2O��2Fe��NO3��3+Cu=Cu��NO3��2+2Fe��NO3��2��
��ȡ������Ӧ�����Һ�����Թ��У�����KSCN��Һ�����������ټ���������ˮ����Һ�����֤����Һ�к���Fe2+������Fe3+��
�ʴ�Ϊ��ȡ����Һ�������μ�������KSCN��Һ�������ֺ�ɫ���ٵμ�����������ˮ�����ֺ�ɫ��
�۱�ͬѧʵ��������ˮϡ�ͺ�õ���Һ500mL����Һ��Fe2+��Cu2+Ũ�Ⱦ�Ϊ0.02mol/L����Һ��NO3-�����ʵ���n��NO3-��=2n��Fe2+��+2n��Cu2+��=2��0.02mol/L��0.5L+2��0.02mol/L��0.5L=0.04mol����NO3-�����ʵ���Ũ��ΪC=$\frac{n}{v}$=$\frac{0.04mol}{0.5L}$=0.08mol/L�������������Ӻ�ͭ����ʧȥ�ĵ��ӵ���+5�۵ĵ��õ��ĵ��ӣ����ݵ�ʧ�����غ�3��n��NO��+1��n��NO2��=2n��Fe2+��+2n��Cu2+��=0.04mol������Nԭ���غ��֪������ԭ��n��HNO3��=n��NO��+n��NO2��=0.02mol����ã�n��NO��=n��NO2��=0.01mol������NO��������ΪV=nVm=0.224L��
�ʴ�Ϊ��0.08�� 0.224��
��4������̽��ʵ���õ�Ũ���ᳬ��ʵ�ʲμӷ�Ӧ����������Ϊ����Ũ�����ӷ���������ӷ������������ȷֽ⣬
�ʴ�Ϊ����Ũ�����ӷ���������ӷ��� ���������ȷֽ⣮
���� ���⿼���˳�������ͭ�����Ļ�ѧ���ʣ���������ʣ�ʵ�����������������ԭ��Ӧ�ļ��㣬���ؿ��������������������ԭ���غ��������ܻ���Ϊ����Ŀ�Ѷ��еȣ�


 �ǻۿ����ܾ�100�ֵ�Ԫ���ؼ��ϵ�д�
�ǻۿ����ܾ�100�ֵ�Ԫ���ؼ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CH4+C12$\stackrel{��}{��}$CH3Cl+HCl | B�� | CH2=CH2+C12�� | ||
| C�� |  +Br2$\stackrel{FeBr_{3}}{��}$ +Br2$\stackrel{FeBr_{3}}{��}$ +HBr +HBr | D�� | CH4+2O2 $\stackrel{��ȼ}{��}$CO2+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | c��A������ʱ��v����kҲ���� | B�� | c��B������ʱ��v����kֵ���� | ||
| C�� | �����¶�ʱ��v����kֵ���� | D�� | �����¶�ʱ��vֵ���䣬k���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | H2SO4��SO2 | B�� | Zn2+��Zn | C�� | H2O��H2 | D�� | CuO��CuCl2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ��֪NH3��HCl������������Ȫʵ������壬������ͬ�������õ������ƿ���ռ���NH3��HCl���壬����ʵ�飨����ƿ�ڳ�����Һ�Ҳ��������ʵ���ɢ��������˵��������ǣ�������
��֪NH3��HCl������������Ȫʵ������壬������ͬ�������õ������ƿ���ռ���NH3��HCl���壬����ʵ�飨����ƿ�ڳ�����Һ�Ҳ��������ʵ���ɢ��������˵��������ǣ�������| A�� | NH3��HCl�ֱ��γ���ɫ����ɫ��Ȫ | |
| B�� | �Ʊ������NH3��HCl������ĸ�����ֱ��Ǽ�ʯ�ҡ�Ũ���� | |
| C�� | ��ΪNO2���壬������Һ���ʵ����ʵ���Ũ����ǰ���߲�ͬ | |
| D�� | ȥ��װ���еĽ�ͷ�ιܣ���Ϊ��������Ҳ��������Ȫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����̿ȥ�������е���ζ | B�� | ʳ�׳�ˮ�� | ||
| C�� | Ư�۾��������� | D�� | ������ʳƷ���ڵ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ���� | �μӷ�Ӧ������ | ������ |
| �� | Cl2��FeBr2 | FeCl3��FeBr3 |
| �� | KMnO4��H2O2��H2SO4 | K2SO4��MnSO4 �� |
| �� | MnO4- �� | Cl2��Mn2+ �� |
| A�� | �ڢ��鷴Ӧ��Cl2�� FeBr2�����ʵ���֮��Ϊ1��2 | |
| B�� | �ڢ��鷴Ӧ���������ΪH2O�� O2 | |
| C�� | ��������ǿ����˳��MnO4-��Cl2��Fe3+��Br2 | |
| D�� | �ڢ��鷴Ӧ������1mol Cl2��ת�Ƶ���2mol |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com