
 �Ȼ�ѧ����ʽ�е�Hʵ����������ѧ�е�һ���������������ʣ�һ����ϵ���ʣ�H����ֽ��ֵ��ĿǰΪֹ��û�а취��ã�������ϵ�����仯ʱ�����ǿ��Բ����ϵ���ʵı仯�����ʱ䣬�á���H����ʾ����H=H����̬��-H��ʼ̬����
�Ȼ�ѧ����ʽ�е�Hʵ����������ѧ�е�һ���������������ʣ�һ����ϵ���ʣ�H����ֽ��ֵ��ĿǰΪֹ��û�а취��ã�������ϵ�����仯ʱ�����ǿ��Բ����ϵ���ʵı仯�����ʱ䣬�á���H����ʾ����H=H����̬��-H��ʼ̬�������� ��1����ѧ��Ӧ������һ�������������ı仯����Ӧ�ʱ���Ҫ��ָ��Ӧǰ��������仯�����������غ�����ʱ䣬����ʱ���㣺��H=H����̬��-H��ʼ̬����Hȷ����Ӧ���ȷ��ȣ���H��0Ϊ���ȷ�Ӧ����H��0Ϊ���ȷ�Ӧ��
��2����ѧ��Ӧ���ʱ��뷴Ӧ���������ļ����йأ���H=H����̬��-H��ʼ̬������������������õ���
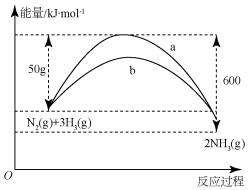
��3�������ǽ��ͷ�Ӧ�Ļ�ܣ��ӿ췴Ӧ���ʣ����ı�ƽ�⣬����b�Ƿ�Ӧ�Ļ�ܽ����ˣ���Ӧ���ʱ䲻�䣮
��� �⣺��1����ѧ��Ӧ������һ�������������ı仯����Ӧ�ʱ���Ҫ��ָ��Ӧǰ��������仯�����ڻ�ѧ��ӦA+B=C+D����H��A��+H��B����H��C��+H��D����H=H����̬��-H��ʼ̬�����жϿ�֪��H��0����Ӧ�Ƿ��ȷ�Ӧ��
�ʴ�Ϊ��С�ڣ� ���ȣ�
��2����֪��H2��g��+Cl2��g��=2HCl��g����H=-185kJ•mol-1����298H��H2��=436kJ•mol-1����H298��Cl2��=247kJ•mol-1�����ݡ�H=H����̬��-H��ʼ̬����
��H=2��H298��HCl��-��H298��H2��-��H298��Cl2��=-185kJ•mol-1�����H298��HCl��=434 kJ•mol-1��
�ʴ�Ϊ��434 kJ•mol-1 ��
��3���÷�Ӧ�ų��������������յ����������Է��ȣ���H=�ų�������-���յ�����=600kJ/mol-508kJ/mol=92kJ/mol���÷�Ӧ���Ȼ�ѧ����ʽΪ��N2��s��+3H2��g��=2NH3��g������H=-92 kJ/mol�������ܸı䷴Ӧ��·����ʹ������Ӧ����Ļ�ܽ��ͣ������ı仯ѧƽ�⣬��Ӧ����ЧӦ���䣬��������b�Ƿ�Ӧ�Ļ�ܽ����ˣ���Ӧ���ʱ䲻�䣬�����Ǽ����˴������£�
�ʴ�Ϊ��aδʹ�ô�����bʹ���˴�����
���� ���⿼���˷�Ӧ�������仯����Ӧ���ʱ���㷽�����ʱ��������ʵļ����ϵ����˹���ɵļ���Ӧ�ã���Ŀ�Ѷ��еȣ�����������ѧ�������Ӧ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Һ�п϶���SO42-��Cu2+��һ��û��Ba2+���������Ӳ���ȷ�� | |
| B�� | ��Һ�п϶���SO42-��Cu2+��������Na+��Cl- | |
| C�� | ��Һ�п϶���SO42-��Cu2+��Cl-��������Na+ | |
| D�� | ��Һ�����ͬʱ��Na+��Cl-����C��Na+����C��Cl-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������Һ������������̼��Ӧ��C6H5O-+CO2+H2O=C6H5OH+HCO3- | |
| B�� | ̼������������ʯ��ˮ��Ӧ��HCO3-+Ca2++OH-=CaCO3��+H2O | |
| C�� | ��������KHSO4��Һ�е���Ba��OH��2��Һʹ��ҺpH=7��SO42-+2H++Ba2++2OH-=BaSO4��+2H2O | |
| D�� | ��KAl��SO4��2��Һ�м�������������Һ��SO42-������ȫ��Al3++2SO42-+2Ba2++4OH-=2BaSO4��+AlO2-+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ʵ��Ŀ�� | ʵ����� | |
| A | ��֤��Ȳ�ܱ����Ը��������Һ���� | ���Ҵ���Ũ���ᷴӦ���ɵ�����ͨ�����Ը��������Һ���۲���Һ�Ƿ���ɫ |
| B | �������ˮ�����Ļ�ԭ�� | ȡ����������Һ����ϡ���Ṳ�Ⱥ��ټ���������Һ��ˮԡ���ȣ��۲��Ƿ�������� |
| C | �����������е���Ԫ�� | ȡ���������飬������������Һ���Ⱥ������������Һ���۲��Ƿ����dz��ɫɫ���� |
| D | ֤����������ȥ��Ӧ����ϩ���� | ���Թ��м����������������NaOH���Ҵ���Һ�����ȣ�����Ӧ������������ͨ��ʢ��ˮ��ϴ��ƿ��ͨ�����Ը��������Һ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CO | B�� | CO2 | C�� | C2H4 | D�� | C2H6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CH3��CH2��4CH3������ | B�� | ��CH3��2CHCH��CH3��2 2��3-�������� | ||
| C�� | ��C2H5��2CHCH3��2-�һ����� | D�� | C2H5C��CH3��3�� 2��2-�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��ͼΪ�Զ��Ե缫���е���װ�ã�
��ͼΪ�Զ��Ե缫���е���װ�ã��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������ˮ������Ƿ���л�ԭ�ԣ���������ˮ������Һ��ֱ�Ӽ������Ƶ�Cu��OH��2������ | |
| B�� | ���顢��ϩ�ͱ��ڹ�ҵ�϶���ͨ��ʯ�ͷ���õ� | |
| C�� | �����Ӳ֬�ụΪͬϵ�C6H14��C9H20Ҳһ����Ϊͬϵ�� | |
| D�� | �Ե�����ĽṹΪ �����Է���������ˮ�⡢�ӳɵȷ�Ӧ �����Է���������ˮ�⡢�ӳɵȷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
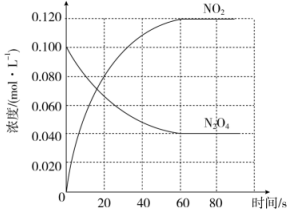 ���ݻ�Ϊ1.00L�������У�ͨ��һ������N2O4��������ӦN2O4��g��?2NO2��g�������¶����ߣ�����������ɫ���
���ݻ�Ϊ1.00L�������У�ͨ��һ������N2O4��������ӦN2O4��g��?2NO2��g�������¶����ߣ�����������ɫ����鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com