
下列关于甲、乙、丙、丁四种仪器装置的有关用法, 其中不合理的是( )
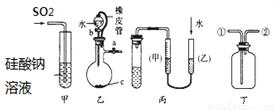
A. 甲装置:可用来证明硫的非金属性比硅强
B. 乙装置:橡皮管的作用是能使水顺利流下
C. 丙装置:用图示的方法能检查此装置的气密性
D. 丁装置:可在瓶中先装入某种液体收集NO气体
科目:高中化学 来源:2017届江苏省、溧水高级中学)等六校高三2月联考化学试卷(解析版) 题型:选择题
在给定条件下,下列选项中所示的物质间转化均能一步实现的是
A. 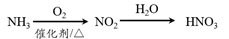
B. 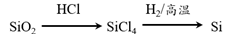
C. 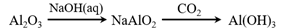
D. 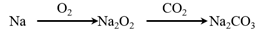
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三下学期开学考试化学试卷(解析版) 题型:简答题
随着科技的进步,合理利用资源、保护环境成为当今社会关注的焦点
(1)氨氮是造成水体富营养化的重要因素之一,用次氯酸钠水解生成的次氯酸将水中的氨氮(用NH3表示)转化为氮气除去,其相关反应的主要热化学方程式如下:
反应①:NH3(aq)+HClO(aq)= NH2Cl(aq)+H2O(l)△H1= akJ•mol﹣1
反应②:NH2Cl(aq)+HClO(aq)= NHCl2(aq)+H2O(I)△H2= bkJ•mol﹣1
反应③:2NHCl2(aq)+H2O(l)= N2(g)+HClO(aq)+3HCl(aq)△H3= ckJ•mol﹣1
① 2NH3(aq)+3HClO(aq)= N2(g)+3H2O(I)+3HCl(aq)的△H=______。
② 溶液pH对次氯酸钠去除氨氮有较大的影响(如图1所示)。在pH较低时溶液中有无色无味的气体生成,氨氮去除效率较低,其原因是_________________。
③ 用电化学法也可以去除废水中氨氮.在蒸馏水中加入硫酸铵用惰性电极直接电解发现氨氮去除效率极低,但在溶液中再加入一定量的氯化钠后,去除效率可以大大提高。反应装置如图2所示,b为电极__极,电解时阴极的电极反应式为_____________。
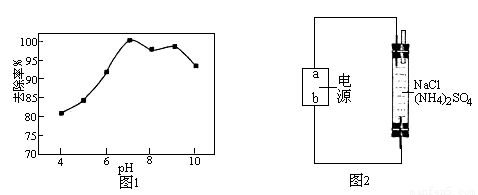
(2)“低碳经济”正成为科学家研究的主要课题。
① 以二氧化钛表面覆盖Cu2Al2O4 为催化剂,可以将CO2 和CH4 直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率如右图所示。250~300 ℃时,温度升高而乙酸的生成速率降低的原因是__________________。
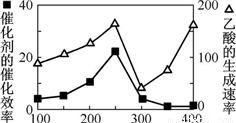
② 为了提高该反应中CO2的转化率,可以采取的措施是_____________。(写一条即可)
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三下学期开学考试化学试卷(解析版) 题型:选择题
下列有关物质的性质与用途具有对应关系的是
A. Al具有良好延展性和抗腐蚀性,可制成铝箔包装物品
B. 浓硫酸具有脱水性,可用于干燥NH3、SO2等
C. 明矾易溶于水,可用作净水剂
D. 苯酚具有强氧化性,可加入药皂起到杀菌消毒的作用
查看答案和解析>>
科目:高中化学 来源:2017届福建省漳州市八校高三2月联考化学试卷(解析版) 题型:选择题
下图是某校实验小组设计的一套原电池装置,下列有关描述 不正确的是( )
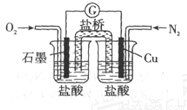
A. 石墨的电极反应: 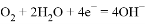
B. 此装置能将化学能转变为电能
C. 电子由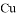 电极经导线流向石墨电极
电极经导线流向石墨电极
D. 电池总反应: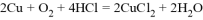
查看答案和解析>>
科目:高中化学 来源:2017届福建省漳州市八校高三2月联考化学试卷(解析版) 题型:选择题
下列各组离子中,一定能够大量共存的是( )
A. Na+、Al3+、Cl-、CO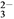 B. Fe2+、H+、SO
B. Fe2+、H+、SO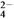 、NO
、NO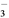
C. K+、Fe3+、NO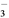 、SCN- D. Mg2+、NH
、SCN- D. Mg2+、NH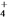 、Cl-、SO
、Cl-、SO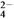
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省淮安市高一上学期期末调研测试化学试卷(解析版) 题型:填空题
填空:
(1)0. 5 mol NH3分子中所含氮原子数为__________个;
(2)1.2g RSO4中含0.01 mol R2+,则RSO4的摩尔质量是__________;
(3)0.1 mol·L-1的 Cu(NO3)2溶液中NO3-的物质的量浓度是__________;
(4)新制氯水在阳光照射下产生的无色气体是__________;
(5)配制100 mL 1 mol/L NaCl溶液,定容后,把容量瓶倒置摇匀后发现液面低于刻度线,补加水至刻度处,会引起所配溶液物质的量浓度__________(选填“偏高、偏低、无影响”);
(6)实验室制备氯气时,收集氯气常采用__________法。
查看答案和解析>>
科目:高中化学 来源:2017届山东省菏泽市高三上学期期末学分认定考试B卷化学试卷(解析版) 题型:简答题
随着大气污染的日趋严重,“节能减排”,减少全球温室气体排放,研究NOx、SO2、CO等大气污染气体的处理具有重要意义。
(1)下图是在101 kPa,298K条件下1mol NO2和1mol CO反应生成1mol CO2和1mol NO过程中的能量变化示意图。
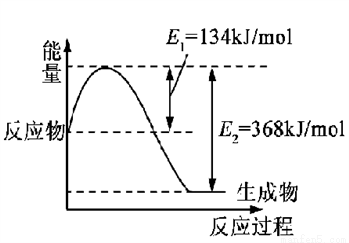
已知:① N2(g)+O2(g)=2NO(g) △H= +179.5kJ/mol
② 2NO(g)+O2(g)=2NO2(g) △H= -112.3kJ/mol
请写出NO与CO反应生成无污染气体的热化学方程式: ____________________
(2)将0.20 mol NO2和0.10 mol CO充入一个容积恒定为1L的密闭容器中发生反应,在不同条件下,反应过程中部分物质的浓度变化状况如下图所示。
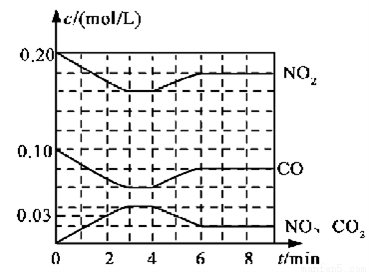
①下列说法正确的是___________(填序号)。
a.容器内的压强不发生变化说明该反应达到平衡
b.当向容器中再充入0.20 mol NO时,平衡向正反应方向移动,K增大
c.升高温度后,K减小,NO2的转化率减小
d.向该容器内充入He气,反应物的体积减小,浓度增大,所以反应速率增大
②计算产物NO在0~2 min内平均反应速率v(NO)=__________mol·L-1·min-1
③第4 min时改变的反应条件为__________________。
④计算反应在第6 min时的平衡常数K=________。若保持温度不变,此时再向容器中充入CO、NO各0.060 mol,平衡将________移动(填“正向”、“逆向”或“不”)。
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三下学期二调考试理综化学试卷(解析版) 题型:填空题
A、B、C、D、E、F均为周期表中前四周期的元素。请按要求回答下列问题。
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如下表所示:

下列有关A、B的叙述不正确的是(____)a.离子半径A<B b.电负性A<B
c.单质的熔点A>B d.A、B的单质均能与氧化物发生置换
e.A的氧化物具有两性 f.A、B均能与氯元素构成离子晶体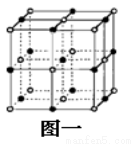
(2)C是地壳中含量最高的元素,C基态原子的电子排布式为_______。Cn-比D2+少l个电子层。二者构成的晶体的结构与NaCl晶体结构相似(如图一所示),晶体中一个D2+周围和它最邻近且等距离的D2+有_____个。
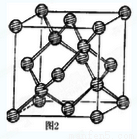
(3)E元素原子的最外层电子数是其次外层电子数的2倍,则乙酸分子中E原子的杂化方式有_____。E的一种单质其有空间网状结构,晶胞结构如图2。己知位于晶胞内部的4个原子,均位于体对角线的1/4或3/4处,E-E键长为apm,则E晶体的密度为_________g/cm3(用含有NA、a的式子表示)。
(4)F与硒元素同周期,F位于p区中未成对电子最多的元素族中,F的价电子排布图为
______,FO33-离子的空间构型为__________;F第一电离能_______硒元素(填“>”或“<”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com