
| A.Fe3O4 | B.MnO2 | C.V2O5 | D.Cr2O3 |
科目:高中化学 来源:不详 题型:单选题
| A.铝制品在生活中被广泛使用,说明铝是一种不活泼的金属 |
| B.氧化铝的熔点很高,是一种较好的耐火材料 |
| C.Al(OH)3碱性很强,故可用于治疗胃酸过多 |
| D.铝是地壳中含量最多的元素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
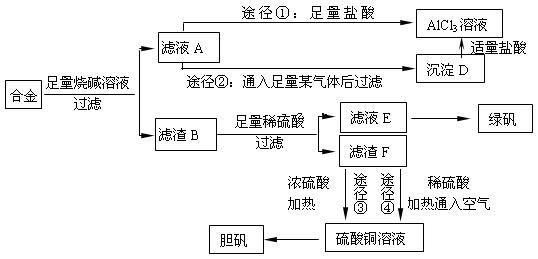
 是 。上述实验方案多处采用了过滤操作,过滤所用到的玻璃仪器有 和玻璃棒;其中玻璃棒的作用是 。
是 。上述实验方案多处采用了过滤操作,过滤所用到的玻璃仪器有 和玻璃棒;其中玻璃棒的作用是 。 ④制取胆矾,必须进行的实验操作步骤:加硫酸、加热通氧气、过滤、 、冷却结晶、 、自然干燥。其中“加热通氧气”所起的作用为 (用离子方程式表示)。
④制取胆矾,必须进行的实验操作步骤:加硫酸、加热通氧气、过滤、 、冷却结晶、 、自然干燥。其中“加热通氧气”所起的作用为 (用离子方程式表示)。 (5)测定所得胆矾(CuSO4·xH2O)中x值的实验方案是蒸发硫酸铜晶体中的水得到白色的无水硫酸铜,冷却后称量。此变化的化学方程式为:CuSO4·xH2O===C
(5)测定所得胆矾(CuSO4·xH2O)中x值的实验方案是蒸发硫酸铜晶体中的水得到白色的无水硫酸铜,冷却后称量。此变化的化学方程式为:CuSO4·xH2O===C uSO4+xH2O ,但温度过高,CuSO4会继续分解为CuO和SO3。在此实验过程中,称量操作至少进行 次。若测定结果x值偏高,可能的原因是 。
uSO4+xH2O ,但温度过高,CuSO4会继续分解为CuO和SO3。在此实验过程中,称量操作至少进行 次。若测定结果x值偏高,可能的原因是 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
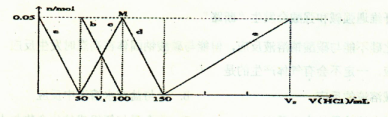
| A.原混合溶液中的CO32-与AlO2-的物质的量之比为1:2 |
| B.V1:V2=1:5 |
| C.M点时生成的CO2为0.05mol |
| D.a曲线表示的离子方程式为:AlO2-+H++H2O=Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.100mL | B.150mL | C.200mL | D.300mL |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.5mol | B.3mol | C.b/2mol | D.5b/3mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
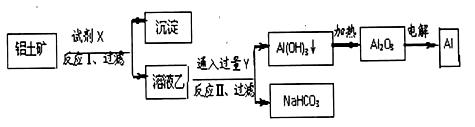
| A.试剂X为氢氧化钠溶液,试剂Y为CO2 |
| B.结合质子(H+)的能力南强到弱的顺序是CO32->AlO2->OH |
| C.反应Ⅱ中生成Al(OH)3的反应为CO2+AlO2-+2H2O=Al(OH)3↓+HCO3- |
| D.Al2O3熔点很高,电解时向Al2O3中加入冰晶石,使Al2O3的熔点降低,从而减少冶炼过程中能量消耗。 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com