
【题目】基于临床研究,抗疟疾药物磷酸氯喹被证实在治疗新冠肺炎过程中具有疗效。4,7-二氯喹啉是合成磷酸氯喹的一种中间体,其结构简式如图所示。下列有关该物质的说法正确的是( )
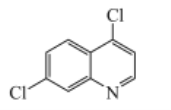
A.1mol 4,7-二氯喹啉最多可以消耗2molNaOH
B.分子中不可能所有原子在同一平面上
C.分子式为C8H5NCl2
D.苯环上的一氯代物有3种
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源: 题型:
【题目】实验室为监测空气中汞蒸气的含量,往往悬挂涂有CuI的滤纸,根据滤纸是否变色或颜色发生变化所用去的时间来判断空气中的含汞量,其反应为4CuI+Hg=Cu2HgI4+2Cu。
(1)上述反应产物Cu2HgI4中,Cu元素显__价。
(2)以上反应中的氧化剂为__,当有1molCuI参与反应时,转移电子_mol。
(3)标明上述反应电子转移的方向和数目____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃、101KPa下,1g甲醇燃烧生成CO2和液态水时放热22.68KJ,下列热化学方程正确的是
A.CH3OH(l)+![]() O2(g)=CO2(g)+2H2O(l) ΔH=+725.8KJ/mol
O2(g)=CO2(g)+2H2O(l) ΔH=+725.8KJ/mol
B.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=-1452KJ/mol
C.CH3OH(l)+![]() O2(g)=CO2(g)+2H2O(g) ΔH=-725.8KJ/mol
O2(g)=CO2(g)+2H2O(g) ΔH=-725.8KJ/mol
D.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH=-1452KJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】50 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1 NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃仪器是________。烧杯间填满碎泡沫塑料的作用是________

(2)大烧杯上如不盖硬纸板,求得的中和热数值_______ (填“偏大”、“偏小”或“无影响”)。
(3)实验中改用60 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1 NaOH溶液进行反应,与上述实验相比,所放出的热量__________(填“相等”或“不相等”),所求中和热__________(填“相等”或“不相等”),
(4)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会_____(填“偏大”“偏小”或“无影响”)。
(5)写出该反应的热化学方程式:____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组进行Fe(OH)3胶体的制备实验并检验其性质。
(1)若将饱和FeCl3溶液分别滴入下列物质中,能形成胶体的是________(填字母)。
A.冷水 B.沸水 C.NaOH浓溶液 D.NaCl浓溶液
(2)现有甲、乙、丙三名同学进行Fe(OH)3胶体的制备:
①甲同学的操作:取一小烧杯,加入25 mL蒸馏水加热至沸腾,向沸水中逐滴加入1~2 mL FeCl3饱和溶液,继续煮沸至混合液呈红褐色,停止加热。请评价该操作是否正确______。
②乙直接加热饱和FeCl3溶液,请评价是否正确______。
③丙向沸水中滴加饱和FeCl3溶液,为了使反应进行充分,煮沸10分钟,请评价是否正确________。
(3)写出制备Fe(OH)3胶体的化学方程式: ____________________。证明有Fe(OH)3胶体生成的实验操作是_____________________。该操作利用胶体的性质是________。
(4)Fe(OH)3胶体稳定存在的主要原因是____________________(填字母,下同)。
A.胶体粒子直径小于1nm B.胶体粒子带正电荷
C.胶体粒子作布朗运动 D.胶体粒子能透过滤纸
(5)Fe(OH)3胶体区别于FeCl3溶液最本质的特征是________。
A.Fe(OH)3胶体粒子的直径在1~100 nm之间
B.Fe(OH)3胶体具有丁达尔效应
C.Fe(OH)3胶体是均一的分散系
D.Fe(OH)3胶体的分散质能透过滤纸
(6)若取少量制得的胶体加入试管中,加入硫酸铵溶液,现象是_____________,这种现象称为胶体的________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。在恒容密闭容器中,将CO和H2S混合加热并达到下列平衡:
CO(g)+H2S(g)![]() COS(g)+H2(g) K=0.1
COS(g)+H2(g) K=0.1
反应前CO物质的量为10mol,平衡后CO物质的量为8mol。下列说法正确的是
A. 升高温度,H2S浓度增加,表明该反应是吸热反应
B. 通入CO后,正反应速率逐渐增大
C. 反应前H2S物质的量为7mol
D. CO的平衡转化率为80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某有机物由C、H、O三种元素组成,球棍模型如图所示:
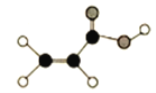
①含有的官能团名称是_______;
②写出此有机物与金属钠反应的化学方程式_______。
(2)四种常见有机物分子的比例模型示意图如下,其中甲、乙、丙为烃,丁为烃的衍生物。

①可以鉴别甲和乙的试剂为_________;
a.稀硫酸 b.溴的四氯化碳溶液 c.水 d.酸性高锰酸钾溶液
②上述物质中有毒、有特殊气味,且不溶于水、密度比水小的是_________(填名称),
③乙和丁的物质的量共1.5mol,完全燃烧需要的氧气的物质的量是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】坦桑石的主要化学成分为Ca2Al3(SiO4)3(OH),还可含有V、Cr、Mn等元素。
(1)下列状态中的铝微粒,电离最外层的一个电子所需能量最大的是____________。
①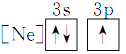 ②
②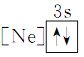 ③
③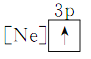 ④
④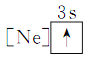
(2)烟酸铬是铬的一种化合物,其合成过程如下:
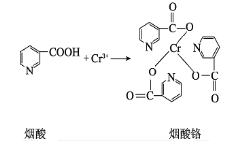
①Cr原子的价层电子排布图为 _______________。这样排布电子遵循的原则是 ______________。
②烟酸中所含元素的第一电离能I1(N)_____ I1(O),原因是_________________ 。
③烟酸中碳、氮原子的杂化方式分别为 _________________、__________________。
(3)SiCl4、SiF4都极易水解。二者都属于______(填“极性”或“非极性”)分子,其熔点关系为SiF4 ______SiCl4(填“>”“<”或“=”)。
(4)将Mn掺入GaAs晶体(图甲)可得到稀磁性半导体材料(图乙),图甲、图乙晶体结构不变。
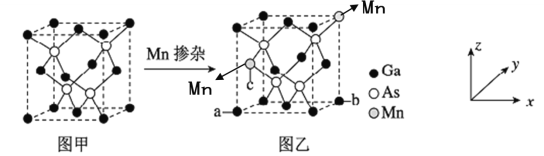
①图乙中a点和b点的原子坐标参数分别为(0,0,0)和(1,1,0),则c点的原子坐标参数为_______。
②设图甲晶体的密度为ρg·cm-3,用NA表示阿伏伽德罗常数的数值,则该晶胞中距离最近的两个砷原子之间的距离为 ___________ pm。(用含ρ、NA的关系式表示最简化的计算式即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次硫酸氢钠甲醛(aNaHSO2bHCHOcH2O)在印染、医药以及原子能工业中应用广泛。以Na2SO3、SO2、HCHO和锌粉为原料制备次硫酸氢钠甲醛的实验步骤如下:

步骤1:在如图所示装置的烧瓶中加入一定量Na2SO3和水,搅拌溶解,缓慢通入SO2,至溶液pH约为4,制得NaHSO3溶液。
步骤2:将装置A中导气管换成橡皮塞。向烧瓶中加入稍过量的锌粉和一定量甲醛溶液,在80~90℃下,反应约3h,冷却至室温,抽滤。
步骤3:将滤液真空蒸发浓缩,冷却结晶。
(1)装置B的烧杯中应加入的溶液是___。
(2)步骤2中加入锌粉时有NaHSO2和Zn(OH)2生成。
①写出加入锌粉时发生反应的化学方程式:___。
②生成的Zn(OH)2会覆盖在锌粉表面阻止反应进行,防止该现象发生的措施是___。
(3)冷凝管中回流的主要物质除H2O外,还有___(填化学式)。
(4)步骤3中次硫酸氢钠甲醛不在敞口容器中蒸发浓缩的原因是___。
(5)步骤2抽滤所得滤渣的成分为Zn和Zn(OH)2,利用滤渣制备ZnO的实验步骤为:将滤渣置于烧杯中,___,900℃煅烧。(已知:Zn与铝类似,能与NaOH溶液反应;Zn2+开始沉淀的pH为5.9,沉淀完全的pH为8.9,pH>11时,Zn(OH)2能生成ZnO22-。实验中须使用的试剂有1.0molL-1NaOH溶液、1.0molL-1HCl溶液、水)
(6)产物组成测定实验:
准确称取1.5400g样品,溶于水配成l00mL溶液;取25.00mL样品溶液经AHMT分光光度法测得溶液吸光度A=0.4000(如图);另取25.00mL样品溶液,加入过量碘水后,加入BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重得到BaSO4固体0.5825g。
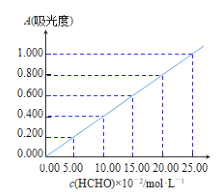
①样品溶液HCHO浓度为___molL-1。
②通过计算确定aNaHSO2·bHCHOcH2O的化学式为___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com