
| A. | NH4HCO3溶液与过量NaOH溶液反应:NH4++OH-═NH3•H2O | |
| B. | 漂白粉的稀溶液中通入过量SO2气体:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO | |
| C. | 用FeC1 溶液腐蚀印刷电路板:Fe3++Cu═Fe2++Cu2+ | |
| D. | 含有a mol FeBr2的溶液中,通入 a mol Cl2:2Fe2++2Br-+2Cl2═Br2+2Fe3++4Cl- |
分析 A.漏掉氢氧根离子与碳酸氢根离子的反应;
B.次氯酸根离子具有强的氧化性,能够氧化二氧化硫;
C.电荷不守恒;
D.等物质的量溴化亚铁与氯气反应,二价铁离子全部被氧化,溴离子一半被氧化.
解答 解:A.NH4HCO3溶液与过量NaOH溶液反应,离子方程式:HCO3-+NH4++2OH-═NH3•H2O+CO32-+H2O,故A错误;
B.漂白粉溶液中通入过量SO2的离子反应为:Ca2++2ClO-+2H2O+2SO2=CaSO4↓+4H++2Cl-+SO42-,故B错误;
C.用FeC1 溶液腐蚀印刷电路板,离子方程式:2Fe3++Cu═2Fe2++Cu2+,故C错误;
D.含有a mol FeBr2的溶液中,通入 a mol Cl2,离子方程式:2Fe2++2Br-+2Cl2═Br2+2Fe3++4Cl-,故D正确;
故选:D.
点评 本题考查离子反应方程式的书写,明确发生的化学反应是解答本题的关键,注意离子方程式的书写遵循客观事实、遵循原子个数、电荷数守恒规律,注意氧化还原反应的先后规律,题目难度中等.


 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 解释或结论 |
| A | 将FeCl3溶液加入Mg(OH)2悬浊液中,振荡,可观察到沉淀由白色变为红褐色 | Fe(OH)3的溶解度小于Mg(OH)2的 |
| B | 用蒸馏水润湿的pH试纸测溶液的pH | 一定会使测定结果偏低 |
| C | 测定中和热时,使用碎泡沫起隔热保温的作用,用普通玻璃棒进行搅拌使酸和碱充分反应,准确读取实验时的最高温度并且取2~3次的实验平均值等,以达到良好的实验效果 | 用简易量热计测定反应热 |
| D | 用氢氧化钾与浓硫酸测定中和反应的反应热 | 测得的结果偏小 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 改变压强,平衡不发生移动,反应放出的热量不变 | |
| B. | 加入催化剂,改变了反应的途径,反应的△H也随之改变 | |
| C. | 升高温度,反应速率加快,反应放出的热量不变 | |
| D. | 若在原电池中进行,反应放出的热量不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ①④⑥ | C. | ②③⑥ | D. | ①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18g H2O中含有的质子数为10NA | |
| B. | 25℃、101 kPa下,16 g O3和O2混合气体中含有的氧原子数为NA | |
| C. | 2.24LCO2中含有的原子数为0.3 NA | |
| D. | 1mol Na与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓硫酸---蒸馏 | B. | 饱和食盐水---蒸馏 | ||
| C. | 饱和碳酸氢钠溶液---分液 | D. | 饱和碳酸钠溶液---分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | x+y<z | B. | 平衡正向移动 | C. | B的浓度增大 | D. | A的转化率降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
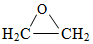 +CaCl2+2H2O
+CaCl2+2H2O +CaCl2+H2O
+CaCl2+H2O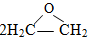
| A. | 12.7% | B. | 25.4% | C. | 50.8% | D. | 76.2% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | T℃1 L pH=6 的纯水中含 10-6 NA个 OH | |
| B. | 6.0 g SiO2 晶体中含有 0.1 NA 个 SiO2分子 | |
| C. | 标准状况下,22.4 L HF 所含电子数为 10NA | |
| D. | 标准状况下,22.4 L 氧气作氧化剂时转移电子数一定为 4NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com