
【题目】某烃A的相对分子质量为84.回答下列问题:
(1)烃A的分子式为 .
(2)若烃A为链烃,分子中所有的碳原子在同一平面上,该分子的一氯取代物只有一种. ①A的结构简式为名称为 .
②链烃A与Br2的CCl4溶液反应生成B,写出由A生成B的化学方程式: .
③与A互为同分异构体,且主链碳原子个数与A相同的链烃有种(不包括A)
(3)若A不能使Br2的CCl4溶液褪色,且其一氯代物只有一种,则A的结构简式为 .
【答案】
(1)C6H12
(2)![]() ;2,3﹣二甲基﹣2﹣丁烯;
;2,3﹣二甲基﹣2﹣丁烯; ![]() +Br2→
+Br2→ 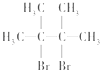 ;2
;2
(3)![]()
【解析】解:(1)烃A的相对分子质量为84,则该烃可能为烯烃或环烷烃,分子式应为C6H12,
所以答案是:C6H12;(2)①若烃A为链烃,应含有一个碳碳双键,分子中所有的碳原子在同一平面上,该分子的一氯取代物只有一种,则A为 ![]() ,名称为:2,3﹣二甲基﹣2﹣丁烯,
,名称为:2,3﹣二甲基﹣2﹣丁烯,
所以答案是: ![]() ;2,3﹣二甲基﹣2﹣丁烯;
;2,3﹣二甲基﹣2﹣丁烯;
② ![]() 与Br2发生2,3位加成反应,生成则B为
与Br2发生2,3位加成反应,生成则B为 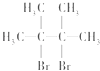 ,故方程式为
,故方程式为 ![]() +Br2→
+Br2→ 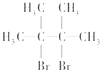 ,
,
所以答案是: ![]() +Br2→
+Br2→  ;
;
③与A互为同分异构体,且主链碳原子个数与A相同的链烃有:CH2=C(CH2)CH(CH3)2,CH2=CHC(CH3)3,
所以答案是:2;(3)若A不能使溴水褪色,且其一氯代物只有一种,则A为环己烷,结构简式为: ![]() ,
,
所以答案是: ![]() .
.


科目:高中化学 来源: 题型:
【题目】下列关于水和无机盐的叙述中,错误的是
A. 无机盐是细胞中能源物质之一 B. 水在维持细胞形态中有重要作用
C. 某些无机盐参与构成细胞复杂化合物 D. 水在活细胞中主要以自由水形式存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用化学反应原理研究氮及其化合物意义重大。请回答下列问题:
(1)已知: N2(g)+3H2(g)![]() 2NH3(g) △H=-92.4 kJ/mol
2NH3(g) △H=-92.4 kJ/mol
N2(g)+O2(g)=2NO(g) △H=+180.5 kJ/mol
2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ/mol
若有34g氨气经催化氧化完全生成一氧化氮气体和水蒸气所放出的热量为_______。
(2)T1温度时,在容积为2 L 的恒容密闭容器中发生反应: 2NO(g)+O2(g)![]() 2NO2(g) △H<0。实验测得:v正=v(NO)消耗=2v(O2 )消耗=k正c2(NO)·c(O2),v逆=v(NO2)消耗=k逆c2(NO2) ,k正、k逆为速率常数,受温度影响。容器中各反应物和生成物的物质的量随时间变化如图所示:
2NO2(g) △H<0。实验测得:v正=v(NO)消耗=2v(O2 )消耗=k正c2(NO)·c(O2),v逆=v(NO2)消耗=k逆c2(NO2) ,k正、k逆为速率常数,受温度影响。容器中各反应物和生成物的物质的量随时间变化如图所示:
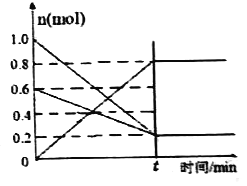
①下列说法能表明该反应已达到平衡状态的是______(填序号)。
A.混合气体的密度不变 B.混合气体的颜色不变
C. k正、k逆不变 D.2v正(O2)= v逆(NO2)
②化学平衡常数K与速率常数k正、k逆的数学关系是K=_______。
③T1温度时,化学平衡常数K=______。将容器的温度改变为T2时,若k正=k逆 ,则T2___T1 (填“>”、“<”或“=”)。
(3) 亚硝酸是氮元素重要的含氧酸之一。25℃,测得amol/LHNO2稀溶液的pH=b,该温度下HNO2电离平衡常数的精确计算表达式为K=______(用含a、b的代数式表示)。将amol/L的NaCN溶液与0.01mol/L的盐酸等体积混合后,测得溶液pH=7,则溶液中![]() =_____(用含a 的代数式表示)。
=_____(用含a 的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知(HF)2(g)2HF(g),△H>0,且平衡体系的总质量[m(总)]与总物质的量[n(总)]之比在不同温度下随压强的变化曲线如图所示.下列说法正确的是( ) 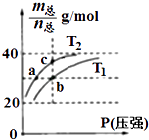
A.温度:T1<T2
B.平衡常数:K(a)=K(b)<K(c)
C.反应速率:Vb>Va
D.当 ![]() =30g/mol时,n(HF):n(HF)2=2:1
=30g/mol时,n(HF):n(HF)2=2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇既可用于基本有机原料,又可作为燃料用于替代矿物燃料.
(1)以下是工业上合成甲醇的反应:CO(g)+2H2(g)CH3OH(g)△H 下表所列数据是该反应在不同温度下的化学平衡常数(K).
温度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.270 | 0.012 |
由表中数据判断反应I为热反应(填“吸”或“放”).
某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2mol/L,则CO的转化率为 , 此时的温度为(从表中选择).
(2)已知在常温常压下: ①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H1 kJ/mol
②2CO(g)+O2(g)=2CO2(g)△H2 kJ/mol
③H2O(g)=H2O(l)△H3 kJ/mol
则反应 CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=kJ/mol(用△H1、△H2、△H3表示)
(3)现以甲醇燃料电池,采用电解法来处理酸性含铬废水(主要含有Cr2O72)时,实验室利用如图装置模拟该法: 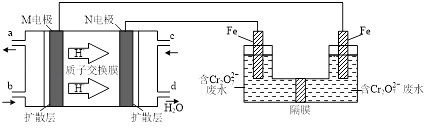
①N电极的电极反应式为 .
②请完成电解池中Cr2O72转化为Cr3+的离子反应方程式:
Cr2O72+Fe2++═Cr3++Fe3++
(4)处理废水时,最后Cr3+以Cr(OH)3形式除去,当c(Cr3+)=1×10-5molL﹣1 时,Cr3+沉淀完全,此时溶液的pH= . (已知,Ksp=6.4×10-31 , lg2=0.3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在试管A中先加入3 mL无水乙醇,然后边振荡试管边慢慢加入2 mL浓硫酸,最后加入2 mL冰醋酸,按下图装置进行实验,并将产生的蒸气经导管通到试管B中饱和碳酸钠溶液的液面上。请回答下列问题:

(1)浓硫酸的作用是__________________________________________。
(2)试管B中观察到的现象是_____________________________。
(3)若试管B中的饱和碳酸钠溶液用冷水代替,实验结束后不能闻到香味的可能原因是________________________________________________________________________。
(4)试管B中的饱和碳酸钠溶液的作用是__________________________________。
(5)通入蒸气的导管不能插入试管B中液面下的原因是_______________________________________。
(6)通入蒸气常选用长导管的目的是________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲制取较纯净的1,2-二氯乙烷,可采用的方法是( )
A. 乙烯和HCl加成 B. 乙烷和Cl2按1∶2的体积比在光照条件下反应
C. 乙烯和氯气加成 D. 乙烯先与HCl加成,再与等物质的量的氯气反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁铝榴石颜色深红,是宝石界中最常见的石榴子石,其化学成分为Fe2Al2( SiO4)3O铁铝榴石中所含元系不属于短周期元素的是
A.AlB.FeC.SiD.O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com