
�����±���Ϣ�������ж���ȷ����
�� | ���볣���������£� |
CH3COOH | Ki=1.8��10-5 |
H2CO3 | Ki1= 4.3��l0-7, Ki2= 5.6��10-11 |
H2S | Ki1= 9.1��10-8, Ki2= 1.1��10-12 |
A��0.10mol/L�����и���ҺpH��Na2S<Na2CO3
B��HCO3-+CH3COOH��H2O+CO2��+CH3COO-
C��������Һ������̼��������Һ��Ӧ
D��pH��ͬ��CH3COOH��H2CO3��H2S����ҺŨ�����μ�С
BC
��������
���������A�����볣��Խ������Խǿ������ݵ���ƽ�ⳣ����֪������̼�����ƴ������⻯�ƣ�����Խ�������Խ����ˮ�⣬��Һ�ļ���Խǿ����0.10mol/L�����и���ҺpH��Na2S��Na2CO3��A����B�����������ǿ��̼�ᣬ����ݽ�ǿ���Ʊ��������֪HCO3-+CH3COOH��H2O+CO2��+CH3COO-��B��ȷ��C��������̼�����ƴ������⻯�ƣ���������Һ������̼��������Һ��Ӧ�������⻯�ƺ�̼���ƣ�C��ȷ��D��������CH3COOH��H2CO3��H2S����pH��ͬ��CH3COOH��H2CO3��H2S����ҺŨ����������D����ѡBC��
���㣺�������ƽ�ⳣ����Ӧ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015�㶫ʡ�����и�һ��ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ������
��10�֣�ij�����Ĺ�ҵ��ˮ�к��д�����FeSO4���϶��Cu2+������Na+���ù����ƻ��ӷ�ˮ�л���FeSO4�ͽ���ͭ��������������ͼ���ش����⡣
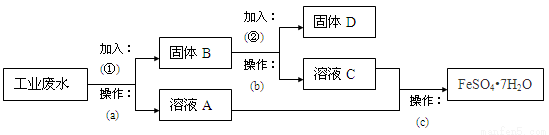
��1��a������Ҫ�õ��IJ��������� ��
��2��������Լ���Ϊ ��Ҫ�ж������Լ����Ƿ����������������� ��
��3�������Լ��ڷ�����Ӧ�����ӷ���ʽ�� ��
��4��c����Ϊ ����ȴ�ᾧ�� ��ϴ�ӡ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�����в�ƽ����һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���й���H2SO3��Һ��˵����ȷ����
A����ʹ���Ը��������Һ��ɫ����ΪH2SO3��Ư����
B��H2SO3�ڿ��������ױ��ʣ���ΪSO2
C����Һ�д��ڵ���ֻ��H+��SO32-
D������NaOH��Һ�������ֽⷴӦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�����в�ƽ����һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ʲ����ںϽ����
A��ˮ�� B����ͭ C������ D��̼�ظ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ϻ��л�����������ѧ����ĩ���в��Ի�ѧ�Ծ��������棩 ���ͣ��ƶ���
�����8�֣���֪̼̼˫�����Ա�������������Ӧ���£�

�����л��� 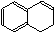 �ϳ�
�ϳ� ������ϳ�;�����£�
������ϳ�;�����£�

���������գ�
42.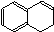 ������ͬϵ���ͨʽΪ ��A�Ľṹ��ʽ�� ��
������ͬϵ���ͨʽΪ ��A�Ľṹ��ʽ�� ��
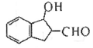 ��һ��ͬ���칹����һ�ַ����ᣬ�ҷ���ֻ����һ������д����������������һ��ͬ���칹��Ľṹ��ʽ ��
��һ��ͬ���칹����һ�ַ����ᣬ�ҷ���ֻ����һ������д����������������һ��ͬ���칹��Ľṹ��ʽ ��
43.��������Ӧ�ķ�Ӧ������ �� �� ��
44.д�����һ����Ӧ�ķ�Ӧ����ʽ_____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ϻ��л�����������ѧ����ĩ���в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��80mL 0.1mol?L-1ϡHNO3��Һ�м���ͭ�ۺ����ۻ���������ȫ�ܽ⣬�ڷ�Ӧ����Һ�еμ����軯����Һ����Һû�г���Ѫ��ɫ��ͭ�ۺ����ۻ���������������
A��0.168g B��0.184g C��0.192g D��0.200g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ϻ��л�����������ѧ����ĩ���в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
������ĽṹΪ �л�������������ȷ����
�л�������������ȷ����
A���䵥�岻�ܷ�����ȥ��Ӧ
B���䵥�����ͨ����Ӧ�γ���Ԫ��״������
C.�䵥�庬��
D�����������ɼӾ۷�Ӧ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�������и߸����ڶ����¿����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��NA�ǰ����ӵ���������ֵ������˵����ȷ����
A��0.1 mol�ǻ��к��еĵ�����Ϊ0.7 NA
B��28g Fe������ϡ���ᷴӦ��ת�Ƶĵ�����ΪNA
C����58.5g NaCl����1 Lˮ�У���Һ������Na+��Cl������Ϊ2NA
D��0.5 mol/L Al2(SO4)3��Һ�к���SO42 ������ĿΪ1.5 NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ϻ��о�����������ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪�����ԣ�Cl2> Fe3+ >I2����FeI2��Һ�м���һ��������ˮ���й����ӷ���ʽ�������
A��2 I��+ Cl2 ��I2 + 2Cl��
B��2Fe2+ + 2I��+ 2Cl2 �� 2Fe3+ + I2 + 4Cl��
C��2Fe2+ + 4I��+ 3Cl2 �� 2Fe3+ + 2I2 + 6Cl��
D��2Fe2+ + 6I��+ 4Cl2 �� 2Fe3+ + 3I2 + 8Cl��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com