
| A、天然蛋白质水解的最终产物是a-氨基酸 |
| B、CuSO4溶液会使蛋白质发生变性 |
| C、浓硝酸会使某些蛋白质变黄 |
| D、凡含有“-CO-NH-”的化合物均为蛋白质 |


 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,78 g Na2O2中含有的阴离子数是2NA |
| B、常温下,l L 0.l mol?L-1NH4NO3溶液中含有的NH4+数是0.l NA |
| C、常温常压下,22.4 L SO2和O2混合气体中含有的氧原子数是2 NA |
| D、铁铝混合物与一定量盐酸反应生成1 mol H2时,转移电子数是2 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:

| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、蚁醛的最简式:CH2O | ||
B、中子数为20的氯原子:
| ||
C、氮原子最外层电子轨道表示式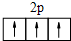 | ||
D、NH4Br的电子式 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、18g H2O和14g N2 |
| B、5.6L O2和11g CO2 |
| C、9g H2O和0.5mol CO |
| D、224mL H2(标准状况)和0.1mol N2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径呈周期性变化 |
| B、元素的化合价呈周期性变化 |
| C、第一电离能呈周期性变化 |
| D、元素原子的核外电子排布呈周期性变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、根据酸分子中含氢原子个数,将酸分为一元酸、二元酸等 |
| B、根据电解质在熔融状态下能否完全电离,将电解质分为强电解质和弱电解质 |
| C、根据元素原子最外层电子数的多少,将元素分为金属和非金属 |
| D、根据是否有离子参与反应,将反应分为离子反应和非离子反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com