
”¾ĢāÄæ”æĢśŹĒÖŲŅŖµÄ½šŹōŌŖĖŲ,ÓĆĶ¾¼«¹ć”£
£Ø1£©Ä³øߊ§¾»Ė®¼ĮæÉÓÉFe(OH)SO4¾ŪŗĻµĆµ½”£¹¤ŅµÉĻŅŌFeSO4”¢NaNO2ŗĶĻ”ĮņĖįĪŖŌĮĻĄ“ÖʱøFe(OH)SO4£¬·“Ó¦ÖŠÓŠNOÉś³É£¬»Æѧ·½³ĢŹ½ĪŖ__________”£
£Ø2£©ŅŃÖŖ£ŗ¢ŁFe2O3(s)+3C(ŹÆÄ«) = 2Fe(s)+3CO(g) ¦¤H1 = + 489.0 kJ/mol
¢ŚC(ŹÆÄ«)+CO2(g) = 2CO(g) ¦¤H2 = + 172.5 kJ/mol
øßĀÆĮ¶Ģś¹ż³ĢÖŠ·¢ÉśµÄÖ÷ŅŖ·“Ó¦ĪŖ£ŗ
1/3Fe2O3(s)+ CO(g) ![]() 2/3Fe(s)+CO2(g) ¦¤H = a kJ/mol£¬Ōņa =_____kJ/mol”£
2/3Fe(s)+CO2(g) ¦¤H = a kJ/mol£¬Ōņa =_____kJ/mol”£
ŅŃÖŖøĆ·“Ó¦ŌŚ²»Ķ¬ĪĀ¶ČĻĀµÄĘ½ŗā³£ŹżČēĻĀ±ķ£ŗ
ĪĀ¶Č/”ę | 1000 | 1115 | 1300 |
Ę½ŗā³£Źż | 4.0 | 3.7 | 3.5 |
ŌŚŅ»øöČŻ»żĪŖ10LµÄĆܱÕČŻĘ÷ÖŠ£¬1000”ꏱ¼ÓČėFe”¢Fe2O3”¢CO”¢CO2ø÷1.0 mol£¬“ĖŹ±vÕż ________vÄę(Ģī”°µČÓŚ”±”¢”°“óÓŚ”±»ņ”°Š”ÓŚ”±)”£¾¹żl0 min£¬ŌŚ1000”ę“ļµ½Ę½ŗā£¬ŌņøĆŹ±¼ä·¶Ī§ÄŚ·“Ó¦µÄĘ½¾ł·“Ó¦ĖŁĀŹv (CO2)= ______________”£ÓūĢįøßÉĻŹö·“Ó¦ÖŠCOµÄĘ½ŗā×Ŗ»ÆĀŹ£¬æɲÉČ”µÄ“ėŹ©ŹĒ______________£»
A.Ģįøß·“Ó¦ĪĀ¶Č B.ŅĘ³ö²æ·ÖCO2 C.¼ÓČėŗĻŹŹµÄ“߻ƼĮ D.¼õŠ”ČŻĘ÷µÄČŻ»ż
”¾“š°ø”æ2FeSO4£«2NaNO2£«H2SO4=2Fe(OH)SO4£«2NO£«Na2SO4£9.5“óÓŚ0.006mol/(L”¤min)B
”¾½āĪö”æ
£Ø1£©“Ė·“Ó¦ĪŖŃõ»Æ»¹Ō·“Ó¦£¬·“Ó¦ĪļÖŠ¼ČÓŠŃõ»Æ¼ĮÓÖÓŠ»¹Ō¼Į£¬ŅĄ¾Ż»ÆŗĻ¼ŪÉż½µĻąµČÅäĘ½¼“æÉ£»
£Ø2£©ŅĄ¾ŻČČ»Æѧ·½³ĢŹ½¼ĘĖć£¬·“Ó¦ģŹ±ä£»ŅĄ¾Ż¼ĘĖćµĆµ½ÅضČÉĢŗĶøĆĪĀ¶ČĻĀĘ½ŗā³£Źż±Č½ĻÅŠ¶Ļ·“Ó¦½ųŠŠ·½Ļņ£¬ŅĄ¾ŻĘ½ŗā³£Źż¼ĘĖćÉś³É¶žŃõ»ÆĢ¼£¬½įŗĻ·“Ó¦ĖŁĀŹøÅÄī¼ĘĖ涞Ńõ»ÆĢ¼µÄ»Æѧ·“Ó¦ĖŁĀŹ£»ÓūĢįøßÉĻŹö·“Ó¦ÖŠCOµÄĘ½ŗā×Ŗ»ÆĀŹ£¬ŠčŅŖ·“Ó¦ÕżĻņ½ųŠŠ£»
£Ø1£©FeSO4”śFe£ØOH£©SO4 £¬FeÓÉ+2±äĪŖ+3£¬¹ŹFeSO4ĪŖ»¹Ō¼Į£¬NaNO2”śNO£¬NÓÉ+3±äĪŖ+2£¬¹ŹNaNO2ĪŖŃõ»Æ¼Į£¬Ļ”ĮņĖį¼Č²»×öŃõ»Æ¼ĮŅ²²»×ö»¹Ō¼Į£®FeSO4”śFe£ØOH£©SO4 ŗĶNaNO2”śNO»ÆŗĻ¼ŪÉż½µĻąµČ£¬¹ŹFeSO4ŗĶNaNO2»Æѧ¼ĘĮæŹżĻąµČ£¬ŅĄ¾ŻŌ×ÓŹŲŗćÅäĘ½æÉµĆ£ŗ2FeSO4+2NaNO2+H2SO4=2Fe£ØOH£©SO4+Na2SO4+2NO”ü£»
£Ø2£©¢ŁFe2O3£Øs£©+3C£ØŹÆÄ«£©=2Fe£Øs£©+3CO£Øg£©”÷H1=+489.0kJ”¤mol£1
¢ŚC£ØŹÆÄ«£©+CO2£Øg£©=2CO£Øg£©”÷H2=+172.5kJ”¤mol£1
ŅĄ¾ŻøĒĖ¹¶ØĀÉ¢Ł”Į1/3-¢ŚµĆµ½øßĀÆĮ¶Ģś¹ż³ĢÖŠ·¢ÉśµÄÖ÷ŅŖ·“Ó¦ĪŖ£ŗ1/3Fe2O3£Øs£©+CO£Øg£©![]() 2/3 Fe£Øs£©+CO2£Øg£©”÷H=-9.5 kJ”¤mol£1£¬Ōņa=-9.5kJ”¤mol£1£»
2/3 Fe£Øs£©+CO2£Øg£©”÷H=-9.5 kJ”¤mol£1£¬Ōņa=-9.5kJ”¤mol£1£»
ŌŚŅ»øöČŻ»żĪŖ£ŗ10LµÄĆܱÕČŻĘ÷ÖŠ£¬1000”ꏱ¼ÓČėFe”¢Fe2O3”¢CO”¢CO2ø÷1.0mol£¬ÅضČÉĢQ=![]() =1£¼K=4£¬ĖµĆ÷·“Ó¦ÕżĻņ½ųŠŠ£¬vÕż£¾vÄę£»
=1£¼K=4£¬ĖµĆ÷·“Ó¦ÕżĻņ½ųŠŠ£¬vÕż£¾vÄę£»
Éč·“Ó¦Ņ»Ńõ»ÆĢ¼ĪļÖŹµÄĮæĪŖx
1/3Fe2O3£Øs£©+CO£Øg£©![]() 2/3 Fe£Øs£©+CO2£Øg£©
2/3 Fe£Øs£©+CO2£Øg£©
ĘšŹ¼Įæ £Ømol£© 1 1
±ä»ÆĮæ£Ømol£© x x
Ę½ŗāĮæ£Ømol£© 1-x 1+x
(1+x)/(1-x)=4
x=0.6
¾¹żl0min£¬ŌŚ1000”ę“ļµ½Ę½ŗā£¬ŌņøĆŹ±¼ä·¶Ī§ÄŚ·“Ó¦µÄĘ½¾ł·“Ó¦ĖŁĀŹv£ØCO2£©=![]() =0.006mol”¤L£1”¤min£1£»
=0.006mol”¤L£1”¤min£1£»
ÓūĢįøßÉĻŹö·“Ó¦ÖŠCOµÄĘ½ŗā×Ŗ»ÆĀŹ£¬Ó¦Ź¹Ę½ŗāÕżĻņ½ųŠŠ£»
A£®·“Ó¦ŹĒ·ÅČČ·“Ó¦£¬ÉżøßĪĀ¶Č£¬Ę½ŗāÄęĻņŅĘ¶Æ£¬Ņ»Ńõ»ÆĢ¼×Ŗ»ÆĀŹ¼õŠ”£¬¹ŹA²»·ūŗĻ£»
B£®ŅĘ³ö²æ·ÖCO2 Ę½ŗāÕżĻņŅĘ¶Æ£¬Ņ»Ńõ»ÆĢ¼×Ŗ»ÆĀŹŌö“󣬹ŹB·ūŗĻ£»
C£®¼ÓČėŗĻŹŹµÄ“߻ƼĮ£¬ÄÜøı䷓ӦĖŁĀŹ²»øıä»ÆŃ§Ę½ŗā£¬Ņ»Ńõ»ÆĢ¼×Ŗ»ÆĀŹ²»±ä£¬¹ŹC²»·ūŗĻ£»
D£®ÓÉÓŚ·“Ó¦Ē°ŗóĘųĢåĢå»ż²»±ä£¬¼õŠ”ČŻĘ÷µÄČŻ»żŌö“óŃ¹Ēæ£¬Ę½ŗā²»ŅĘ¶Æ£¬Ņ»Ńõ»ÆĢ¼×Ŗ»ÆĀŹ²»±ä£¬¹ŹD²»·ūŗĻ£»
¹ŹŃ”B£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ¹ĢĢå¼×ĪŖ·Ē½šŹō£¬I”¢F¾łĪŖ³£¼ūµÄ½šŹō£¬EĪŖĘųĢåµ„ÖŹ£»¹ĢĢåŅŅĪŖŅ»ÖÖŗģ×ŲÉ«¹ĢĢ壻GĪŖ°×É«½ŗד³Įµķ£¬¼ČÄÜČܽāÓŚŃĪĖį£¬ÓÖÄÜČܽāÓŚĒāŃõ»ÆÄĘČÜŅŗ£®AŌŚ³£ĪĀĻĀĪŖĘųĢ¬£¬ÓėŃõĘųĶźČ«·“Ó¦Ź±µÄĢå»ż±ČŹĒ![]() £®WŹĒÓÉČżÖÖ“¦ŌŚ²»Ķ¬¶ĢÖÜĘŚµÄŌŖĖŲ×é³ÉµÄ»ÆŗĻĪļ£¬ÓėĖ®·“Ӧɜ³ÉAŗĶGŹ±µÄ»Æѧ¼ĘĮæŹżÖ®±ČĪŖ
£®WŹĒÓÉČżÖÖ“¦ŌŚ²»Ķ¬¶ĢÖÜĘŚµÄŌŖĖŲ×é³ÉµÄ»ÆŗĻĪļ£¬ÓėĖ®·“Ӧɜ³ÉAŗĶGŹ±µÄ»Æѧ¼ĘĮæŹżÖ®±ČĪŖ![]() £®ø÷ĪļÖŹÓŠČēĻĀĶ¼ĖłŹ¾µÄ×Ŗ»Æ¹ŲĻµ£Ø²æ·Ö·“Ó¦µÄ²śĪļĪ“Č«²æ±ķŹ¾£©£®ŹŌ»Ų“šĻĀĮŠĢā£ŗ
£®ø÷ĪļÖŹÓŠČēĻĀĶ¼ĖłŹ¾µÄ×Ŗ»Æ¹ŲĻµ£Ø²æ·Ö·“Ó¦µÄ²śĪļĪ“Č«²æ±ķŹ¾£©£®ŹŌ»Ų“šĻĀĮŠĢā£ŗ

£Ø1£©BµÄµē×ÓŹ½ĪŖ______£¬¹ĢĢå¼×”¢ŅŅµÄ»ÆѧŹ½·Ö±šŹĒ______”¢______£»
£Ø2£©ÉĻŹö×Ŗ»ÆÖŠ£¬¢Ł![]() ¢Ś
¢Ś![]() ¢Ū
¢Ū![]() ¢Ü
¢Ü![]() ¢Ż
¢Ż![]() ¢Ž
¢Ž![]() ĘäÖŠŹōÓŚÖĆ»»·“Ó¦µÄŹĒ£ØĢīŠņŗÅ£©______£»
ĘäÖŠŹōÓŚÖĆ»»·“Ó¦µÄŹĒ£ØĢīŠņŗÅ£©______£»
£Ø3£©Š“³öWŗĶĖ®·“Ó¦µÄ»Æѧ·½³ĢŹ½______£¬![]() ŗĶ
ŗĶ![]() ČÜŅŗ·“Ó¦µÄĄė×Ó·½³ĢŹ½______£®
ČÜŅŗ·“Ó¦µÄĄė×Ó·½³ĢŹ½______£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĀČ»ÆĢśŹĒ³£¼ūµÄĖ®“¦Ąķ¼Į£¬¹¤ŅµÉĻÖʱøĪŽĖ®FeCl3µÄŅ»ÖÖ¹¤ŅÕČēĻĀ£ŗ
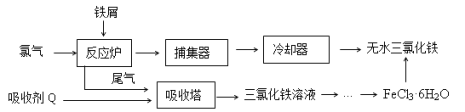
£Ø1£©ÓÉFeCl3”¤ 6H2O¾§ĢåÖʱøĪŽĖ®FeCl3Ó¦²ÉČ”µÄ“ėŹ©ŹĒ£ŗ ”£
£Ø2£©ĮłĖ®ŗĻĀČ»ÆĢśŌŚĖ®ÖŠµÄČܽā¶ČČēĻĀ£ŗ
ĪĀ¶Č/”ę | 0 | 10 | 20 | 30 | 50 | 80 | 100 |
Čܽā¶Č£Øg/100gH2O£© | 74.4 | 81.9 | 91.8 | 106.8 | 315.1 | 525.8 | 535.7 |
“ÓFeCl3ČÜŅŗÖʵĆFeCl3”¤6H2O¾§ĢåµÄ²Ł×÷²½ÖčŹĒ£ŗ¼ÓČėÉŁĮæŃĪĖį”¢ ”¢ ”¢¹żĀĖ”¢Ļ“µÓ”¢øÉŌļ”£
£Ø3£©³£ĪĀĻĀ£¬ČōČÜŅŗµÄpHæŲÖĘ²»µ±»įŹ¹Fe3+³Įµķ£¬pH£½4Ź±£¬ČÜŅŗÖŠc£ØFe3+£©£½ mol”¤L-1”££Ø³£ĪĀĻĀKsp[Fe£ØOH£©3]£½2.6”Į10-39£©”£
£Ø4£©FeCl3µÄÖŹĮæ·ÖŹżĶس£æÉÓƵāĮæ·Ø²ā¶Ø£ŗ³ĘČ”2.300gĪŽĖ®ĀČ»ÆĢśŃłĘ·£¬ČÜÓŚĻ”ŃĪĖį£¬ ŌŁ×ŖŅʵ½100mLČŻĮæĘ棬ÓĆÕōĮóĖ®¶ØČŻ£»Č”³ö10.00mL£¬¼ÓČėÉŌ¹żĮæµÄKIČÜŅŗ£¬³ä·Ö·“Ó¦ŗ󣬵ĪČėijŅ»ÖøŹ¾¼Į²¢ÓĆ0.1000mol”¤L-1Na2S2O3ČÜŅŗµĪ¶ØÓĆČ„12.50mL”£
ŅŃÖŖ£ŗI2£«2S2O32££½2I££«S4O62-
¢Ł Š“³ö¼ÓČėÉŌ¹żĮæµÄKIČÜŅŗ·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ ”£
¢Ś Ēóѳʷ֊ĀČ»ÆĢśµÄÖŹĮæ·ÖŹż£ØŠ“³ö¼ĘĖć¹ż³Ģ£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠŠšŹöÕżČ·µÄŹĒ
A. 24 g Ć¾Óė27 gĀĮÖŠ£¬ŗ¬ÓŠĻąĶ¬µÄÖŹ×ÓŹż
B. Ķ¬µČÖŹĮæµÄŃõĘųŗĶ³ōŃõÖŠ£¬µē×ÓŹżĻąĶ¬
C. 1 molÖŲĖ®Óė1 molĖ®ÖŠ£¬ÖŠ×ÓŹż±ČĪŖ2”Ć1
D. 1 molŅŅĶéŗĶ1 molŅŅĻ©ÖŠ£¬»Æѧ¼üŹżĻąĶ¬
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¹ŲÓŚ»Æѧ·“Ó¦ÖŠµÄÄÜĮæ±ä»Æ£¬ĻĀĮŠĖµ·ØÖŠ²»ÕżČ·µÄŹĒ( )
A. Č¼ÉÕ·“Ó¦¶¼ŹĒ·ÅČČ·“Ó¦
B. ¶ŌÓŚæÉÄę·“Ó¦£ŗaA(g)+bB(g)![]() bC(g)+dD(g)£¬Čē¹ūÕż·“Ó¦·ÅČČ£¬Äę·“Ó¦Ņ»¶ØĪüČČ
bC(g)+dD(g)£¬Čē¹ūÕż·“Ó¦·ÅČČ£¬Äę·“Ó¦Ņ»¶ØĪüČČ
C. ĒāĘųČ¼ÉÕÉś³ÉĖ®ŹĒŅ»øö·ÅČȵĻÆѧ·“Ó¦£¬ĖµĆ÷1 mol H2µÄÄÜĮæøßÓŚ1 mol H2OµÄÄÜĮæ
D. Ö»ÓŠ·ÅČȵÄŃõ»Æ»¹Ō·“Ó¦²ÅæÉŅŌÉč¼ĘĪŖŌµē³Ų
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æµ±ĪĀ¶ČøßÓŚ500 KŹ±£¬æĘѧ¼Ņ³É¹¦ĄūÓƶžŃõ»ÆĢ¼ŗĶĒāĘųŗĻ³ÉĮĖŅŅ“¼(æÉÄę·“Ó¦)£¬ÕāŌŚ½ŚÄܼõÅÅ”¢½µµĶĢ¼ÅÅ·Å·½Ćę¾ßÓŠÖŲ“óŅāŅ唣»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½______________________________________________”£
£Ø2£©ŌŚŗćČŻĆܱÕČŻĘ÷ÖŠ£¬ÅŠ¶ĻÉĻŹö·“Ó¦“ļµ½Ę½ŗāדĢ¬µÄŅĄ¾ŻŹĒ________”£
a£®ĢåĻµŃ¹Ēæ²»ŌŁøıä
b£®H2µÄÅØ¶Č²»ŌŁøıä
c£®ĘųĢåµÄĆÜ¶Č²»Ėꏱ¼äøıä
d£®µ„Ī»Ź±¼äÄŚĻūŗÄH2ŗĶCO2µÄĪļÖŹµÄĮæÖ®±ČĪŖ3:1
£Ø3£©ŌŚŅ»¶ØŃ¹ĒæĻĀ£¬²āµĆÓÉCO2ÖĘČ”CH3CH2OHµÄŹµŃ鏿¾ŻÖŠ£¬ĘšŹ¼Ķ¶ĮĻ±Č”¢ĪĀ¶ČÓėCO2µÄ×Ŗ»ÆĀŹµÄ¹ŲĻµČēĶ¼”£

øł¾ŻĶ¼ÖŠŹż¾Ż
¢Ł½µµĶĪĀ¶Č£¬Ę½ŗāĻņ________·½ĻņŅĘ¶Æ”£
¢ŚŌŚ700 K”¢ĘšŹ¼Ķ¶ĮĻ±Č![]() £½1.5Ź±£¬H2µÄ×Ŗ»ÆĀŹĪŖ________”£
£½1.5Ź±£¬H2µÄ×Ŗ»ÆĀŹĪŖ________”£
¢ŪŌŚ500 K”¢ĘšŹ¼Ķ¶ĮĻ±Č![]() £½2Ź±£¬“ļµ½Ę½ŗāŗóH2µÄÅضČĪŖa mol”¤L£1£¬Ōņ“ļµ½Ę½ŗāŹ±CH3CH2OHµÄÅضČĪŖ________”£
£½2Ź±£¬“ļµ½Ę½ŗāŗóH2µÄÅضČĪŖa mol”¤L£1£¬Ōņ“ļµ½Ę½ŗāŹ±CH3CH2OHµÄÅضČĪŖ________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ·“Ó¦![]() £Ø”÷H£¼0£©ŌŚµČČŻĢõ¼žĻĀ½ųŠŠ”£øıäĘäĖū·“Ó¦Ģõ¼ž£¬ŌŚ¢ń”¢¢ņ”¢¢ó½×¶ĪĢåĻµÖŠø÷ĪļÖŹÅضČĖꏱ¼ä±ä»ÆµÄĒśĻßČēĻĀĶ¼ĖłŹ¾£ŗ
£Ø”÷H£¼0£©ŌŚµČČŻĢõ¼žĻĀ½ųŠŠ”£øıäĘäĖū·“Ó¦Ģõ¼ž£¬ŌŚ¢ń”¢¢ņ”¢¢ó½×¶ĪĢåĻµÖŠø÷ĪļÖŹÅضČĖꏱ¼ä±ä»ÆµÄĒśĻßČēĻĀĶ¼ĖłŹ¾£ŗ

»Ų“šĪŹĢā£ŗ
¢Å·“Ó¦µÄ»Æѧ·½³ĢŹ½ÖŠa”Ćb”ĆcĪŖ£»
¢Ę£ĮµÄĘ½¾ł·“Ó¦ĖŁĀŹv¢ń£ØA£©”¢v¢ņ£ØA£©”¢v¢ó£ØA£©“ӓ󵽊”ÅÅĮŠ“ĪŠņĪŖ£»
¢Ē£ĀµÄĘ½ŗā×Ŗ»ÆĀŹ¦Į¢ń£ØB£©”¢¦Į¢ņ£ØB£©”¢¦Į¢ó£ØB£©ÖŠ×īŠ”µÄŹĒ£¬ĘäÖµŹĒ£»
¢ČÓɵŚŅ»“ĪĘ½ŗāµ½µŚ¶ž“ĪĘ½ŗā£¬Ę½ŗāŅĘ¶ÆµÄ·½ĻņŹĒ£¬²ÉČ”µÄ“ėŹ©ŹĒ£»
¢É±Č½ĻµŚ¢ņ½×¶Ī·“Ó¦ĪĀ¶Č£Ø£Ō£²£©ŗĶµŚ¢ó½×¶Ī·“Ó¦ĪĀ¶Č£Ø£Ō£³£©µÄøßµĶ£»£Ō£²£Ō£³£ØĢī”°£¼”±”°£¾”±”°£½”±£©ÅŠ¶ĻµÄĄķÓÉŹĒ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æµā»ÆŃĒĶ(Cu¢ń)ŹĒŃō¼«ÉäĻß¹Üø²øĒĪļ£¬²»ČÜÓŚĖ®ŗĶŅŅ“¼”£ĻĀĶ¼ŹĒ¹¤ŅµÉĻÓɱłĶÖĘČ”ĪŽĖ®µā»ÆŃĒĶµÄĮ÷³Ģ”£
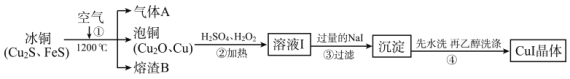
(1)FeSÖŠSµÄ»ÆŗĻ¼ŪĪŖ_____________”£
(2)²½Öč¢ŁÖŠCu2S±»×Ŗ»ÆĪŖCu£¬Ķ¬Ź±ÓŠ“óĘųĪŪČ¾ĪļAÉś³É£¬Ļą¹Ų»Æѧ·“Ó¦·½³ĢŹ½ĪŖ_____________£¬ČŪŌüBµÄÖ÷ŅŖ³É·ÖĪŖŗŚÉ«“ÅŠŌĪļÖŹ£¬Ęä»ÆѧŹ½ĪŖ_____________”£
(3)²½Öč¢ŚÖŠH2O2µÄ×÷ÓĆŹĒ_____________£»²½Öč¢ŪÖŠ¼ÓČė¹żĮæNaIÉę¼°µÄÖ÷ŅŖĄė×Ó·“Ó¦·½³ĢŹ½ĪŖ_____________”£
(4)²½Öč¢ÜÓĆŅŅ“¼Ļ“µÓµÄÓŵćŹĒ_____________£»¼ģŃé³ĮµķŹĒ·ńĻ“µÓøɾ»µÄ·½·ØŹĒ_____________”£
(5)ČÜŅŗIÖŠĶس£ŗ¬ÉŁĮæFe(¢ó)”£ŅŃÖŖøĆ¹¤ŅµĢõ¼žĻĀ£¬Fe(OH)3µÄKsp=1.0”Į10£38£¬¾Ż“Ė·ÖĪö³żČ„Fe(¢ó)(¼“c(Fe3+)”Ü1.0”Į10£5mol/L)Ó¦µ÷½ŚpH²»Š”ÓŚ_____________(Ė®µÄĄė×Ó»żŅŌ³£ĪĀ¼Ę)”£
(6)×¼Č·³ĘČ” m g CuIѳʷ£¬¼ÓČė×ćĮæµÄFe2(SO4)3ČÜŅŗ£¬·¢Éś·“Ó¦ĪŖ2Cu¢ń+4Fe3+===2Cu2++4Fe2++I2£¬“żŃłĘ·ĶźČ«·“Ó¦ŗó£¬ÓĆamol/LĖįŠŌKMnO4ČÜŅŗµĪ¶ØFe(¢ņ)£¬Ļūŗıź×¼ŅŗµÄĢå»żĘ½¾łÖµĪŖ¢„mL”£ŃłĘ·ÖŠCuIµÄÖŹĮæ·ÖŹżµÄ¼ĘĖć±ķ“ļŹ½ĪŖ_____________£»Čē¹ūµĪ¶ØĒ°£¬ĖįŹ½µĪ¶Ø¹ÜƻӊÓƱź×¼ŅŗČóĻ“£¬CuIµÄÖŹĮæ·ÖŹż_____________(Ģī”°Ę«µĶ”±”¢”°Ę«øß”±»ņ”°ĪŽÓ°Ļģ”±)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”潫µČĪļÖŹµÄĮæµÄX”¢YĘųĢå³äČėŅ»øöĆܱÕČŻĘ÷ÖŠ£¬ŌŚŅ»¶ØĢõ¼žĻĀ·¢ÉśČēĻĀ·“Ó¦²¢“ļµ½Ę½ŗā£ŗX(g)£«Y(g) ![]() 2Z(g)””¦¤H<0”£µ±øıäijøöĢõ¼ž²¢“ļµ½ŠĀĘ½ŗāŗó£¬ĻĀĮŠŠšŹöÕżČ·µÄŹĒ(””””)
2Z(g)””¦¤H<0”£µ±øıäijøöĢõ¼ž²¢“ļµ½ŠĀĘ½ŗāŗó£¬ĻĀĮŠŠšŹöÕżČ·µÄŹĒ(””””)
A. ÉżøßĪĀ¶Č£¬XµÄĢå»ż·ÖŹż¼õŠ”
B. Ōö“óŃ¹Ēæ(ĖõŠ”ČŻĘ÷Ģå»ż)£¬ZµÄÅØ¶Č²»±ä
C. ±£³ÖČŻĘ÷Ģå»ż²»±ä£¬³äČėŅ»¶ØĮæµÄ¶čŠŌĘųĢ壬YµÄÅØ¶Č²»±ä
D. ±£³ÖČŻĘ÷Ģå»ż²»±ä£¬³äČėŅ»¶ØĮæµÄZ£¬XµÄĢå»ż·ÖŹżŌö“ó
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com