
【题目】写出下列反应的化学方程式或离子方程式。
(1)H2O2将碱性工业废水中的CN-氧化为碳酸盐和氨气的离子方程式:____________。
(2)硫化氢具有还原性,可以和许多氧化剂反应。在硫酸溶液中,H2S和KMnO4反应生成S、MnSO4、K2SO4和 H2O,写出该反应的化学方程式:________。
(3)ClO2常用于水的净化,工业上可用Cl2氧化NaClO2溶液制取ClO2,写出该反应的离子方程式:__。
(4)FeCl3与KClO在强碱性条件下反应可生成K2FeO4和KCl,写出该反应的离子方程式:____。
(5)催化反硝化法中,H2能将![]() 还原为N2,反应进行一段时间后溶液呈碱性,写出该反应的离子方程式:________。
还原为N2,反应进行一段时间后溶液呈碱性,写出该反应的离子方程式:________。
【答案】H2O2+CN-+OH-= ![]() +NH3↑ 5H2S+2KMnO4+3H2SO4=5S↓+2MnSO4+K2SO4+8H2O Cl2+2
+NH3↑ 5H2S+2KMnO4+3H2SO4=5S↓+2MnSO4+K2SO4+8H2O Cl2+2![]() =2ClO2+2Cl- 2Fe3++3ClO-+10OH+=2
=2ClO2+2Cl- 2Fe3++3ClO-+10OH+=2![]() +3Cl-+5H2O 5H2+2
+3Cl-+5H2O 5H2+2![]() =N2+2OH-+4H2O
=N2+2OH-+4H2O
【解析】
(1)H2O2将碱性工业废水中的CNˉ氧化为碳酸盐和氨气,相应的离子方程式为:H2O2+CN-+OH-=CO32-+NH3↑;
(2)H2S和KMnO4反应生成S、MnSO4、K2SO4和H2O,结合原子守恒书写化学方程式,3H2SO4+5H2S+2KMnO4=5S↓+2MnSO4+K2SO4+8H2O;
(3)Cl2氧化NaClO2溶液制取ClO2,本身被还原为氯离子,1个氯气分子反应得到2个电子,因此离子方程式:Cl2+2![]() =2ClO2+2Cl- ;
=2ClO2+2Cl- ;
(4)FeCl3与KClO在强碱性条件下反应可制取K2FeO4,结合电子守恒、原子守恒和电荷守恒配平书写离子方程式:2Fe3++10OH-+3ClO-═2FeO42-+3Cl-+5H2O;
(5)催化反硝化法中,H2能将NO3-还原为N2,反应进行一段时间后溶液呈碱性,所以产生氢氧根离子,离子反应方程式为:2NO3-+5H2=N2+2OH-+4H2O。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】(1)2015年11月首架C919打飞机总装下线,标志着我国跻身飞机研制先进国家行列。
①机身蒙皮使用的是第三代铝锂合金材料。下列不属于铝锂合金性质的是___(填字母)。
a.密度大 b.硬度大 c.抗腐蚀
②飞机轮胎属于橡胶制品。下列材料可用来合成橡胶的是____(填字母)。
a.石英砂 b.石灰石 c.异戊二烯
③机体先进复合材料的使用率达12%。下列属于复合材料的是___(填字母)。
a.钛合金 b.玻璃钢 c.普通陶瓷
(2)秋葵是一种大众喜爱的食材,含有蛋白质、维生素A、维生素C、纤维素、阿拉伯果糖和丰富的铁、锌、钙等元素,其中:

①属于人体所需微量元素的是____。
②属于水溶性维生素的是____,属于糖类的有阿拉伯果糖、___。
③蛋白质在人体内最终的水解产物是_____。
(3)化学能帮助我们更好地认识生活、改善生活。
①家用铁锅未洗净晾干,放置一段时间后出现红褐色锈斑,其主要的原因是铁发生了____腐蚀。
②乘车禁止携带物品的部分标识如图所示。在浓硝酸、食盐、汽油、石膏四种物品中,不能携带上车的是_____。

③过氧乙酸(![]() )易分解为乙酸和氧气,其稀溶常用于餐具、器械的消毒。写出过氧乙酸分解的化学方程式______。某胃药的主要成分是AlbMgc(OH)mCO3,常用于治疗胃酸过多,写出其中与胃酸反应的化学方程式_______。
)易分解为乙酸和氧气,其稀溶常用于餐具、器械的消毒。写出过氧乙酸分解的化学方程式______。某胃药的主要成分是AlbMgc(OH)mCO3,常用于治疗胃酸过多,写出其中与胃酸反应的化学方程式_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验能达到预期目的是
编号 | 实验内容 | 实验目的 |
A | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体,溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
B | 室温下,用pH试纸测定浓度为0.1mol/LNaClO溶液和0.1mol/LCH3COONa溶液的pH | 比较HClO和CH3COOH的酸性强弱 |
C | 等体积pH=2的HX和HY两种酸分别与足量的铁反应,排水法收集气体,HX放出的氢气多且反应速率快 | 证明HX酸性比HY强 |
D | 向10mL 0.2mol/L NaOH溶液中滴2滴0.1mol/L MgCl2溶液,产生白色沉淀后,再滴加2滴0.1mol/L FeCl3溶液,又生成红褐色沉淀 | 证明在相同温度下Ksp: Mg(OH)2>Fe(OH)3 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题
(1)我国规定生活用水中镉排放的最大允许浓度为0.005 mg/L。处理含镉废水可采用化学沉淀法。试回答下列问题:
①磷酸镉(Cd3(PO4)2)沉淀溶解平衡常数的表达式Ksp=_____________________。
②在某含镉废水中加人Na2S,当S2-浓度达到7.9 × 10-8mol/L时,水体中Cd2+浓度为_____mol/L(已知:Ksp(CdS)=7.9 × 10-27,Cd的相对原子质量:112);此时是否符合水源标准?______(填“是”或“否”)。
(2)炼锌烟尘(主要成份为ZnO,含少量CuO和FeO)为原料,可以制取氯化锌和金属锌。制取氯化锌主要工艺如下:
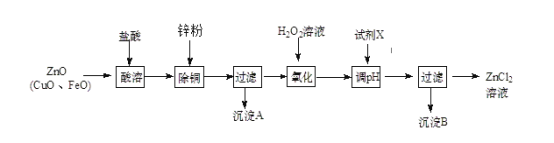
下表列出了相关金属离子生成氢氧化物沉淀的pH (开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算)。
金属离子 | Fe3+ | Zn2+ | Fe2+ |
开始沉淀的pH | 1. 1 | 5. 2 | 5. 8 |
沉淀完全的pH | 3. 2 | 6. 4 | 8. 8 |
①加入H2O2溶液的作用是________________。
②流程图中,调节pH时,加入的试剂X可以是________(填序号);
a、ZnO b、NaOH c、Zn2(OH)2CO3 d、ZnSO4
pH应调整到______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在含镍酸性废水中用电解法可以实现铁上镀镍并得到氯化钠,其装置如图所示,下列叙述错误的是

A. 待镀铁棒为阴极
B. 选用镍棒替换碳棒,镀镍效果更好
C. 通电后中间隔室的NaCl溶液浓度增大
D. 阳极的电极反应式为4OH- — 4e-=O2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂除去杂质,从而得到纯净的NaNO3晶体,相应的实验流程如图所示。

请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X____。
(2)上述实验流程中①②③步均要进行的实验操作是____(填操作名称)。
(3)上述实验流程中加入过量Na2CO3溶液的目的是____________。
(4)按此实验方案得到的溶液3中肯定含有杂质。为了解决这个问题,可以向溶液3中加入适量的________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四氯化锡(SnCl4)常用于染色的媒染剂等,工业上常用氯气与金属锡反应制备四氯化锡,某研究性学习小组在实验室用以下装置模拟四氯化锡的制备(夹持装置略)。

已知:①金属锡熔点为231℃,化学活泼性与铁相似。
②SnCl4为无色液体,熔点-33℃,沸点114℃,极易水解生成SnO2·xH2O,在潮湿的空气中发烟。
③SnCl2中的Sn2+易被氧化为Sn4+。
请回答下列问题:
(1)仪器F的名称是_______________,装置B中的试剂是_____________(填名称)。
(2)实验前应先点燃_________(填“A”或“E”)处的酒精灯,待__________(填实验现象)后,再点燃另外一处的酒精灯。
(3)若没有装置C(其他均相同),则D中发生的主要副反应的化学方程式为__________。
(4)该实验装置存在设计缺陷,你的改进措施为______________________________。
(5)该小组通过下列方法测定所用锡粉的纯度(杂质不参与反应):取0.7500g锡粉溶于足量稀盐酸中,向生成的SnCl2溶液中加入过量的FeCl3溶液,用物质的量浓度为0.1000molL-1 K2Cr2O7标准溶液滴定生成的Fe2+(已知酸性环境下Cr2O72-可被还原为Cr3+),共用去K2Cr2O7溶液的体积为20.00mL。
①锡粒中锡的质量分数_____。
②若溶解锡粉的过程生成的SnCl2溶液中含有Sn![]() ,则测定结果将__________(填“偏高”、“偏低”或“无影响”)
,则测定结果将__________(填“偏高”、“偏低”或“无影响”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,将33.6LHCl气体溶于50mL水再配成500mL溶液,求:
(1)所得盐酸的物质的量浓度为___________________。
(2)若将此溶液再加水稀释至1.5L,则稀释后盐酸的物质的量浓度为__________。
(3)将(2)的溶液取出1L与足量的石灰石反应,产生的CO2在标准状况下的体积为___________?(此问写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过测定反应过程中所放出的热量可计算中和热。50mL 0.50mol/L盐酸与50mL 0.55mol/LNaOH溶液在图示的装置中进行中和反应.回答下列问题:
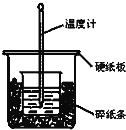
(1)从实验装置上看,图中尚缺少的一种玻璃仪器是___________.
(2)大烧杯上如果不盖硬纸板,求得的中和热数值__________(填“偏大”,“偏小”或“无影响”).
(3)实验中改用60mL 0.50mol/L盐酸跟50mL 0.55mol/LNaOH溶液进行反应,与上述实验相比,所求中和热________(填“相等”“不相等”),简述理由:______________________.
(4)若两溶液的密度都是1g/mL,中和后所得溶液的比热容c=4.18J/(g·℃),三次平行操作测得终止温度与起始温度差(t2﹣t1)分别为:①3.2℃ ②2.2℃ ③3.0℃,写出表示盐酸与NaOH溶液反应的中和热的热化学方程式________________________.(小数点后保留一位小数)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com