

 £»·“Ó¦¢Ū
£»·“Ó¦¢Ū £®
£®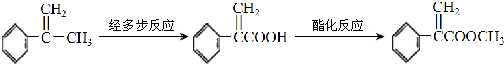
·ÖĪö AĪŖ·¼ĻćĢž£¬½įŗĻBµÄ·Ö×ÓŹ½æÉÖŖ£¬AĪŖ±½ŅŅĻ©»ņŅŅ±½”¢¶ž¼×±½£¬AµÄŗĖ“Ź²ÕńĒāĘ×ÖŠ³öĻÖ5øö·å£¬ĘäĆ껿±ČĪŖ1£ŗ1£ŗ2£ŗ2£ŗ2£¬ŌņAĪŖ £¬Óėäå»ÆĒā·¢Éś¼Ó³É·“Ӧɜ³ÉB£¬B·¢ÉśĀ±“śĢžµÄĖ®½ā·“Ӧɜ³ÉC£¬CæÉŅŌĮ¬Šų·¢ÉśŃõ»Æ·“Ó¦£¬ŌņBĪŖ
£¬Óėäå»ÆĒā·¢Éś¼Ó³É·“Ӧɜ³ÉB£¬B·¢ÉśĀ±“śĢžµÄĖ®½ā·“Ӧɜ³ÉC£¬CæÉŅŌĮ¬Šų·¢ÉśŃõ»Æ·“Ó¦£¬ŌņBĪŖ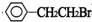 £¬CĪŖ
£¬CĪŖ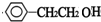 £¬DĪŖ
£¬DĪŖ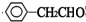 £¬EĪŖ
£¬EĪŖ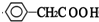 £®±½ŅŅĖįÓėŅŅ“¼·¢ÉśČ”“ś·“Ӧɜ³ÉFĪŖ
£®±½ŅŅĖįÓėŅŅ“¼·¢ÉśČ”“ś·“Ӧɜ³ÉFĪŖ £¬FÓė¼×Ėį¼×õ„·¢ÉśČ”“ś·“Ӧɜ³É
£¬FÓė¼×Ėį¼×õ„·¢ÉśČ”“ś·“Ӧɜ³É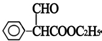 £¬
£¬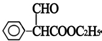 ÓėĒāĘų·¢Éś¼Ó³É·“Ӧɜ³ÉGĪŖ
ÓėĒāĘų·¢Éś¼Ó³É·“Ӧɜ³ÉGĪŖ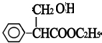 £¬GŌŁ·¢ÉśĻūČ„·“Ó¦µĆ°¢ĶŠĖįŅŅõ„£®
£¬GŌŁ·¢ÉśĻūČ„·“Ó¦µĆ°¢ĶŠĖįŅŅõ„£®
½ā“š ½ā£ŗAĪŖ·¼ĻćĢž£¬½įŗĻBµÄ·Ö×ÓŹ½æÉÖŖ£¬AĪŖ±½ŅŅĻ©»ņŅŅ±½”¢¶ž¼×±½£¬AµÄŗĖ“Ź²ÕńĒāĘ×ÖŠ³öĻÖ5øö·å£¬ĘäĆ껿±ČĪŖ1£ŗ1£ŗ2£ŗ2£ŗ2£¬ŌņAĪŖ £¬Óėäå»ÆĒā·¢Éś¼Ó³É·“Ӧɜ³ÉB£¬B·¢ÉśĀ±“śĢžµÄĖ®½ā·“Ӧɜ³ÉC£¬CæÉŅŌĮ¬Šų·¢ÉśŃõ»Æ·“Ó¦£¬ŌņBĪŖ
£¬Óėäå»ÆĒā·¢Éś¼Ó³É·“Ӧɜ³ÉB£¬B·¢ÉśĀ±“śĢžµÄĖ®½ā·“Ӧɜ³ÉC£¬CæÉŅŌĮ¬Šų·¢ÉśŃõ»Æ·“Ó¦£¬ŌņBĪŖ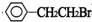 £¬CĪŖ
£¬CĪŖ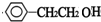 £¬DĪŖ
£¬DĪŖ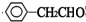 £¬EĪŖ
£¬EĪŖ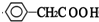 £®±½ŅŅĖįÓėŅŅ“¼·¢ÉśČ”“ś·“Ӧɜ³ÉFĪŖ
£®±½ŅŅĖįÓėŅŅ“¼·¢ÉśČ”“ś·“Ӧɜ³ÉFĪŖ £¬FÓė¼×Ėį¼×õ„·¢ÉśČ”“ś·“Ӧɜ³É
£¬FÓė¼×Ėį¼×õ„·¢ÉśČ”“ś·“Ӧɜ³É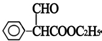 £¬
£¬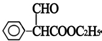 ÓėĒāĘų·¢Éś¼Ó³É·“Ӧɜ³ÉGĪŖ
ÓėĒāĘų·¢Éś¼Ó³É·“Ӧɜ³ÉGĪŖ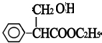 £¬GŌŁ·¢ÉśĻūČ„·“Ó¦µĆ°¢ĶŠĖįŅŅõ„£®
£¬GŌŁ·¢ÉśĻūČ„·“Ó¦µĆ°¢ĶŠĖįŅŅõ„£®
£Ø1£©ÓÉÉĻŹö·ÖĪöæÉÖŖ£¬AĪŖ £¬Ćū³ĘĪŖ±½ŅŅĻ©£¬BĪŖ
£¬Ćū³ĘĪŖ±½ŅŅĻ©£¬BĪŖ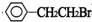 £¬ŗ¬ÓŠµÄ¹ŁÄÜĶÅĪŖäåŌ×Ó£¬¼ģŃéäåŌ×Ó·½·ØĪŖ£ŗ½«Ā±“śĢžŌŚNaOHĖ®ČÜŅŗ”¢¼ÓČČĢõ¼žĖ®½āµĆµ½NaBr£¬ŌŁÓĆĻ”ĻõĖįĖį»Æ£¬×īŗó¼ÓČėĻõĖįŅųČÜŅŗ£¬ÓŠµ»ĘÉ«³ĮµķÉś³É£¬
£¬ŗ¬ÓŠµÄ¹ŁÄÜĶÅĪŖäåŌ×Ó£¬¼ģŃéäåŌ×Ó·½·ØĪŖ£ŗ½«Ā±“śĢžŌŚNaOHĖ®ČÜŅŗ”¢¼ÓČČĢõ¼žĖ®½āµĆµ½NaBr£¬ŌŁÓĆĻ”ĻõĖįĖį»Æ£¬×īŗó¼ÓČėĻõĖįŅųČÜŅŗ£¬ÓŠµ»ĘÉ«³ĮµķÉś³É£¬
¹Ź“š°øĪŖ£ŗ±½ŅŅĻ©£»NaOHĖ®ČÜŅŗ”¢Ļ”HNO3”¢AgNO3ČÜŅŗ£»
£Ø2£©·“Ó¦¢ŚµÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ £»·“Ó¦¢ŪµÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ
£»·“Ó¦¢ŪµÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ £¬
£¬
¹Ź“š°øĪŖ£ŗ £»
£» £»
£»
£Ø3£©ÓÉ°¢ĶŠĖį¼×õ„µÄ½į¹¹æÉÖŖ£¬Ėłŗ¬¹ŁÄÜĶÅÓŠ£ŗõ„»ł”¢Ģ¼Ģ¼Ė«¼ü£»°¢ĶŠĖį¼×õ„ÓŠ¶ąÖÖĶ¬·ÖŅģ¹¹Ģ壬ĘäÖŠ±½»·ÉĻÖ»ÓŠŅ»øöÖ§Į“£¬ÄÜÓėNaHCO3ČÜŅŗ·“Ó¦£¬ŗ¬ÓŠ-COOH£¬ÓÖÄÜŹ¹äåµÄĖÄĀČ»ÆĢ¼ČÜŅŗĶŹÉ«£¬ŗ¬ÓŠĢ¼Ģ¼Ė«¼ü£¬æÉŅŌ±½»·Č”“śĻ©ĖįĢž»łÖŠHŌ×ӵƵ½£¬Ļ©ĖįÓŠ£ŗCH2=CHCH2COOH£¬CH3CH=CHCOOH£¬CH2=C£ØCH3£©COOH£¬Ģž»ł·Ö±šÓŠ3”¢3”¢2ÖÖHŌ×Ó£¬¹Ź·ūŗĻĢõ¼žµÄĶ¬·ÖŅģ¹¹Ģå¹²ÓŠ8ÖÖ£¬
¹Ź“š°øĪŖ£ŗõ„»ł”¢Ģ¼Ģ¼Ė«¼ü£»8£»
£Ø4£© Óėäå·¢Éś¼Ó³É·“Ó¦µĆµ½
Óėäå·¢Éś¼Ó³É·“Ó¦µĆµ½ £¬ŌŚŌŚĒāŃõ»ÆÄĘĖ®ČÜŅŗ”¢¼ÓČČĢõ¼žĻĀ·¢ÉśĖ®½ā·“Ó¦µĆµ½
£¬ŌŚŌŚĒāŃõ»ÆÄĘĖ®ČÜŅŗ”¢¼ÓČČĢõ¼žĻĀ·¢ÉśĖ®½ā·“Ó¦µĆµ½ £¬ŌŁ·¢ÉśŃõ»Æ·“Ó¦µĆµ½
£¬ŌŁ·¢ÉśŃõ»Æ·“Ó¦µĆµ½ £¬×īŗó·¢ÉśĻūČ„·“Ó¦µĆµ½
£¬×īŗó·¢ÉśĻūČ„·“Ó¦µĆµ½ £¬
£¬
¹Ź“š°øĪŖ£ŗCADB£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĪļĶʶĻ£¬¹Ų¼üŹĒÅŠ¶ĻAµÄ½į¹¹£¬ŌŁ½įŗĻ·“Ó¦Ģõ¼ž½ųŠŠĶʶĻ£¬ŠčŅŖѧɜŹģĮ·ÕĘĪÕ¹ŁÄÜĶŵĊŌÖŹÓė×Ŗ»Æ£¬·“Ó¦¢Ś·½³ĢŹ½ŹéŠ“ĪŖŅדķµć£¬Ń§ÉśČŻŅ×ČĻĪŖÓėŃõĘų·“Ó¦£¬£Ø3£©ÖŠ×¢ŅāĄūÓĆČ”“ś·ØÅŠ¶ĻĶ¬·ÖŅģ¹¹ĢåŹżÄ棬ÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
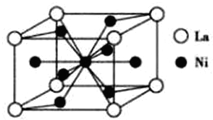 Ē°36ŗÅŌŖĖŲA”¢B”¢C”¢DµÄŗĖµēŗÉŹżŅĄ“ĪŌö“ó£®µŚ¶žÖÜĘŚŌŖĖŲAŌ×ÓµÄŗĖĶā³É¶Ōµē×ÓŹżŹĒĪ“³É¶Ōµē×ÓŹżµÄ2±¶£¬BŌ×ÓµÄ×īĶā²ćp¹ģµĄµÄµē×ÓĪŖ°ė³äĀś½į¹¹£¬C×īĶā²ćµē×ÓŹżŹĒµē×Ó²ćŹżµÄČż±¶£®DŹĒµŚĖÄÖÜĘŚŌŖĖŲ£¬ĘäŌ×ÓŗĖĶā×īĶā²ćµē×ÓŹżÓėĒāŌ×ÓĻąĶ¬£¬ĘäÓąø÷²ćµē×Ó¾łČ«³äĀś£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
Ē°36ŗÅŌŖĖŲA”¢B”¢C”¢DµÄŗĖµēŗÉŹżŅĄ“ĪŌö“ó£®µŚ¶žÖÜĘŚŌŖĖŲAŌ×ÓµÄŗĖĶā³É¶Ōµē×ÓŹżŹĒĪ“³É¶Ōµē×ÓŹżµÄ2±¶£¬BŌ×ÓµÄ×īĶā²ćp¹ģµĄµÄµē×ÓĪŖ°ė³äĀś½į¹¹£¬C×īĶā²ćµē×ÓŹżŹĒµē×Ó²ćŹżµÄČż±¶£®DŹĒµŚĖÄÖÜĘŚŌŖĖŲ£¬ĘäŌ×ÓŗĖĶā×īĶā²ćµē×ÓŹżÓėĒāŌ×ÓĻąĶ¬£¬ĘäÓąø÷²ćµē×Ó¾łČ«³äĀś£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | øÖŹĒÓĆĮæ×ī“ó£¬ÓĆĶ¾×ī¹ćµÄŗĻ½š | |
| B£® | ±½·ÓÕ“µ½Ę¤·ōÉĻ£¬Ó¦Į¢¼“ÓĆ“óĮæµÄČČĖ®³åĻ“ | |
| C£® | ĄūÓĆøß“æµ„ÖŹ¹č£¬æÉŅŌÖĘ³É¹āµē³Ų | |
| D£® | ŗ¬ĀČ£¬äåµÄ·ś“śĶéæɶŌ³ōŃõ²ć²śÉśĘĘ»µ×÷ÓĆ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ŃŠ¾æNOx”¢SO2”¢COµČ“óĘųĪŪČ¾ĘųĢåµÄ“¦Ąķ¾ßÓŠÖŲŅŖŅāŅ壮
ŃŠ¾æNOx”¢SO2”¢COµČ“óĘųĪŪČ¾ĘųĢåµÄ“¦Ąķ¾ßÓŠÖŲŅŖŅāŅ壮²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ń”Ļī | ŹµŃéŹĀŹµ | ½įĀŪ |
| A | ½«¶žŃõ»ÆĮņĶØČėäåĖ®ÖŠ£¬äåĖ®ĶŹÉ« | ¶žŃõ»ÆĮņÓŠĘư׊Ō |
| B | ½«”°84”±Ļū¶¾Ņŗ£Øŗ¬NaClO£©µĪČėĘ·ŗģČÜŅŗÖŠ£¬ĶŹÉ«»ŗĀż£¬ČōĶ¬Ź±¼ÓČėŹ³“×£¬ŗģÉ«ŗÜæģĶŹĪŖĪŽÉ« | ĖęČÜŅŗpH¼õŠ”£¬”°84”±Ļū¶¾ŅŗŃõ»ÆÄÜĮ¦ŌöĒæ |
| C | Ķ·ÅČėĻ”ĮņĖįÖŠ£¬ĪŽĆ÷ĻŌĻÖĻó£¬ŌŁ¼ÓČėĻõĖįÄĘ¹ĢĢ壬ČÜŅŗ±äĄ¶£¬ÓŠĆ÷ĻŌĘųÅŻ·Å³ö£¬ĶČܽā | ĻõĖįÄĘæÉŅŌ¼ÓæģĶÓėĻ”ĮņĖį·“Ó¦ĖŁĀŹ |
| D | µķ·ŪÓėĻ”ĮņĖį¹²ČČ£¬ŌŁ¼ÓŅų°±ČÜŅŗĖ®Ō”¼ÓČČ£¬ĪŽŅų¾µÉś³É | µķ·ŪƻӊĖ®½ā |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ³£ĪĀĻĀpH=5µÄŃĪĖįČÜŅŗĻ”ŹĶ103±¶ŗó£¬pHµČÓŚ8 | |
| B£® | ÅØ¶Č¾łĪŖ0.1mol/LµÄ°±Ė®ŗĶĀČ»Æļ§ČÜŅŗ£¬Ė®µēĄė³öµÄc£ØH+£©Ē°Õߊ”ÓŚŗóÕß | |
| C£® | Na2CO3ČÜŅŗÖŠ“ęŌŚ£ŗ2c£ØNa+£©=c£ØCO32-£©+c£ØHCO3-£©+c£ØH2CO3£© | |
| D£® | ³£ĪĀĻĀ£¬pH=2µÄCH3COOHČÜŅŗÓėpH=12µÄKOHČÜŅŗµČĢå»ż»ģŗĻ£ŗc£ØK+£©+c£ØH+£©=c£ØOH-£©+c£ØCH3COO-£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  ČēĶ¼µÄ¼üĻߏ½±ķŹ¾ĢžµÄĆū³ĘĪŖ£ŗ3-¼×»ł-4-ŅŅ»ł-7-¼×»łŠĮĶé | |
| B£® | ·ūŗĻ·Ö×ÓŹ½ĪŖC3H8OµÄ“¼ÓŠČżÖÖ²»Ķ¬µÄ½į¹¹ | |
| C£® | ŅŅĻ©ŌŚŅ»¶ØĢõ¼žĻĀÄÜ·¢Éś¼Ó³É·“Ó¦£¬¼Ó¾Ū·“Ó¦£¬±»Ėį»ÆøßĆĢĖį¼ŲČÜŅŗŃõ»Æ£¬Ņ²ÄÜŌŚŅ»¶ØĢõ¼žĻĀ±»ŃõĘųŃõ»Æ³ÉŅŅĖį | |
| D£® |  ÖĪĮĘű¼²µÄĒąŻļĖŲ£ØČēĶ¼£©£¬·Ö×ÓŹ½ŹĒC15H20O5 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ”÷H1£¾0 | B£® | ”÷H2£¾0 | C£® | ”÷H2£¼”÷H3 | D£® | ”÷H5=2”÷H4+”÷H1 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com