
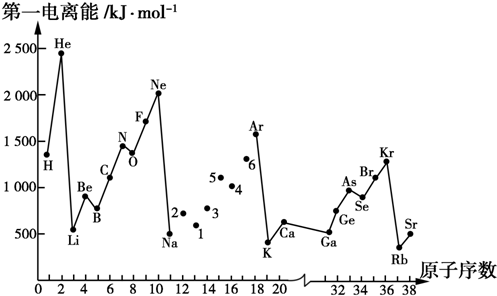
分析 (1)同一周期元素中,元素的第一电离能随着原子序数的增大而呈增大的趋势,但第ⅡA元素第一电离能大于第ⅢA元素,第ⅤA族的第一电离能大于第ⅥA族元素;
(2)同一主族元素原子的第一电离能I1,从上到下依次减小;
(3)5元素为15号元素氮,在周期表中氮的位置为第三周期,第ⅤA族;
(4)根据第一电离能,同周期从左向右整体呈增大趋势,但第ⅡA>ⅢA,ⅤA>ⅥA特殊,所以图中4、5、6号三种元素分别为S、P、Cl,据此书写氢化物;
(5)根据1~6号元素中,6号为Cl为非金属性最强,所以最高价氧化物对应水化物中酸性最强,呈两性的元素为Al,据此解答.
解答 解:(1)根据图片知,同一周期元素中,元素的第一电离能随着原子序数的增大而呈增大的趋势,但第ⅡA元素第一电离能大于第ⅢA元素,第ⅤA族的第一电离能大于第ⅥA族元素,所以Na~Ar之间的元素用短线连接起来的图象为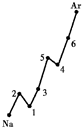 ;故答案为:
;故答案为: ;
;
(2)同一主族元素原子的第一电离能I1,如上图以第ⅠA族为例,变化规律从上到下依次减小,其他族一致;故答案为:从上到下依次减小;
(3)5号元素为15号元素氮,在周期表中的位置为第三周期,第ⅤA族;故答案为:第三周期,ⅤA族;
(4)根据第一电离能,同周期从左向右整体呈增大趋势,但第ⅡA>ⅢA,ⅤA>ⅥA特殊,所以图中4、5、6号三种元素分别为S、P、Cl,则对应的氢化物分别为:H2S、PH3、HCl,故答案为:H2S、PH3、HCl;
(5)根据1~6号元素中,6号为Cl为非金属性最强,所以最高价氧化物对应水化物HClO4酸性最强,呈两性的元素为Al,则两性化合物有Al2O3、Al(OH)3,故答案为:HClO4;Al2O3、Al(OH)3.
点评 本题考查了第一电离能的变化趋势,难度不大,注意“同一周期元素中,元素第一电离能的变化趋势,及异常现象”,为易错点.


科目:高中化学 来源: 题型:解答题
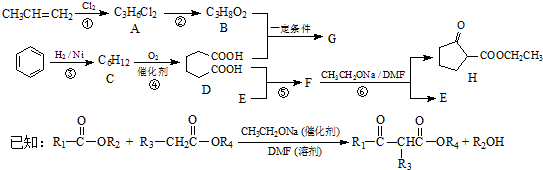
 .
.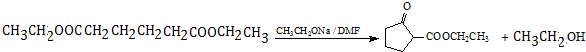 .
.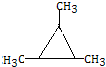 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3C(CH3)2OH | B. | CH3CHOHCH(CH3)CH3 | ||
| C. | CH3CH2CH2CHOHCH3 | D. | CH3CH2CHOHCH2CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
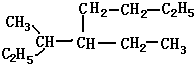 名称:3-甲基-4-乙基-辛烷
名称:3-甲基-4-乙基-辛烷查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg、Al、B | B. | N、O、S | C. | Li、Be、Mg | D. | B、F、Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某钠盐溶液含甲电离出的阴离子,则该溶液只能与酸反应 | |
| B. | 丁和甲中各元素质量比相同,则丁中一定含有-l价的元素 | |
| C. | 丙中含有第二周期ⅣA族的元素,则丙一定是只含C、H的化合物 | |
| D. | 乙与氧气的摩尔质量相同,则乙一定含有极性键和非极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 6种 | B. | 5种 | C. | 4种 | D. | 2种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2A在水溶液中的电离方程式为:H2A?2H++A2- | |
| B. | 0.1mol.L-1的H2A溶液pH<2 | |
| C. | 体积相等pH=1的盐酸与H2A溶液分别与足量的Zn反应,H2A溶液产生的H2多 | |
| D. | (NH4)2 A溶液中存在离子浓度关系:c(A2- )>C(NH4+ )>C(H+ )>C(OH- ) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com