
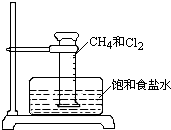
 某课外活动小组利用如图所示装置探究甲烷于氯气的反应.根据题意,回答下列问题:
某课外活动小组利用如图所示装置探究甲烷于氯气的反应.根据题意,回答下列问题:分析 ①甲烷为饱和烷烃,在光照条件下能够与氯气发生取代反应,若用日光直射,可能会引起爆炸;甲烷与氯气发生一氯取代反应生成一氯甲烷和氯化氢;
②甲烷发生取代反应生成氯化氢,氯气消耗所以量筒内颜色变浅,气体减少所以压强减小,量筒内的压强减小,量筒内液面上升.因生成的HCl易溶于水,溶液中Cl-浓度增大,使氯化钠的溶解平衡逆向移动,反应生成CH2Cl2、CHCl3、CCl4常温下是无色油液体;
③氯气在饱和食盐水中的溶解度降低;
④取代反应是指有机化合物分子中任何一个原子或基团被试剂中同类型的其它原子或基团所取代的反应;依据反应2CHCl3+O2→2COCl2+2HCl,生成的产物氯化氢的性质解答.
解答 解:①CH4和Cl2在光照(或光亮处)条件下发生反应,若用日光直射,反应非常剧烈,可能会引起爆炸,甲烷与氯气反应生成一氯甲烷的方程式为:CH4+Cl2$\stackrel{光}{→}$CH3Cl+HCl,
故答案为:光照(或光亮处);爆炸;CH4+Cl2$\stackrel{光}{→}$CH3Cl+HCl;
②甲烷发生取代反应生成氯化氢,氯气消耗所以量筒内颜色变浅,气体减少所以压强减小,量筒内的压强减小,量筒内液面上升.因生成的HCl易溶于水,溶液中Cl-浓度增大,使氯化钠的溶解平衡逆向移动,反应生成CH2Cl2、CHCl3、CCl4常温下是无色油液体,所以看到的现象有:量筒内壁出现油状液滴,饱和食盐水中有少量固体析出,量筒内黄绿色气体颜色变浅;量筒内液面上升;
故答案为:量筒内黄绿色气体颜色变浅 量筒内液面上升;
③氯气和水反应生成盐酸和次氯酸,饱和食盐水电离出氯离子,氯气在饱和食盐水中的溶解度降低,所以用饱和食盐水而不用水的原因是降低Cl2在水中溶解度,抑制Cl2和水的反应,
故答案为:降低Cl2在水中溶解度,抑制Cl2和水的反应;
④反应前碳与氢原子和三个氯原子都是以单的键相连,反应之后碳氧之间是双键,不符合取代反应的特点,不所以取代反应;
氯仿如果变质则发生反应2CHCl3+O2→2COCl2+2HCl,生成的氯化氢溶于水,电离产生氢离子和氯离子,所以能够使湿润的蓝色石蕊试纸变红色,加入硝酸银溶液会发生反应生成白色的氯化银沉淀,
故选:B;BE.
点评 本题考查了探究甲烷于氯气的反应的实验,熟悉甲烷的结构、性质是解题关键,注意④为易错选项,抓住物质的性质是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | HClO4、KClO3 | B. | KClO、KCl | C. | NaClO、KCl | D. | NaCl、KCl |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 金属性逐渐增强 | B. | 原子半径逐渐增大 | ||
| C. | 最高正价数值逐渐增大 | D. | 从硅到氯负价从-4-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用渗析法分离Fe(OH)3胶体和FeCl3溶液的混合物 | |
| B. | 用重结晶法提纯NaCl和KNO3的混合物中的KNO3 | |
| C. | 用蒸馏法分离乙醇和甲醇的混合物 | |
| D. | 用分液的方法分离甘油和水的混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 表示的分子式C6H14;名称是2-甲基戊烷.
表示的分子式C6H14;名称是2-甲基戊烷. 中含有的官能团的名称为羟基、酯基.
中含有的官能团的名称为羟基、酯基.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 编号 | 化学反应 | 离子方程式 | 评价 |
| A | 过氧化钠与水反应 | 2O22-+2H2O═4OH-+O2↑ | 正确 |
| B | 漂白粉溶液中通入过量SO2 | ClO-+H2O+SO2═ HSO3-+HClO | 正确 |
| C | Fe3O4溶于盐酸 | Fe3O4+8H+═2Fe3++Fe2++4H2O | 错误,应只生成Fe3+ |
| D | 碳酸氢钙溶液中加入过量的氢氧化钠溶液 | Ca2++HCO3-+OH- ═CaCO3↓+H2O | 错误,产物及配平不对 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com