
| A. | 3.0g由葡萄糖和冰醋酸组成的混合物中含有的原子总数为0.3NA | |
| B. | 氢气与氯气反应生成标准状况下22.4L氯化氢,断裂化学键的总数为2NA | |
| C. | 1mol的白磷(P4)或四氯化碳(CCl4)中所含的共价健数均为4NA | |
| D. | 工业上电解饱和氯化钠溶液,得到标准状况下22.4L氢气时,转移的电子数为2NA |
分析 A.葡萄糖和冰醋酸最简式相同为CH2O,只需要计算3.0gCH2O的物质的量计算原子数;
B.当反应生成2molHCl时,断裂2mol化学键;
C.1个白磷分子含有6个P-P键,1个四氯化碳分子含有4个C-Cl键;
D.依据电解氯化钠过程和氧化还原反应电子守恒计算得到.
解答 解:A.葡萄糖和冰醋酸最简式相同为CH2O,只需要计算3.0gCH2O的物质的量计算原子数=$\frac{3.0g}{30g/mol}$×4×NA=0.4NA,故A错误;
B.当反应生成2molHCl时,断裂2mol化学键,故当生成标况下22.4LHCl即1molHCl时,断裂1mol化学键即NA个,故B错误;
C.1mol的白磷(P4)含的共价健数均为6NA,四氯化碳(CCl4)中所含的共价健数为4NA,故C错误;
D.电解饱和食盐水若产生标准状况下22.4L氢气,物质的量为1mol,阳极氯离子失电子生成氯气,依据氢气生成计算转移的电子数为2NA,故D正确;
故选:D.
点评 本题考查了阿伏伽德罗常数的应用,主要考查物质组成特征,质量换算物质的量计算微粒数,气体摩尔体积的条件应用,电解反应电子转移计算,题目难度中等,注意白磷与四氯化碳结构区别.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 甲 | 乙 | |
| 丙 | 丁 | 戊 |
| A. | 非金属性:甲<丙 | B. | 原子半径:乙<丁 | ||
| C. | 最外层电子数:乙<丙 | D. | 戊一定是硫元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
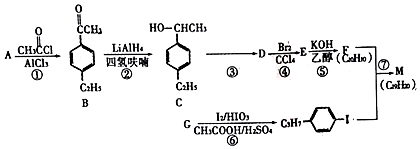
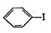 +H≡C-H→
+H≡C-H→ =C+H,回答下列问题:
=C+H,回答下列问题: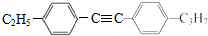 ,A的名称为乙苯.
,A的名称为乙苯. .
.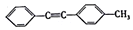 的合成路线:
的合成路线:查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 青蒿素分子式为C15H2405 | |
| B. | 反应②原子利用率为100% | |
| C. | 该过程中青蒿素生成双氢青蒿素属于氧化反应 | |
| D. | 1 mol青蒿琥酯与氢氧化钠溶液反应,最多消耗1 mol氢氧化钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
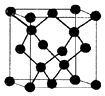 有A、B、C、D、E五种原子序数增大的元素,只有一种为金属.A、B、C均为第二周期紧邻元素,其第一电离能顺序为B>C>A;B与D同主族;E为第4周期副族元素,其价层电子为全满.
有A、B、C、D、E五种原子序数增大的元素,只有一种为金属.A、B、C均为第二周期紧邻元素,其第一电离能顺序为B>C>A;B与D同主族;E为第4周期副族元素,其价层电子为全满.| 氢化物 | HxA-AHx | HmB-BHm | HnC-CHn |
| 键能(kJ.mol-1 | 346 | 247 | 207 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com