
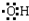 ;
;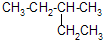 的系统命名为3-甲基戊烷.
的系统命名为3-甲基戊烷.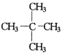 ;
; .
. .
. 分析 (1)羟基为中性原子团,氧原子最外层含有7个电子;
(2)该有机物为烷烃,根据烷烃的命名原则写出其名称;
(3)设烷烃的分子式为CxH(2x+2),根据相对分子质量为72,列出方程式进行计算x值,支链越多,沸点越低;
(4)某芳香烃的相对分子质量为102,则分子中最大C原子数目为$\frac{102}{12}$=8…6,结合烷烃中碳原子与H原子关系,可知7个碳原子最多需要16故H原子,故该芳香烃中含有8个碳原子、6个H原子,分子式为C8H6,不饱和度为$\frac{8×2+2-6}{2}$=6,则侧链不饱和度为2,该分子内所有原子均在同一平面内,应是苯乙炔;
(5)先根据碳链异构和位置异构写出同分异构体,然后根据手性碳原子指连有四个不同基团的碳原子来确定结构简式.
解答 解:(1)羟基中含有1个氧氢键,为中性原子团,羟基的电子式为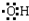 ,故答案为:
,故答案为: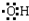 ;
;
(2)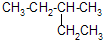 的主链为戊烷,甲基在3号C,该有机物名称为:3-甲基戊烷,故答案为:3-甲基戊烷;
的主链为戊烷,甲基在3号C,该有机物名称为:3-甲基戊烷,故答案为:3-甲基戊烷;
(3)设烷烃的分子式为CxH(2x+2),
则14x+2=72,解得x=5,
所以该烷烃的分子式为C5H12,
分子式为C5H12的同分异构体有主链有5个碳原子的:CH3CH2CH2CH2CH3,
主链有4个碳原子的:CH3CH(CH3)CH2CH3,
主链有3个碳原子的:CH3C(CH3)2CH3;
支链越多,沸点越低,故沸点最低的为:CH3C(CH3)2CH3,
故答案为: ;
;
(4)某芳香烃的相对分子质量为102,则分子中最大C原子数目为$\frac{102}{12}$=8…6,结合烷烃中碳原子与H原子关系,可知7个碳原子最多需要16故H原子,故该芳香烃中含有8个碳原子、6个H原子,分子式为C8H6,不饱和度为$\frac{8×2+2-6}{2}$=6,则侧链不饱和度为2,该分子内所有原子均在同一平面内,应是苯乙炔,结构简式为 ,
,
故答案为: ;
;
(5)C4H10O的同分异构体中,属于醇类且含有“手性碳原子”的结构简式为

点评 本题考查了有机物结构与性质、有机物分子式、结构简式的确定,题目难度中等,明确常见有机物结构与性质为解答关键,试题知识点较多、综合性较强,充分考查学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:填空题
 为验证氧化性:Cl2>Fe3+>SO2,某小组用图所示装置进行实验(夹持仪器和甲中加热装置已略,气密性已检验).
为验证氧化性:Cl2>Fe3+>SO2,某小组用图所示装置进行实验(夹持仪器和甲中加热装置已略,气密性已检验).| 步骤3溶液中含有的离子 | 步骤5溶液中含有的离子 | |
| Ⅰ | 既有Fe3+又有Fe2+ | 有SO42- |
| Ⅱ | 有Fe3+无Fe2+ | 有SO42- |
| Ⅲ | 有Fe3+无Fe2+ | 有Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该元素的名称是铁 | B. | 该元素的原子序数为26 | ||
| C. | 该元素在地壳中的含量为55.85% | D. | 该元素的元素符号为Fe |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | P4和NO2都是共价化合物 | |
| B. | 次氯酸的结构式为H-Cl-O | |
| C. | 在CaO和SiO2晶体中,都不存在单个小分子 | |
| D. | CCl4和NH4Cl都是以共价键结合的分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (1)(2) | B. | (1)(3) | C. | (2)(3) | D. | (1)(2)(3)(4) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 糖类物质是绿色植物光合作用的产物,是动、植物所需能量的重要来源 | |
| B. | 淀粉和纤维素是天然高分子化合物 | |
| C. | 虽然纤维素水解的最终产物是葡萄糖,但由于人体内没有水解纤维素的酶,所以食物中的纤维素对人体没有任何作用 | |
| D. | 食物中的营养素主要包括糖类、油脂、蛋白质、维生素、无机盐和水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com