
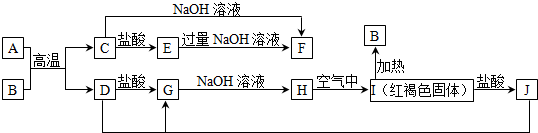
分析 I为红褐色固体,则I为Fe(OH)3,加热分解生成B为Fe2O3,I与盐酸反应生成J,则J为FeCl3;D与J反应生成G,G与氢氧化钠反应生成H,H在空气中转化为氢氧化铁,则H为Fe(OH)2.A、D为金属单质,A与B的反应生成C与D,则C为金属氧化物,C能与氢氧化钠、盐酸反应,则C为Al2O3,故A为Al,D为Fe,则G为FeCl2,结合转化关系可知E为AlCl3,F为NaAlO2,据此进行解答.
解答 解:I为红褐色固体,则I为Fe(OH)3,加热分解生成B为Fe2O3,I与盐酸反应生成J,则J为FeCl3.D与J反应生成G,G与氢氧化钠反应生成H,H在空气中转化为氢氧化铁,则H为Fe(OH)2.A、D为金属单质,A与B的反应生成C与D,则C为金属氧化物,C能与氢氧化钠、盐酸反应,则C为Al2O3,故A为Al,D为Fe,则G为FeCl2,结合转化关系可知E为AlCl3,F为NaAlO2,
(1)由上述分析可知,C是Al2O3,H为Fe(OH)2,
故答案为:Al2O3;Fe(OH)2;
(2)A为Al,B为氧化铁,铝与氧化铁在高温下发生铝热反应,反应的化学方程式为:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3,工业上利用该反应进行焊接钢轨,
故答案为:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3;焊接钢轨;
(3)D为Fe,G为FeCl2,J与D反应转化为G的离子方程式为:2Fe3++Fe═3Fe2+,
故答案为:2Fe3++Fe═3Fe2+.
点评 本题考查无机物推断,难度中等,I为红褐色及C能与酸、碱反应等为突破口,侧重考查学生的推理能力及对与元素化合物的性质熟练掌握,试题培养了学生的分析、理解能力及逻辑推理能力.


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:选择题
| A. | FeBr2溶液中通入少量的Cl2:2Fe2++Cl2═2Fe3++2Cl- | |
| B. | Ca(HCO3)2溶液与过量NaOH溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O | |
| C. | 等物质的量的MgCl2、Ba(OH)2和HCl溶液混合:Mg2++2OH-═Mg(OH)2↓ | |
| D. | 铜溶于稀硝酸中:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径 (10-10m) | 0.73 | 1.02 | 1.34 | 1.06 | 0.99 | .5 4 | 0.75 | 1.18 |
| 最高或最 低化合价 | +6 | +1 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -2 | -3 | -1 | -3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
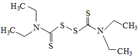 )会抑制肝脏中的乙醛脱氢酶,造成危害,严重的可能导致死亡.许多抗菌药(如:头孢)具有与双硫仑相似的作用,因此服用头孢后严禁饮酒.下列有关说法不正确的是( )
)会抑制肝脏中的乙醛脱氢酶,造成危害,严重的可能导致死亡.许多抗菌药(如:头孢)具有与双硫仑相似的作用,因此服用头孢后严禁饮酒.下列有关说法不正确的是( )| A. | “双硫仑”分子式为C10H12N2S4,在水中的溶解度较小 | |
| B. | 反应①②均属于氧化反应 | |
| C. | 一个人的酒量大小取决于体内上述两种酶的多少 | |
| D. | 乙醛是对人体有害的物质,含官能团名称为“醛基” |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有些活泼金属如钠、镁、铝可作热还原法的还原剂 | |
| B. | 用电解熔融NaCl的方法来冶炼金属钠 | |
| C. | 回收废旧金属可以重新制成金属或它们的化合物 | |
| D. | 可用焦炭或一氧化碳还原氧化铝的方法来冶炼铝 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com