
分析 (1)设硫酸溶液的质量为m,表示出不同浓度硫酸中溶质的质量,二者之和为混合后溶液中溶质质量,混合后溶液的质量为2m,进而计算混合后的溶质的质量分数;
设体积分别为VmL,30%的H2SO4溶液密度为ρ1,50%的H2SO4溶液密度为ρ2,表示出混合后溶液中溶质质量分数,硫酸的浓度越大密度越大,结合表达式判断质量分数关系;
(2)设98%的浓H2SO4的密度为ρ1,49%的H2SO4的密度为ρ2,硫酸浓度越大,密度越大,则ρ1>ρ2,根据c=$\frac{1000ρω}{M}$表示出物质的量浓度,据此判断;
解答 解:(1)设硫酸溶液的质量为m,30%的H2SO4溶质为质量0.3m,50%的H2SO4溶质的质量为0.5m,混合后总质量为2m,所以w(H2SO4)=$\frac{0.3m+0.5m}{2m}$=40%;
如果等体积混合,设体积分别为VmL,30%的H2SO4溶液密度为ρ1,50%的H2SO4溶液密度为ρ2,则混合后溶液的质量分数为w(H2SO4)=$\frac{V{ρ}_{1}×30%+V{ρ}_{2}×50%}{V{ρ}_{1}+V{ρ}_{2}}$=30%+20%×$\frac{{ρ}_{2}}{{ρ}_{1}+{ρ}_{2}}$,因硫酸的浓度越大,密度越大,则ρ1<ρ2,则$\frac{{ρ}_{2}}{{ρ}_{1}+{ρ}_{2}}$>$\frac{1}{2}$,故30%+20%×$\frac{{ρ}_{2}}{{ρ}_{1}+{ρ}_{2}}$>40%,
故答案为:等于;大于;
(2)设98%的浓H2SO4的密度为A,49%的H2SO4的密度为a,根据c=$\frac{1000ρω}{M}$可知,18.4=$\frac{1000ρ1×49%}{98}$,49%的H2SO4的物质的量浓度为$\frac{1000{ρ}_{2}×49%}{98}$mol/L,硫酸浓度越大,密度越大,则ρ1>ρ2,故$\frac{1000{ρ}_{2}×49%}{98}$mol/L<9.2mol/L,
故答案为:小于;
点评 本题考查溶液浓度计算,侧重考查学生分析计算能力,注意对公式的理解与应用,注意硫酸的浓度越大密度越大,题目难度中等.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 它是一种共价化合物 | |
| B. | 在加热时此化合物可以分解为 PH3和 HI 或 H2和 I2 | |
| C. | 这种化合物能跟碱反应 | |
| D. | 该化合物可以由 PH3 和 HI 化合而成 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
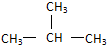
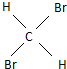 与
与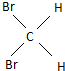
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇和浓硫酸加热到140℃制取乙烯 | |
| B. | 乙烷和氯气光照下制取纯净的氯乙烷 | |
| C. | 在苯和溴水的混合物中加入铁粉制取溴苯 | |
| D. | 用酸性高锰酸钾溶液区分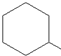 和 和 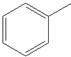 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 在新生成的AgCl沉淀中滴入稀KI溶液,振荡 | 白色沉淀转化为黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| B | 向装有Fe(NO3)2溶液的试管中加入稀H2SO4, | 在管口观察到红棕色气体 | HNO3分解成了NO2 |
| C | 向CH3CH2X中加入少量AgNO3溶液,加热 | 有浅黄色沉淀生成 | CH3CH2X中含有Br- |
| D | 向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后再加入新制Cu(OH)2浊液,加热, | 没有红色沉淀生成 | 淀粉没有水解成葡萄糖 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 乙醇分子球棍模型: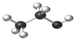 | B. | 含有10个中子的氧原子${\;}_{-8}^{-18}$O | ||
| C. | -OH的电子式: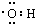 | D. | CH4Si的结构式: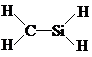 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | 用图①所示实验可比较氯、碳、硅三种元素的非金属性强弱 | |
| B. | 用图②所示实验装置排空气法收集CH4气体 | |
| C. | 图③表示可逆反应“CO(g)+H2O(g)?CO2(g)+H2(g)”为放热反应 | |
| D. | 图④中的装置可形成原电池,电流从锌片经导线流向铜片 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com