
常温下,用0.1000 mol·L-1 NaOH溶液分别滴定20.00 mL 0.100 0 mol·L-1 HA溶液(滴定曲线见图1)和20.00 mL 0.100 0 mol·L-1 HB溶液(滴定曲线见图2)。下列说法正确的是( )
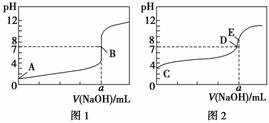
A.图1可以表示NaOH滴定盐酸的曲线
B.图1中B点状态时,溶液中有:c(Na+)=c(A-)
C.达到B、E状态时,反应消耗n(HA)<n(HB)
D.当0<V(NaOH)<20.0 mL时,对应混合溶液中各离子浓度由大到小的顺序均为c(A-)>c(Na+)>c(H+)>c(OH-)
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
工业上制备纯硅反应的热化学方程式如下:
SiCl4(g)+2H2(g) 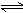 Si(s)+4HCl(g)
Si(s)+4HCl(g)  mol(Q>0)
mol(Q>0)
某温度、压强下,将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是
A.反应过程中,若增大压强能提高SiCl4的转化率
B.若反应开始时SiCl4为1 mol,则达平衡时,吸收热量为Q kJ
C.反应至4 min时,若HCl浓度为0.12 mol/L,则H2的反应速率为0.03 mol/(L·min)
D.当反应吸收热量为0.025Q kJ时,生成的HCl通入100 mL 1 mol/L的NaOH溶液恰好反应
查看答案和解析>>
科目:高中化学 来源: 题型:
向某一容积为5 L的密闭容器中,加入 0.2 mol CO和0.2 mol H2O,在800℃和催化剂的条件下,发生如下反应:CO(g)+H2O(g) 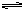 CO2(g)+H2(g) ΔH>0,反应中CO2的浓度随时间变化关系如下图所示:
CO2(g)+H2(g) ΔH>0,反应中CO2的浓度随时间变化关系如下图所示:
(1)由图可知,反应从开始至达到平衡时,CO的化学反应速率v(CO)= ;H2的物质的量浓度c(H2)= ;该温度下此反应的平衡常数K= 。
(2)能说明该反应已达到平衡状态的是 (填序号)。
①CO、H2O、CO2、H2的浓度都相等
②密闭容器内压强保持不变
③CO减少的化学反应速率和CO2减少的化学反应速率相等
④CO、H2O、CO2、H2的浓度都不再发生变化
⑤密闭容器内密度保持不变
(3)若开始时向该容器中加入CO、H2O(g)、CO2和H2各0.1 mol,在相同条件下,反应达到平衡时,水蒸气的物质的量浓度c(H2O)= 。
(4)查表已知BaSO4(s)+4C(s)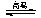 4CO(g)+BaS(s) △H1= +571.2 kJ·mol-1 ①
4CO(g)+BaS(s) △H1= +571.2 kJ·mol-1 ①
BaSO4(s)+2C(s)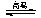 2CO2(g)+BaS(s) △H2= +226.2 kJ·mol-1 ②
2CO2(g)+BaS(s) △H2= +226.2 kJ·mol-1 ②
则反应C(s)+CO2(g)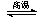 2CO(g)的△H= 。
2CO(g)的△H= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间的转化关系如下图所示。下列有关物质的推断正确的是( )
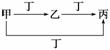
| 选项 | 甲 | 乙 | 丙 | 丁 |
| A | C | CO | CO2 | O2 |
| B | CO | HCO | CO2 | H+ |
| C | Cl2 | FeCl3 | FeCl2 | Fe |
| D | Al3+ | Al(OH)3 | AlO | NH3·H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,向20 mL 0.2 mol·L-1 H2A溶液中滴加0.2 mol·L-1 NaOH溶液。有关微粒物质的量变化如下图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-)。根据图示判断,下列说法正确的是( )
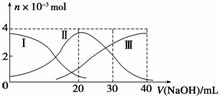
A.H2A在水中的电离方程式是:H2A===H++HA-、HA-H++A2-
B.当V(NaOH)=20 mL时,溶液中各粒子浓度的大小顺序为c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
C.等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水大
D.当V(NaOH)=30 mL时,溶液中存在以下关系:2c(H+)+c(HA-)+2c(H2A)=c(A2-)+2c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
室温下,将0.05mol Na2CO3固体溶于水配成100mL溶液,向溶液中加入下列物质。有关结论正确的是
| 加入的物质 | 结论 | |
| A | 50mL 1mol·L-1H2SO4 | 反应结束后,c(Na+)=c(SO42-) |
| B | 0.05molCaO | 溶液中 |
| C | 50mL H2O | 由水电离出的c(H+)·c(OH—)不变 |
| D | 0.1molNaHSO4固体 | 反应完全后,溶液pH减小,c(Na+)不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
[选修3—物质结构与性质]
19—Ⅰ(6分)下列物质的结构或性质与氢键无关的是
A.乙醚的沸点 B.乙醇在水中的溶解度
C.氢化镁的晶格能 D.DNA的双螺旋结构
19—Ⅱ(14分)钒(23V)是我国的丰产元素,广泛用于催化及钢铁工业。
回答下列问题:
(1)钒在元素周期表中的位置为 ,其价层电子排布图为 。
(2)钒的某种氧化物的晶胞结构如图1所示。晶胞中实际拥有的阴.阳离子个数分别为 . 。
(3)V2O5常用作SO2 转化为SO3的催化剂。SO2 分子中S原子价层电子对数是 对,分子的立体构型为 ;SO3气态为单分子,该分子中S原子的杂化轨道类型为 ;SO3的三聚体环状结构如图2所示,该结构中S原子的杂化轨道类型为 ;该结构中S—O键长由两类,一类键长约140pm,另一类键长约为160pm,较短的键为 (填图2中字母),该分子中含有 个键。
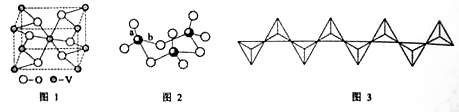
(4)V2O5 溶解在NaOH溶液中,可得到钒酸钠(Na3VO4),该盐阴离子的立体构型为 ;也可以得到偏钒酸钠,其阴离子呈如图3所示的无限链状结构,则偏钒酸钠的化学式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
由14CO和12CO组成的混合气体与同温同压下空气的密度相等(空气的平均相对分子质量为29),则下列关系正确的是( )
A.混合气体中,12CO占有的体积大于14CO占有的体积
B.混合气体中,12CO与14CO分子个数之比为1∶2
C.混合气体中,12CO与14CO质量之比为15∶14
D.混合气体中,12CO与14CO密度之比为14∶15
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com