
设NA为阿伏加德罗常数,下列叙述正确的是
①lmolCH3CH2C(CH3)3所含甲基个数为4NA
②2.8g乙烯和2.8g聚乙烯中含碳原子数均为0.2NA
③1.0L1.0mol/LCH3COOH溶液中,CH3COOH分子数为NA
④8.8g乙酸乙酯中含共用电子对数为1.4NA
⑤标准状况下,22.4L乙醇完全燃烧后生成CO2的分子数为2NA
⑥常温常压下,17g甲基(一14CH3)所含的中子数为9NA
⑦标准状况下,11.2L氯仿中含有C—Cl键的数目为1.5NA
⑧lmolC15H32分子中含碳碳键数目为14NA
A.①③⑤⑦ B.①②④⑧ C.②③⑥⑧ D.①②⑥⑧
科目:高中化学 来源:2016届河南省洛阳市高三上学期12月统考化学试卷(解析版) 题型:选择题
室温下,0.1 mol/L的某二元酸H2A溶液中,溶液中可能存在的含A粒子(H2A、HA一、A2-)的物质的量分数随pH变化的关系如图所示,下列说法正确的是
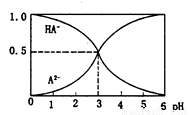
A.H2A的电离方程式:H2A  H十+HA-
H十+HA-
B.pH=5时,在NaHA和Na2A的混合溶液中:c(HA-):c(A2-)=l:100
C.等物质的量浓度NaHA和Na2A溶液等体积混合,离子浓度大小关系为:[c(Na+))c(HA-)>c(A2-)
D.Na2A溶液必存在c(OH一)=c(H+)+c(HA-)十2c(H2A),各粒子浓度均大0
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三上学期12月月考化学试卷(解析版) 题型:选择题
下列实验装置设计正确、且能达到目的的是
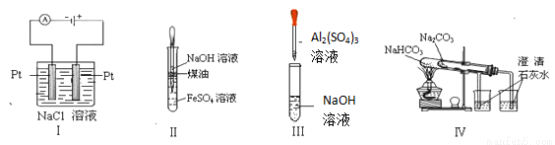
A.实验Ⅰ:制取金属钠
B.实验II:制取Fe(OH)2
C.实验Ⅲ:制取少量的氢氧化铝
D.实验Ⅳ:比较两种物质的热稳定性
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三上学期第四次月考化学试卷(解析版) 题型:选择题
下列电解质溶液的有关叙述正确的是
A.同浓度、同体积的强酸与强碱溶液混合后,溶液的pH=7
B.在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)增大
C.含1 mol KOH的溶液与1 mol CO2完全反应后,溶液中c(K+)= c(HCO3-)
D.在CH3COONa溶液中加入适量CH3COOH,可使 c(Na+)= c(CH3COO-)
c(Na+)= c(CH3COO-)
查看答案和解析>>
科目:高中化学 来源:2016届河南省洛阳市高三上学期12月统考化学试卷(解析版) 题型:选择题
心脏起搏器一般是给心跳缓慢的病人使用。某种类型的心脏起搏器工作时发生下列反应:4Li+2SOC12 =4LiC1+S+SO2,下列有关判断正确的是
A.还原剂只有锂
B.SOC12中每个原子都达到8电子稳定结构
C.氧化产物包括LiCl和SO2
D.生成1. 12 LSO2时,反应转移电子为0.2 mol
查看答案和解析>>
科目:高中化学 来源:2016届山东省北校高三上学期第二次单元测试化学试卷(解析版) 题型:填空题
短周期主族元素A、B、C、D、E、F的原子序数依次递增,A、B两元素相邻,B、C、E原子的最外层电子数之和为13,C原子最外层电子数是E原子最外层电子数的3倍,B、F原子最外层电子数之和等于C、E原子最外层电子数之和.请回答下列问题:
(1)B元素在元素周期表中的位置为 .
(2)元素C和D可形成两种化合物D2C、D2C2,其中均含有的化学键类型是 ;元素E、F形成的最高价氧化物对应水化物的碱性强弱关系为 > (填化学式).
(3)E的单质能与A的最高价氧化物发生置换反应,反应的化学方程式为 ;
(4)F的单质加入到D的最高价氧化 物对应水化物的溶液中,发生反应的离子方程式为 .
物对应水化物的溶液中,发生反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源:2016届山东省北校高三上学期第二次单元测试化学试卷(解析版) 题型:选择题
用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g)?CH3OH(g)△H<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示.下列说法正确的是

A.温度: T1>T2>T3
B.正反应速率:υ(b)>υ(d) υ(a)>υ(c)
C.平衡常数:K(a)>K(c) K(b)=K(d)
D.平均摩尔质量: M(b)>M(d) M(a)<M(c)
查看答案和解析>>
科目:高中化学 来源:2016届山西省高三上学期11月半月考试化学试卷 (解析版) 题型:实验题
有一混合物的水溶液,只可能含以下离子中的若干种:K+ 、Al3+ 、Fe3+ 、Mg2+ 、Ba2+ 、 NH4+、Cl- 、CO32-、SO42 -,现取三份100 mL溶液进行如下实验:
①第一份加入AgNO3溶液有沉淀产生。
②第二份加过量NaOH溶液加热后收集到气体0.02 mol,无沉淀生成,同时得到溶液甲。
③在甲溶液中通过量CO2,生成白色沉淀,沉淀经过滤、洗涤、灼烧,质量为1.02 g。
④第三份加足量BaCl2溶液后得白色沉淀,沉淀经足量盐酸洗涤干燥后质量为11.65 g。
根据上述实验回答:
(1)一定不存在的离子是___________,不能确定是否存在的离子是_____________。
(2)试确定溶液中肯定存在的阴离子及其浓度(可不填满):
离子符号______,浓度__________________;
离子符号______,浓度__________________;
(3)试确定K+ 是否存在________(填“是”或“否”),判断的理由是__________。
查看答案和解析>>
科目:高中化学 来源:2016届陕西省高三上学期第四次质检化学试卷(解析版) 题型:选择题
对于白磷引起的中毒,硫酸铜溶液是一种解毒剂,有关反应如下:11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4下列关于该反应的说法正确的是
A.CuSO4发生了氧化反应
B.生成1 mol H3PO4时,有10 mol 电子转移
C.白磷只作还原剂
D.氧化产物和还原产物的物质的量之比为6∶5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com