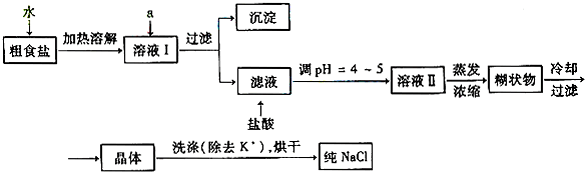
解:(1)①要除去SO
42-,只有选BaCl
2溶液,若选用Ba(NO
3)
2,会引入新的离子NO
3-,再选用NaOH溶液除去Mg
2+和Fe
3+溶液,最后选用Na
2CO
3溶液除去Ca
2+,此处不能选用K
2CO
3溶液,否则会引入新的K
+,再用HCl除去过量的CO
32-,Na
2CO
3溶液不能加在BaCl
2溶液前,否则会引入Ba
2+,故答案为:BaCl
2、NaOH、Na
2CO
3;加适量盐酸,与①中过量NaOH溶液和过量Na
2CO
3溶液发生反应,生成氯化钠、水和二氧化碳气体,故答案为:BaCl
2、NaOH、Na
2CO
3;中和溶液中过量的OH
-和CO
32-;
②检验洗涤液中是否有钾离子,可用干净铂丝取最后一次洗涤液在酒精灯上灼烧,透过蓝色钴玻璃,如不出现紫色火焰,则说明已洗净,故答案为:用干净铂丝取最后一次洗涤液在酒精灯上灼烧,透过蓝色钴玻璃,如不出现紫色火焰,则说明已洗净;
(2)需氯化钠的质量为m=0.5L×4.00mol?L
-1×58.5g/mol=117.0g;配制500mL4.00mol?L
-1NaCl溶液,操作步骤有计算、称量、溶解、移液、洗涤移液、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解,用玻璃棒搅拌,加速溶解,恢复室温后转移到500mL容量瓶中,并用玻璃棒引流,洗涤2-3次,并将洗涤液移入容量瓶中,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.
所以需要的仪器有托盘天平、烧杯、玻璃棒、500ml的容量瓶、胶头滴管、药匙.
使用还需要托盘天平、500ml的容量瓶、胶头滴管,故答案为:117;天平、500mL容量瓶、胶头滴管;
(3)电解饱和食盐水的反应:2NaCl+2H
2O

2NaOH+Cl
2↑+H
2↑,在阴级区内产生的Cl
2能与该区生成的NaOH反应NaCl、NaClO和H
2O,使得部分的Cl
2被消耗,所以同样条件下收集到的Cl
2小于2L,故答案为:<;电解生成的氯气与电解生成的NaOH发生了反应.
分析:(1)①欲除去溶液I中的Ca
2+、Mg
2+、Fe
3+、SO
42-离子,可以分别采用碳酸钠、氢氧化钠、氢氧化钠和氯化钡,根据试剂的添加原则来回答;加入盐酸可以除去过量的碳酸钠和氢氧化钠等; ②检验洗涤液中是否有钾离子;
(2)利用n=cv计算出氯化钠的物质的量,再根据m=nM计算所需氯化钠的质量;根据配制溶液的步骤操作选择所用仪器;
(3)根据电解饱和食盐水时的产物以及氯气和氢氧化钠的反应来回答.
点评:本题主要考查了在粗盐提纯的过程中所选用除杂和净化的方法、溶液的配制等,除去杂质不要引入新的杂质,对于实验过程中过量的试剂都要除去.


 2NaOH+Cl2↑+H2↑,在阴级区内产生的Cl2能与该区生成的NaOH反应NaCl、NaClO和H2O,使得部分的Cl2被消耗,所以同样条件下收集到的Cl2小于2L,故答案为:<;电解生成的氯气与电解生成的NaOH发生了反应.
2NaOH+Cl2↑+H2↑,在阴级区内产生的Cl2能与该区生成的NaOH反应NaCl、NaClO和H2O,使得部分的Cl2被消耗,所以同样条件下收集到的Cl2小于2L,故答案为:<;电解生成的氯气与电解生成的NaOH发生了反应.

 名校课堂系列答案
名校课堂系列答案