
分析 ①CH2═CHCH2CH2CH2OH中含碳碳双键、-OH,具有烯烃和醇的性质;
②(CH3)3COH含-OH,具有醇的性质;
③(CH3)3CCH2OH含-OH,具有醇的性质;
④CH2═CHCOOH含碳碳双键、-COOH,具有烯烃和羧酸的性质;
⑤CH3CH(CH3)OH,含-OH,具有醇的性质,以此来解答.
解答 解:①CH2═CHCH2CH2CH2OH中含碳碳双键、-OH,具有烯烃和醇的性质;
②(CH3)3COH含-OH,具有醇的性质;
③(CH3)3CCH2OH含-OH,具有醇的性质;
④CH2═CHCOOH含碳碳双键、-COOH,具有烯烃和羧酸的性质;
⑤CH3CH(CH3)OH,含-OH,具有醇的性质,则
(1)上述物质所含有的官能团除了羟基外,还有碳碳双键、羧基,故答案为:碳碳双键、羧基;
(2)与-OH相连C的邻位C上没有H不能发生消去反应,则上述醇中③不能发生消去反应,故答案为:③;
(3)只有④中含-COOH,与金属钠反应放氢气最快,故答案为:④;
(4)与-OH相连C上有H可发生催化氧化,则上述醇中②不能发生催化氧化,故答案为:②;
(5)含碳碳双键与溴水发生加成反应,含-COOH与碳酸氢钠反应生成气体,则④既能使溴的四氯化碳溶液褪色,又能与NaHCO3作用放出CO2气体,故答案为:④.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物的官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意烯烃、醇、羧酸的性质,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
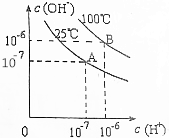
| A. | 25℃时,0.1mol/LNaOH溶液与0.1mol/L乙酸溶液等体积混合,所得溶液的pH等于7 | |
| B. | 25℃时,pH=11的氨水与pH=3的盐酸等体积混合,所得溶液的pH小于7 | |
| C. | 100℃时,pH=12的NaOH溶液aL和pH=2的H2SO4溶液bL恰好中和,则a:b=1:1 | |
| D. | 100℃时,pH=12的NaOH溶液和pH=9的NaOH溶液等体积混合,所得溶液的pH约为11.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
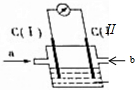 如右图所示的原电池装置中,电解质溶液为氢氧化钠溶液,a、b分别为H2、O2中的一种,C(Ⅰ)、C(Ⅱ)均为多孔石墨电极.通入气体后,发现电流表指针发生如图所示偏转.则:
如右图所示的原电池装置中,电解质溶液为氢氧化钠溶液,a、b分别为H2、O2中的一种,C(Ⅰ)、C(Ⅱ)均为多孔石墨电极.通入气体后,发现电流表指针发生如图所示偏转.则:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源:2017届湖北省荆门市高三上九月联考化学试卷(解析版) 题型:填空题
一种回收并利用含碘(I-)废液的工艺流程如下: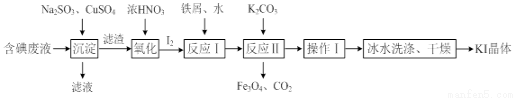
(1)“沉淀”中生成CuI的离子方程式为___________________。
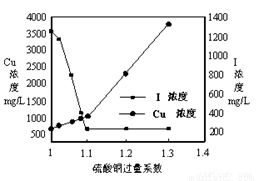
(2)CuSO4的投加量对废水中I-的去除量影响较大,不同投加量(用过量系数表示)下,反应后I-和Cu2+的浓度如图所示,则适宜的CuSO4过量系数应为_____________,分析原因_________________。
(3)反应Ⅰ中生成铁与碘的化合物(其中铁与碘的质量比为21:127),则加入的水的作用是________________,反应Ⅱ的化学方程式是_________________________。
(4)操作Ⅰ包括____________,冰水洗涤的目的是_______________。
查看答案和解析>>
科目:高中化学 来源:2017届福建省高三上第二次月考化学试卷(解析版) 题型:选择题
将氯化铝溶液和氢氧化钠溶液等体积混合,得到的沉淀物中铝元素的质量与溶液中所含铝元素的质量相等,则原氯化铝溶液和氢氧化钠溶液的物质的量浓度之比可能是( )
A.1∶3 B.2∶3 C.1∶4 D.2∶1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com