
【题目】同为1L的HCl溶液(浓度为c1)和H2SO4溶液(浓度为c2),若其中的c(H+)相同,则它们的物质的量的浓度c1和c2的关系是
A. c1 < c2 B. 2c1=c2 C. c1=2c2 D. 不能确定
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某可充电的锂离子电池以LiMn2O4为正极,嵌入锂的碳材料为负极,含Li+导电固体为电解质.充放电时的电池反应为:Li+LiMn2O4 ![]() Li2Mn2O4 . 下列说法正确的是( )
Li2Mn2O4 . 下列说法正确的是( )
A.放电时,LiMn2O4发生氧化反应
B.放电时,正极反应为:Li++LiMn2O4+e﹣═Li2Mn2O4
C.充电时,LiMn2O4发生氧化反应
D.充电时,阳极反应为:Li++e﹣═Li
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】秋葵是一种大众喜爱的食材,含有蛋白质、维生素A、维生素C、纤维素、阿拉伯果糖和丰富的铁、锌、钙等元素,其中属于糖类的有( )
A. 维生素A和维生素C
B. 蛋白质和维生素A和维生素C
C. 纤维素和阿拉伯果糖
D. 阿拉伯果糖 和铁、锌、钙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的性质或应用说法不正确的是 ( )
A. 用溴水可以区分苯和四氯化碳
B. 淀粉和纤维素水解的最终产物均为葡萄糖
C. 烷烃、烯烃都属于碳氢化合物
D. 食用植物油在烧碱溶液中水解的主要产物是高级饱和脂肪酸钠和甘油
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA代表阿伏加德罗常数的值,下列说法正确的是
A. 阿伏伽德罗常数是6.02×1023 B. 标准状况下,11.2 L CCl4所含分子数为0.5NA
C. 0.1 mol CH4所含氢原子数为0.4NA D. 常温常压下,28 g N2中所含原子个数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)反应Fe(s)+CO2(g)![]() FeO(s)+CO(g) ΔH1,平衡常数为K1
FeO(s)+CO(g) ΔH1,平衡常数为K1
反应Fe(s)+H2O(g)![]() FeO(s)+H2(g) ΔH2,平衡常数为K2
FeO(s)+H2(g) ΔH2,平衡常数为K2
在不同温度时K1、K2的值如下表:
700℃ | 900℃ | |
K1 | 1.47 | 2.15 |
K2 | 2.38 | 1.67 |
反应CO2(g)+H2(g)![]() CO(g)+H2O(g) ΔH,平衡常数为K,则ΔH=_______(用ΔH1和ΔH2表示),K=________(用K1和K2表示),且由上述计算可知,反应CO2(g)+H2(g)
CO(g)+H2O(g) ΔH,平衡常数为K,则ΔH=_______(用ΔH1和ΔH2表示),K=________(用K1和K2表示),且由上述计算可知,反应CO2(g)+H2(g) ![]() CO(g)+H2O(g)是_________反应(填“吸热”或“放热”)。
CO(g)+H2O(g)是_________反应(填“吸热”或“放热”)。
(2)一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应Fe(s)+CO2(g)![]() FeO(s)+CO(g) ΔH>0,CO2的浓度与时间的关系如图1所示:
FeO(s)+CO(g) ΔH>0,CO2的浓度与时间的关系如图1所示:

①该条件下反应的平衡常数为___________;若铁粉足量,CO2的起始浓度为2.0 mol/L,则平衡时CO2的浓度为________mol/L。
②下列措施中能使平衡时CO物质的量百分数增大的是________(填序号)。
A.升高温度 B.增大压强
C.再充入一定量的CO2 D.再加入一定量铁粉
(3)对于可逆反应Fe(s)+CO2(g)![]() FeO(s)+CO(g),该反应的逆反应速率随时间变化的关系如图2。
FeO(s)+CO(g),该反应的逆反应速率随时间变化的关系如图2。
①从图中看到,反应在t2时达平衡,在t1时改变了某种条件,改变的条件可能是______。
A.升温 B.增大CO2浓度 C.使用催化剂
②如果在t3时从混合物中分离出部分CO,t4~t5时间段反应处于新平衡状态,请在图上画出t3~t5的v逆变化曲线_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2L的恒容密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示: 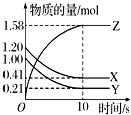
(1)该反应的化学方程式为 .
(2)从反应开始到10s时,用Y表示的反应速率为 , X的转化率为 . (保留三位有效数字)
(3)10s时,该反应达到了化学平衡状态.(填“是”或“否”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将6mol A 气体和3mol B气体置于3L的密闭容器中,混合后发生如下反应:2A(g)+B(g)═2C(g).若经2s后测得B的浓度为0.4mol/L,下列说法正确的是( )
A.用物质A表示的反应速率为0.4mol/(Ls)
B.用物质B表示的反应速率为0.4mol/(Ls)
C.2 s时物质B的转化率为40%
D.2 s时物质C的浓度为1.2 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中反应制得:①3SiO2+6C+2N2![]() Si3N4+6CO;也可由SiCl4的蒸汽和NH3反应制取:②3SiCl4+4NH3
Si3N4+6CO;也可由SiCl4的蒸汽和NH3反应制取:②3SiCl4+4NH3![]() Si3N4+12HCl。则下列叙述正确的是
Si3N4+12HCl。则下列叙述正确的是
A. 反应②属于离子反应
B. 若制取等量的Si3N4,则反应①②转移电子数目必然相等
C. 反应①的氧化剂是N2
D. 反应①中氧化产物与还原产物物质的量之比为1∶6
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com