
二甲醚(CH3OCH3)是一种重要的清洁燃料气,其储运、燃烧安全性、理论燃烧温度等性能指标均优于液化石油气,也可用作燃烧电池的燃料,具有很好的好展前景。
(1)已知H2、CO和CH3OCH3的燃烧热(ΔH)分别为-285.5kJ/mol、-283kJ/mol和-1460.0 kJ/mol,则工业上利用水煤气成分按1:1合成二甲醚的热化学方程式为 。
(2)工业上采用电浮远凝聚法处理污水时,保持污水的pH在5.0,通过电解生成Fe(OH)3胶体,吸附不溶性杂质,同时利用阴极产生的H2,将悬浮物带到水面,利于除去。实验室以二甲醚燃料电池模拟该方法设计的装置如下图所示:
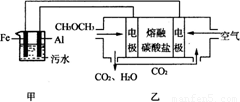
①乙装置以熔融碳酸盐为电解质,稀土金属材料为电极。写出该燃料电池的正极电极反应式 ;下列物质可用做电池熔融碳酸盐的是 。
A.MgCO3 B.Na2CO3 C.NaHCO3 D.(NH4)2CO3
②写出甲装置中阳极产物离子生成Fe(OH)3沉淀的离子方程式: 。
③已知常温下Kap[Fe(OH)3]=4.0×10—38,电解一段时间后,甲装置中c(Fe3+)= 。
④已知:H2S的电离平衡常数:K1=9.1×10—8、K2=1.1×10—12;H2CO3的电离平衡常数:K1=4.31×10—7、K2=5.61×10—11。测得电极上转移电子为0.24mol时,将乙装置中生成的CO2通入200mL 0.2mol/L的Na2S溶液中,下列各项正确的是
A.发生反应的离子方程式为:CO2+S2—+H2O=CO32—+H2S
B.发生反应的离子方程式为:CO2+S2—+H2O=HCO3—+HS—
C.c(Na+)=2[c(H2S)+c(HS—)+c(S2—)]
D.c(Na+)+c(H+)=2c(CO32—)+2c(S2—)+c(OH—)
E.c(Na+)>c(HCO3—)>c(HS—)>c(OH—)
(1)3H2(g)+3CO(g)=CH3OCH3(g)+CO2(g)ΔH= -246.4kJ/mol
(2)① O2 + 4e—+2CO2 =2CO32—;B
② 4Fe2++O2+10H2O=4Fe(OH)3↓+8H+
③ 4.0×10—11mol/L ④B、C、E
【解析】
试题分析:(1)根据盖斯定律可知:工业上利用水煤气成分按1:1合成二甲醚的热化学方程式为3H2(g)+3CO(g)=CH3OCH3(g)+CO2(g)ΔH=-246.4kJ/mol。(2)①以二甲醚为燃料的电池,通入燃料的电极为负极,通入O2的电极为正极。正极电极反应式O2 + 4e—+2CO2 =2CO32—。NaHCO3和(NH4)2CO3 受热易分解,所以不能用熔融碳酸盐电解质。MgCO3和Na2CO3都是离子化合物,离子键前者大于后者,熔化需要消耗更多的能量,所以一般用Na2CO3来做熔融盐电池的电解质。 ②在甲装置中Al作阴极。Fe作阳极。阳极发生氧化反应:Fe-2e-=Fe2+. 然后发生反应:4Fe2++O2+10H2O=4Fe(OH)3↓+8H+。产生4Fe(OH)3沉淀,来吸附不溶性杂质,从而使水变得澄清。③在常温下Kap[Fe(OH)3] =4.0× 10—38,pH在5.0,c(OH-)=10-9mol/L, c(Fe3+)= Kap[Fe(OH)3]÷ c(OH-)3=4.0×10—38÷ (10-9)3= 4.0×10—11mol/L. ④在甲醚燃料电池中的负极发生的电极反应为::CH3OCH3+3H2O=2CO2+12e-+12H+。可见每转移6mol的电子,产生1÷mol的CO2气体,今转移电子0.24mol,所以产生CO2气体的物质的量为0.24mol÷6= 0.04mol.n(Na2S)= 0.2L× 0.2mol/L=0.04mol. 因此结合电离平衡常数二者发生反应的反应为CO2+S2—+ H2O=HCO3—+HS—。因此A错误。B正确。C.根据物料守恒可得c(Na+)=2c(S2—)(开始)=2[c(H2S)+ c(HS—)+c(S2—)]。正确。D. 根据电荷守恒可得:c(Na+)+c(H+)= 2c(CO32—)+2c(S2—)+ c(OH—)+c(HCO3—)+c(HS—).错误。E.根据二者之间的反应及物料守恒可得c(Na+)= c(HCO3—)(开始)+c(HS—)(开始). HCO3—和HS—都要发生水解反应,要消耗,因为电离平衡常数H2CO3>H2S。酸的电离常数越大,越容易电离,酸根离子水解程度就越小。即水解程度HCO3—<HS—。水解程度越大溶液中该离子的浓度就越小。所以c(HCO3—)>c(HS—)。水解使溶液显碱性。但盐水解总的来说是很微弱的,因此溶液中各离子的浓度关系为:c(Na+)>c(HCO3—)>c(HS—)>c(OH—)。正确。
考点:考查热化学方程式和离子方程式的书写、燃料电池、电解池的反应原理、离子浓度的大小比较。


科目:高中化学 来源: 题型:
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol?L-1) | 0.28 | 0.86 | 0.86 |
查看答案和解析>>
科目:高中化学 来源:2011-2012学年江苏省无锡市高三上学期期末考试化学试卷 题型:填空题
(14分)二甲醚(CH3OCH。)和甲醇(CH3OH)被称为21世纪的新型燃料,具有清洁、高效等优良的性能。以CH4和H2O为原料制备二甲醚和甲醇的工业流程如下:

(1)催化反应室B中CO与H2合成二甲醚的化学方程式为 .
(2)催化反应室A中发生的反应为:
CH4(g)+H2O(g) CO(g)+3H2(g)……(I)、CO(g)+H2O(g)
CO(g)+3H2(g)……(I)、CO(g)+H2O(g) CO2(g)+H2(g)……(Ⅱ)催化反应室C中发生的反应为:
CO2(g)+H2(g)……(Ⅱ)催化反应室C中发生的反应为:
CO(g)+2H2(g) CH3OH(g)……(Ⅲ)、CO2(g)+3H2(g)
CH3OH(g)……(Ⅲ)、CO2(g)+3H2(g) CH3OH(g)+H2O(g)……(Ⅳ)
CH3OH(g)+H2O(g)……(Ⅳ)
①已知:原子利用率= ×100%,试求反应(Ⅳ)的原子利用率为 。
×100%,试求反应(Ⅳ)的原子利用率为 。
②反应(Ⅳ)的△S 0(填“>”、“=”或“<”)。
③在压强为5MPa,体积为VL的反应室c中,amol CO与20mol H2在催化剂作用下发生反应(Ⅲ)生成甲醇,CO的转化率与温度的关系如右图。则该反应的△H 0(填“>”、“=”或“<”)。300℃时该反应的平衡常数K= (用含字母的代数式表示)。

(3)我国某科研所提供一种碱性“直接二甲醚燃料电池”。
该燃料电池负极的电极反应式为:
CH3OCH3一12e一+16OH一=2CO2-3+11H2O。有人提出了一种利用氯碱工业产品治理含二氧化硫(体积分数为x)废气的方法如下:
①将含SO2的废气通人电解饱和食盐水所得溶液中,得NaHSO3溶液;
②将电解饱和食盐水所得气体反应后制得盐酸;
③将盐酸加入NaHSO3溶液中得SO2气体回收。
用上述碱性“直接二甲醚燃料电池”电解食盐水来处理标准状况下VL的废气,计算消耗二甲醚的质量。
查看答案和解析>>
科目:高中化学 来源: 题型:
(14分)二甲醚(CH3OCH。)和甲醇(CH3OH)被称为21世纪的新型燃料,具有清洁、高效等优良的性能。以CH4和H2O为原料制备二甲醚和甲醇的工业流程如下:
(1)催化反应室B中CO与H2合成二甲醚的化学方程式为 .
(2)催化反应室A中发生的反应为:
CH4(g)+H2O(g)![]() CO(g)+3H2(g)……(I)、CO(g)+H2O(g)
CO(g)+3H2(g)……(I)、CO(g)+H2O(g)![]() CO2(g)+H2(g)……(Ⅱ)催化反应室C中发生的反应为:
CO2(g)+H2(g)……(Ⅱ)催化反应室C中发生的反应为:
CO(g)+2H2(g)![]() CH3OH(g)……(Ⅲ)、CO2(g)+3H2(g)
CH3OH(g)……(Ⅲ)、CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)……(Ⅳ)
CH3OH(g)+H2O(g)……(Ⅳ)
①已知:原子利用率= ×100%,试求反应(Ⅳ)的原子利用率为 。
×100%,试求反应(Ⅳ)的原子利用率为 。
②反应(Ⅳ)的△S 0(填“>”、“=”或“<”)。
③在压强为5MPa,体积为VL的反应室c中,amol CO与20mol H2在催化剂作用下发生反应(Ⅲ)生成甲醇,CO的转化率与温度的关系如右图。则该反应的△H 0(填“>”、“=”或“<”)。300℃时该反应的平衡常数K= (用含字母的代数式表示)。
(3)我国某科研所提供一种碱性“直接二甲醚燃料电池”。
该燃料电池负极的电极反应式为:
CH3OCH3一12e一+16OH一=2CO2-3+11H2O。有人提出了一种利用氯碱工业产品治理含二氧化硫(体积分数为x)废气的方法如下:
①将含SO2的废气通人电解饱和食盐水所得溶液中,得NaHSO3溶液;
②将电解饱和食盐水所得气体反应后制得盐酸;
③将盐酸加入NaHSO3溶液中得SO2气体回收。
用上述碱性“直接二甲醚燃料电池”电解食盐水来处理标准状况下VL的废气,计算消耗二甲醚的质量。
查看答案和解析>>
科目:高中化学 来源:2012届江苏省无锡市高三上学期期末考试化学试卷 题型:填空题
(14分)二甲醚(CH3OCH。)和甲醇(CH3OH)被称为21世纪的新型燃料,具有清洁、高效等优良的性能。以CH4和H2O为原料制备二甲醚和甲醇的工业流程如下:
(1)催化反应室B中CO 与H2合成二甲醚的化学方程式为 .
与H2合成二甲醚的化学方程式为 .
(2)催化反应室A中发生的反应为:
CH4(g)+H2O(g) CO(g)+3H2(g)……(I)、CO(g)+H2O(g)
CO(g)+3H2(g)……(I)、CO(g)+H2O(g) CO2(g)+H2(g)……(Ⅱ)催化反应室C中发生的反应为:
CO2(g)+H2(g)……(Ⅱ)催化反应室C中发生的反应为:
CO(g)+2H2(g) CH3OH(g)……(Ⅲ)、CO2(g)+3H2(g)
CH3OH(g)……(Ⅲ)、CO2(g)+3H2(g) CH3OH(g)+H2O(g)……(Ⅳ)
CH3OH(g)+H2O(g)……(Ⅳ)
①已知:原子利用率= ×100%,试求反应(Ⅳ)的原子利用率为 。
×100%,试求反应(Ⅳ)的原子利用率为 。
②反应(Ⅳ)的△S 0(填“>”、“=”或“<”)。
③在压强为5MPa,体积为VL的反应室c中,amol CO与20mol H2在催化剂作用下发生反应(Ⅲ)生成甲醇,CO的转化率与温度的关系如右图。则该反应的△H 0(填“>”、“=”或“<”)。300℃时该反应的平衡常数K= (用含字母的代数式表示)。
(3)我国某科研所提供一种碱性“直接二甲醚燃料电池”。
该燃料电池负极的电极反应式为:
CH3OCH3一12e一+16OH一=2CO2-3+11H2O。有人提出了一种利用氯碱工业产品治理含二氧化硫(体积分数为x)废气的方法如下:
①将含SO2的废气通人电解饱和食盐水所得溶液中,得NaHSO3溶液;
②将电解饱和食盐水所得气体反应后制得盐酸;
③将盐酸加入NaHSO3溶液中得SO2气体回 收。
收。
用上述碱性“直接二甲醚燃料电池”电解食盐水来处理标准状况下VL的废气,计算消耗二甲醚的质量。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com