
��NAΪ�����ӵ�������ֵ������˵������ȷ����(����)
A�����³�ѹ�£�22.4 L��ϩ�к�C��H������ĿΪ4NA
B��0.1 mol��L��1��NaHSO4��Һ�к��������ӵ�����Ϊ0.2NA
C��7.8 g Na2S�����7.8 g Na2O2�����к��е���������Ŀ��Ϊ0.1NA
D����״���£�2.24 L Cl2�����ϡNaOH��Һ��Ӧ��ת�Ƶĵ�������Ϊ0.1NA
 ��Կ���Ծ�ϵ�д�
��Կ���Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij��Ӧ��������Ӧ A BC���ɣ���Ӧ�����е������仯������ͼ������������ȷ���� (����)��

A��������Ӧ��Ϊ���ȷ�Ӧ
B�����ֻ�������C���ȶ�
C�����������ı䷴Ӧ���ʱ�
D��������Ӧ�Ħ�H��E1��E2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���գ����������о�С��ͨ����ͬŬ�����������۵������ӣ�ͬʱʹ�����������̺�﮲������缫������������ӳ���أ��乤��ԭ��ʾ��ͼ��ͼ��ʾ�����ڸõ�ص�˵������ȷ���� (����)��
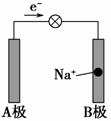
A���ŵ�ʱA��������
B���ŵ�ʱNa�� ���ƶ�
C�����ʱ�ǽ���ѧ��ת��Ϊ����
D�����ʱB��Ϊ����������������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��Ԫ�صĻ�����Ӧ��ʮ�ֹ㷺����ش�
��1�����ȼ��Һ̬ƫ�����£�C2H8N2������Һ̬N2O4�������������߷�Ӧ�ų��������ȣ�������������Ⱦ�������ˮ����֪�����£�1 gȼ����ȫȼ���ͷų�������Ϊ42.5kJ����÷�Ӧ���Ȼ�ѧ����ʽΪ ��

��2��298 Kʱ����2L�̶�������ܱ������У��������淴Ӧ��2NO2(g) N2O4(g) ��H��-a kJ/mol (a>0) ��N2O4�����ʵ���Ũ����ʱ��仯��ͼ����ƽ��ʱ��N2O4��Ũ��ΪNO2��2�����ش��������⣺
N2O4(g) ��H��-a kJ/mol (a>0) ��N2O4�����ʵ���Ũ����ʱ��仯��ͼ����ƽ��ʱ��N2O4��Ũ��ΪNO2��2�����ش��������⣺
��298kʱ���÷�Ӧ��ƽ�ⳣ��Ϊ L��mol��1����ȷ��0.01����
������������Ǵ���ƽ��״̬���� ��
A.���������ܶȱ��ֲ��䣻 B.����������ɫ���ٱ仯�� C.��ѹ�㶨ʱ
������Ӧ��398K���У�ijʱ�̲��n(NO2)=0.6 moln(N2O4)=1.2mol�����ʱV������ V���棩���� ��>������<����=������
��3��NH4HSO4�ڷ����Լ���ҽҩ�����ӹ�ҵ����;�㷺������100 mL 0.1 mol��L��1NH4HSO4��Һ�еμ�0.1 mol��L��1NaOH��Һ���õ�����ҺpH��NaOH��Һ����Ĺ�ϵ������ͼ��ʾ���Է���ͼ��a��b��c��d��e����㡣
��b��ʱ����Һ�з���ˮ�ⷴӦ��������______��
����c�㣬��Һ�и�����Ũ���ɴ�С������˳�� ��
��d��e���Ӧ��Һ�У�ˮ����̶ȴ�С��ϵ��d e���>������<����=������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��NAΪ�����ӵ�������ֵ������˵����ȷ����(����)
A��25 �棬pH��13��NaOH��Һ�У�����OH������ĿΪ0.1NA
B��1.2 g C60��ʯī�Ļ�����У����е�̼ԭ����ĿΪ0.1NA
C��2.24 L N2��NH3�Ļ�������У����еĹ��õ��Ӷ���ĿΪ0.3NA
D����״���£�6.72 L NO2��ˮ��ַ�Ӧת�Ƶĵ�����ĿΪ0.1NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ڿ��淴Ӧ�У�ƽ�ⳣ���뷴Ӧ���е��ȵĹ�ϵ��ȷ����(����)
A��KԽ��Ӧ�̶�Խ��
B��KԽ��Ӧ�̶�ԽС
C��K�Ĵ�С�뷴Ӧ�̶���
D�������¶ȣ�K����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ȷ�ӦCO(g)��H2O(g)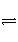
 CO2(g)��H2(g)���¶�t1ʱ�ﵽƽ�⣬[CO]1��[H2O]1��1.0 mol��L��1����ƽ�ⳣ��ΪK1�������������䣬���߷�Ӧ��ϵ���¶���t2ʱ����Ӧ���ƽ��Ũ�ȷֱ�Ϊ[CO]2��[H2O]2��ƽ�ⳣ��ΪK2����(����)
CO2(g)��H2(g)���¶�t1ʱ�ﵽƽ�⣬[CO]1��[H2O]1��1.0 mol��L��1����ƽ�ⳣ��ΪK1�������������䣬���߷�Ӧ��ϵ���¶���t2ʱ����Ӧ���ƽ��Ũ�ȷֱ�Ϊ[CO]2��[H2O]2��ƽ�ⳣ��ΪK2����(����)
A��������COŨ�ȣ�K2��K1������ B��K2��K1
C��[CO]2��[H2O]2 D��[CO]1��[CO]2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
Ϊ�ⶨij�л���A�Ľṹ����������ʵ�飺
(1)���л���A�����������г��ȼ�գ�ʵ���ã�����5.4 g H2O��8.8 g CO2����������6.72 L(��״����)����������и�Ԫ�ص�ԭ�Ӹ�������________��
(2)�����Dzⶨ�л����������Է�������Ϊ46��������ʵķ���ʽ��________��
(3)���ݼۼ����ۣ�Ԥ��A�Ŀ��ܽṹ��д���ṹ��ʽ________��
(4)�˴Ź�����ԭ�ӹ����ܶ��л�������в�ͬλ�õ���ԭ�Ӹ�����ͬ�ķ�ֵ(�ź�)�����ݷ�ֵ(�ź�)����ȷ����������ԭ�ӵ���������Ŀ�����磺���ȼ���(Cl—CH2—O—CH3)��������ԭ�ӣ���˴Ź���������ͼ����ʾ�����ⶨ���л���A�ĺ˴Ź�������ʾ��ͼ��ͼ����ʾ����A�Ľṹ��ʽΪ________��

(5)A��һ����������ˮ������B��B�ɺϳɰ�װ����C����д��Bת��ΪC�Ļ�ѧ��Ӧ����ʽ��______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����й������ϵ��������ȷ����
A����Ϊ���������ǿ�������ᣬ������Ԫ�صķǽ�����ǿ����
B����Ϊ����������ȣ�������NaOH��Һ�к͵������Ũ�ȵĴ�������ᣬǰ�߷ų�������
C����ΪKCl���ܽ�����¶ȵĽ��Ͷ���С�����Խ����¶�KCl��Һ����������һ�����С
D����ΪC3H8(g)+5O2(g)=3CO2(g)+4H2O(1)��Ҫ���ȷ��ܷ��������Ը÷�Ӧһ�������ȷ�Ӧ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com