
| A. | 胶体与溶液的本质区别是能否发生丁达尔效应 | |
| B. | 胶体加入某些盐可产生沉淀,而溶液不能 | |
| C. | 胶体是一种介稳性的分散系,而溶液是一种非常稳定的分散系 | |
| D. | 胶体能够发生丁达尔现象,溶液也能发生丁达尔现象 |
分析 A、分散系的本质区别是分散质粒子直径的大小;
B、胶体遇电解质溶液发生聚沉;
C、胶体中的胶粒带电,故胶粒间相互排斥;
D、丁达尔效应是胶体所特有的性质.
解答 解:A、分散系的本质区别是分散质粒子直径的大小,丁达尔效应只是胶体所特有的性质,但不是本质区别,故A错误;
B、胶体中的胶粒带电,故遇电解质溶液发生聚沉,而溶液也能和某些盐发生反应生成沉淀,故B错误;
C、胶体中的胶粒带电,故胶粒间相互排斥,故胶体属于介稳体系,而溶液是均一稳定的体系,故C正确;
D、丁达尔效应是胶体所特有的性质,溶液不能发生,故D错误.
故选C.
点评 本题考查了胶体和其它分散系的本质区别以及胶体的性质,应注意的是胶体遇电解质溶液发生聚沉生成沉淀,而溶液也可以和其它的电解质溶液发生反应生成沉淀.


 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 金属原子失去电子越多,还原性越强 | |
| B. | 盐酸酸化的高锰酸钾溶液氧化性更强 | |
| C. | 强氧化剂与强还原剂不一定能发生氧化还原反应 | |
| D. | 工业上镁铝单质都是电解对应熔融的氯化物得到的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5种 | B. | 6 种 | C. | 8种 | D. | 10种 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
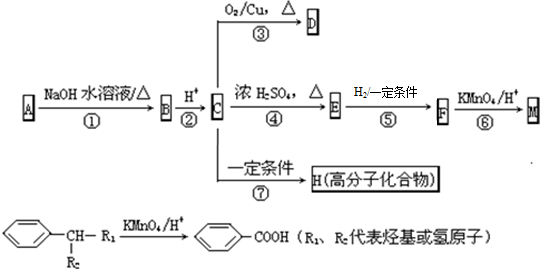
 .
.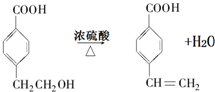 反应⑦的化学方程式为
反应⑦的化学方程式为 .
.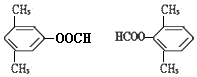 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将磁性氧化铁溶于稀硫酸:Fe3O4+8H+=3Fe3++4H2O | |
| B. | 0.2mol明矾与300mL1mol/L的氢氧化钡溶液混合:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓ | |
| C. | 将氯化亚铁溶液和稀硝酸混合:Fe2++4H++NO3-=Fe3++2H2O+NO↑ | |
| D. | 将铁粉加入稀硫酸中:2Fe+6H+=2Fe3++3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 保持体积不变,充入H2O(g)使体系压强增大 | |
| B. | 将容器的体积缩小一半 | |
| C. | 保持体积不变,充入N2使体系压强增大 | |
| D. | 保持压强不变,充入N2使容器体积变大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
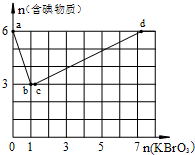 现向含6mol KI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加入KBrO3的物质的量的关系如图所示.
现向含6mol KI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加入KBrO3的物质的量的关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硝酸钾 | B. | 醋酸钠 | C. | 硫酸氢钠 | D. | 硫酸铜 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com