
【题目】将洁净的金属片Fe、Zn、A、B 分别与Cu用导线连接浸在合适的电解质溶液里。实验并记录电压表指针的移动方向和电压表的读数如下表所示。
金属 | 电子流动方向 | 电压/V |
Fe | Fe→Cu | +0.78 |
Zn | Zn→Cu | +1.10 |
A | Cu→A | -0.15 |
B | B→Cu | +0.3 |
根据表中实验记录,回答下列问题:
(1)构成两电极的金属活动性相差越大,电压表的读数越 (填“大”或“小”)。
(2)Zn、A、B三种金属活动性由强到弱的顺序是 。
(3)Cu与A构成的原电池中, 为负极,此电极反应为 。
(4)A、B形成合金,露置在潮湿空气中, 先被腐蚀。
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】用胆矾配制0.2mol/L的CuSO4溶液,下列操作正确的是( )
A.取50g胆矾溶于1L水中
B.取50g胆矾溶于水配成1L溶液
C.取32g胆矾溶于水配成1L溶液
D.取无水硫酸铜32g溶于1L水中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验现象的描述中,正确的是
A.金属钠在氯气中燃烧,有白雾生成
B.铜在氯气中燃烧,生成蓝色的氯化铜颗粒
C.钠投入硫酸铜溶液中,会产生蓝色沉淀
D.钠在空气中燃烧后得到白色粉末状固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有M,N两种气态化合物,其摩尔质量之比为2:1,试回答下列问题:
①同温同压下,M,N气体的密度之比为
②相同温度下,在两个相同体积的密闭容器中分别充入M,N,若两个容器中气体的密度相等,则两个容器中的压强之比为
③将M,N两种气体分别溶于水(M,N与水均不反应)配成溶液,当两种溶液的质量分数相同时,其密度分别为d1和d2 , 则两种溶液的物质的量浓度之比为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 三氯化碘(ICl3)在药物合成中用途非常广泛,其熔点:33℃,沸点:73℃。实验室可用下图所示装置制取ICl3 :
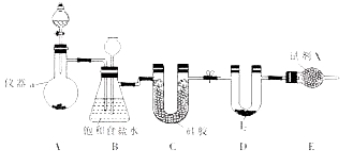
(1)仪器a 的名称是 。
(2)制备氯气选用的药品为漂白粉固体[主要成分为Ca(ClO)2]和浓盐酸,有关反应的化学方程式为 。
(3)装置B(吸滤瓶)即可用于除杂,也是安全瓶,能监侧实验进行时装置C中是否发生了堵塞。请描述发生堵塞时B中现象 。
(4)试剂X为 。
(5)氯气与单质碘需在温度稍低于70℃下反应,则装置D适宜的加热方式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下除杂方法(括号内为杂质)中,错误的是( )
A.CH3CH2OH(H2O):加CaO,蒸馏
B.NaCl(I2):加热,升华
C.溴苯(溴):加NaOH溶液,分液
D.NaCl(KNO3):配成溶液,降温结晶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属腐蚀的电化学原理可用下图模拟。
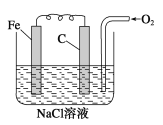
(1)请写出有关电极反应式:①铁棒上的电极反应式:_______________________。
碳棒上的电极反应式:_________________________。
(2)该图所表示的是_________________________(填“析氢”或“吸氧”)腐蚀。
(3)若将O2撤走,并将NaCl溶液改为稀H2SO4溶液,则此图可表示__________(填“析氢”或“吸氧”)腐蚀原理;若用牺牲阳极法来保护铁棒不被腐蚀溶解,即可将碳棒改为_________棒。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁生锈是比较常见的现象,某实验小组,为研究铁生锈的条件,设计了以下快速、易行的方法:
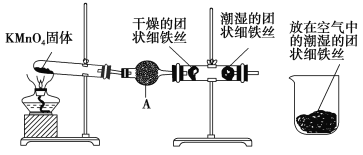
首先检查制氧装置的气密性,然后按图连接好装置,点燃酒精灯给药品加热,持续3分钟左右,观察到的实验现象为:①直形管中用蒸馏水浸过的光亮铁丝表面颜色变得灰暗,发生锈蚀;②直形管中干燥的铁丝表面依然光亮,没有发生锈蚀;③烧杯中潮湿的铁丝表面依然光亮。
试回答以下问题:
(1)由于与金属接触的介质不同。金属腐蚀分成不同类型,本实验中铁生锈属于________。能表示其原理的反应方程式为___________________________________。
(2)仪器A的名称为________,其中装的药品可以是________,其作用是________。
(3)由实验可知,该类铁生锈的条件为_____________________________________,直形管实验与烧杯实验的对比,说明决定铁生锈快慢的一个重要因素是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如下能量关系示意图分析,下列说法正确的是
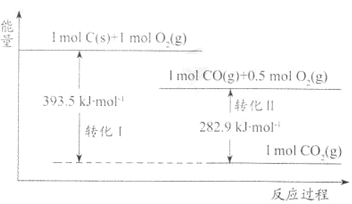
A. 1molC(g)与1molO2(g)的能量之和为393.5kJ
B. 反应2CO(g)+O2(g)=2CO2(g)中,反应物的总键能小于生成物的总键能
C. C→CO的热化学方程式为2C(s) +O2(g)=2CO(g) △H=-110.6kJ/mol
D. 热值是指一定条件下单位质量的物质完全燃烧所放出的热量,则CO的热值△H=10.1kJ/g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com