
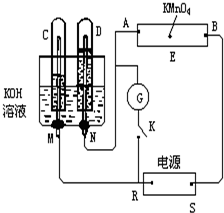
 如图所示,E为沾有Na2SO4溶液的滤纸,并加入几滴酚酞.A,B分别为Pt片,压在滤纸两端,R、S为电池的电极.M、N是用多微孔的Ni的电极材料,它在碱溶液中可以视为惰性电极.G为电流计,K为开关.C、D和电解池中都充满浓KOH溶液.若在滤纸中央点上一滴紫色的KMnO4溶液,K打开,接通电源一段时间后,C、D中有气体产生.
如图所示,E为沾有Na2SO4溶液的滤纸,并加入几滴酚酞.A,B分别为Pt片,压在滤纸两端,R、S为电池的电极.M、N是用多微孔的Ni的电极材料,它在碱溶液中可以视为惰性电极.G为电流计,K为开关.C、D和电解池中都充满浓KOH溶液.若在滤纸中央点上一滴紫色的KMnO4溶液,K打开,接通电源一段时间后,C、D中有气体产生.分析 (1)根据C、D两电极得到的气体体积判断电极名称,从而确定电源R、S电极名称;
(2)先判断A、B 的电极名称,根据电解池的工作原理来书写电极反应式;
(3)根据电解池的工作原理判断电解时溶液中离子的移动方向;
(4)根据原电池中燃料电池的工作原理和规律来回答.
解答 解:(1)闭合K,通直流电,电极C、D及氢氧化钾溶液构成电解池,根据离子的放电顺序,溶液中氢离子、氢氧根离子放电,分别生成氢气和氧气,氢气和氧气的体积比为2:1,通过图象知,C极上气体体积是D极上气体体积的2倍,所以C极上得氢气,D极上得到氧气,故R是负极,S是正极,所以B极是阳极,A极是阴极.
故答案为:负;
(2)A极是阴极,电解高锰酸钾时,在该极上放电的是氢离子,所以该极上碱性增强,酚酞显红色,B极是阳极,该极附近发生的电极反应式为:4OH--4e-=2H2O+O2↑,故答案为:溶液变红;4OH--4e-=2H2O+O2↑;
(3)浸有高锰酸钾的滤纸和电极A、B与电源也构成了电解池,因为R是负极,S是正极,所以B极是阳极,A极是阴极,电解质溶液中的阴离子高锰酸跟离子向阳极移动,所以B极呈紫色,故答案为:B;
(4)当C、D里的气体产生到一定量时,切断外电源并接通开关K,构成氢氧燃料电池,在燃料电池中,燃料氢气为负极,方程式为2H2+O2=2H2O;
氧气作正极,方程式为O2+2H2O+4e-=4OH-;故答案为:氢气和氧气构成燃料电池;H2+2OH--2e-=2H2O.
点评 本题考查了原电池、电解池工作原理,会根据电池反应式及元素化合价变化书写正负极电极反应式,再结合各个物理量之间的关系式进行计算,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 物质的摩尔质量等于其相对分子(原子)质量 | |
| B. | “物质的量”是国际单位制中的一个基本单位 | |
| C. | 0.012kg 12C中所含的碳原子数为NA | |
| D. | 1 mol任何物质都含有约6.02×1023个原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,1.12L CCl4含有的共价键数为0.2NA | |
| B. | 常温常压下,2.3g NO2和N2O4的混合物中含有的氧原子数为0.2NA | |
| C. | 过氧化钠与水反应时,生成0.lmol氧气转移的电子数为0.2NA | |
| D. | 常温下,0.1mol•L-1溶液中阴离子总数大于0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、MnO4-、Ag+、Cl- | B. | Cu2+、NO3-、Na+、OH- | ||
| C. | Fe2+、NH4+、NO3-、SO42- | D. | Al3+、Na+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钠、盐酸都为强电解质 | |
| B. | 铁生锈、食物腐败都有氧化反应发生 | |
| C. | 糖类、蛋白质都为高分子化合物 | |
| D. | 一氧化碳和二氧化碳都是酸性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在含有大量[Al(OH)4]-的溶液中:NH4+、Na+、Cl-、H+ | |
| B. | 含有大量Fe3+的溶液中:Na+、Mg2+、I-、SCN- | |
| C. | pH=13的溶液中:K+、NH4+、SO42-、NO3- | |
| D. | 由水电离产生的c(OH-)=1×10-12mol•L-1的溶液中:K+、Na+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 烧菜用过的铁锅,经放置常出现红棕色斑迹 | |
| B. | 用煤气灶燃烧沼气(主要成分为甲烷:CH4)为炒菜提供热量 | |
| C. | 铝制容器因长期存放酸性或碱性食物被腐蚀 | |
| D. | 用醋酸除去水垢[主要成分是CaCO3、Mg(OH)2] |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com