
【题目】下列物质中含原子个数最多的是
A. 9gNH3 B. 标准状况下5.6LCO2
C. 9g H2O D. 0.4mol O3
【答案】A
【解析】
根据n=![]() ,原子的物质的量越多,原子的数目就越多,结合物质的构成微粒计算。
,原子的物质的量越多,原子的数目就越多,结合物质的构成微粒计算。
A. 9gNH3的物质的量是n(NH3)=![]() ,在一个NH3中含有4个原子,所以共含有原子的物质的量为n=4n(NH3)=
,在一个NH3中含有4个原子,所以共含有原子的物质的量为n=4n(NH3)=![]() ;
;
B.标准状况下5.6LCO2气体的物质的量为n(CO2)=![]() ,由于在一个CO2中含有3个原子,所以共含有原子的物质的量为n=3n(CO2)=0.75mol;
,由于在一个CO2中含有3个原子,所以共含有原子的物质的量为n=3n(CO2)=0.75mol;
C.9g H2O的物质的量是n(H2O)=![]() ,由于在一个H2O中含有3个原子,所以共含有原子的物质的量为n=3n(H2O)=1.5mol;
,由于在一个H2O中含有3个原子,所以共含有原子的物质的量为n=3n(H2O)=1.5mol;
D.在一个O3分子中含3个原子, 0.4mol O3中含有的原子物质的量是n=3×0.4mol=1.2mol,可见含有原子物质的量最多的是NH3。由于n=![]() 可知:原子的物质的量越多,含有的原子数目就越多,故原子数目最多的是NH3,选项A合理。
可知:原子的物质的量越多,含有的原子数目就越多,故原子数目最多的是NH3,选项A合理。


科目:高中化学 来源: 题型:
【题目】有甲、乙两种物质:
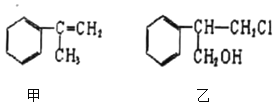
(1)乙中含有的官能团的名称为__________________(不包括苯环)。
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):
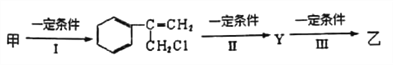
反应I的化学其中反应I的反应类型是____________________,反应II的条件是________,反应III的化学方程式为_________________(不需注明反应条件)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,可逆反应:mA+nB![]() pC达到平衡,若:
pC达到平衡,若:
(1)A、B、C都是气体,减少压强,平衡向正反应方向移动,则m+n和p的关系是
(2)A、C是气体,增加B的量,平衡不移动,则B为 态。
(3)A、C是气体,而且m+n=p,增大压强可使平衡发生移动,则平衡移动的方向是
(4)加热后,可使C的质量增加,则正反应是 反应(放热或吸热)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的分类是学习化学的一种重要方法,科学合理的分类对于系统掌握知识、提高学习效率、解决问题都有着重要的意义。
请回答下列问题:
(1)纯净物根据其组成和性质有如图分类形式,这种分类方法层次分明、简洁直观。

①图中所示所属的分类方法为___________。
②现有碳、一氧化碳、二氧化碳、碳酸氢钠四种物质,采用下列分类标准,无法将其中两种物质归为一类的是___________________。
A.具有还原性 B.属于氧化物 C.碳元素化合价相同 D.属于电解质
③实验室常根据物质分类的原则存放药品,某学校实验室其中的四个药品柜已经存放了如下部分药品,实验室新购进一些晶体碘,应该将它存放在________________。
药品柜 | 甲柜 | 乙柜 | 丙柜 | 丁柜 |
药品 | 乙醇、乙酸 | 活性炭、红磷 | 锌粒、铜片 | 氯化钠、氯化钾 |
A.甲柜 B.乙柜 C.丙柜 D. 丁柜
④“三酸(硫酸、盐酸、硝酸)”与“两碱(氢氧化钠、碳酸钠)”能发生反应。将一定量的稀硫酸逐滴滴入到氢氧化钠和碳酸钠的混合溶液中,边滴加边搅拌,直至有少量气泡产生,此过程中共发生的离子反应有_______个。
(2)含铁元素的物质有很多,在生产、生活中应用广泛。取少量某油漆的原料Fe2O3(红棕色粉末),加人适量浓盐酸,反应后得到棕黄色溶液,取少量棕黄色溶液置于试管中再滴入NaOH溶液,可观察到有沉淀生成,生成沉淀的离子方程式为_______________________________,另在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入2 mL上述棕黄色溶液,继续加热至液体呈_______色,停止加热,证明所得分散系类型的实验方法的名称是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列有关容量瓶的使用方法的操作中,错误的是_________。
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.定容时,将蒸馏水小心倒入容量瓶中到刻度线齐平处
D.配制溶液时,如果试样是液体,用量筒量取试样后直接倒入容量瓶中定容
E.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复上下颠倒、摇匀。
(2)实验室中需2mol/L的Na2CO3溶液950mL,配制时应选用容量瓶的规格和称取Na2CO3的质量分别是______________。
A.1000mL; 212g B.950mL;543.4g
C.任意规格; 572g D.500mL; 106g
(3)现用98%、密度为1.8g/mL的浓硫酸配制500mL的稀硫酸。请回答下列问题:
①配制稀硫酸时,需要的玻璃仪器有玻璃棒、烧杯、量筒,还缺少的玻璃仪器有_______(填写仪器名称)。
②经计算,配制500mL0.2mol/L的稀硫酸需要上述浓硫酸的体积为___________。
③稀浓硫酸时,实验操作步骤:____________________。
(4)误差
①用量筒量取浓硫酸时仰视读数,导致最终结果______(填“偏大”“偏小”或“不变”);
②定容时仰视读数,导致最终结果__________(填“偏大”“偏小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上曾经通过反应“3Fe + 4NaOH![]() Fe3O4 + 2H2↑+ 4Na↑”生产金属钠。下列说法正确的是
Fe3O4 + 2H2↑+ 4Na↑”生产金属钠。下列说法正确的是
A. 还原产物是钠Na和Fe3O4
B. 用磁铁可以将Fe与Fe3O4分离
C. 将生成的气体在空气中冷却可获得钠
D. 每生成1 mol H2,该反应转移的电子数约为4×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯用途广泛,工业上可通过下列流程合成二甘醇及其衍生物。已知:R-OH + SOCl2 → R-Cl + SO2 ↑+ HCl↑ 请回答:

(1)写出B的官能团的电子式________________________。
(2)写出有关物质的结构简式:A_________________D_________________。
(3)指出反应类型:②_________________。
(4)写出下列化学方程式:反应①______________;反应②___________。
(5)①二甘醇又名(二)乙二醇醚,根据其结构判断下列说法正确的是____(填序号)。
a. 难溶于水 b. 沸点较高 c. 不能燃烧
②E的同分异构体很多,写出其中能够发生银镜反应的两种异构体的结构简式_________________。
(6)请写出由1-氯丙烷合成丙酮的合成路线图并注明反应条件(无机试剂任选)________。合成路线流程图示例如下:CH3CH2OH![]() CH2=CH2
CH2=CH2![]() Br-CH2CH2-Br
Br-CH2CH2-Br
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除杂方法不正确的是
A. 除去NH4Cl溶液中的FeCl3,可向溶液中加入氨水调节pH
B. 除去金属离子Cu2+、Hg2+,可向溶液中加入Na2S、H2S等沉淀剂
C. 除去某溶液中的SO42-可向溶液中加入镁盐
D. 除去ZnCl2溶液中的Fe3+可向溶液中加入Zn(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用H2还原WO3制备金属W的装置如图所示(Zn粒中往往含有硫等杂质,焦性没食子酸溶液用于吸收少量氧气),下列说法正确的是
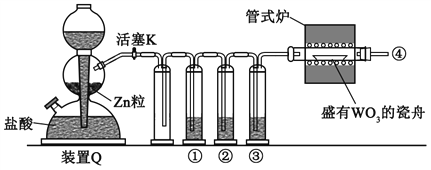
A. ①、②、③中依次盛装KMnO4溶液、浓H2SO4、焦性没食子酸溶液
B. 管式炉加热前,用试管在④处收集气体并点燃,通过声音判断气体纯度
C. 结束反应时,先关闭活塞K,再停止加热
D. 装置Q(启普发生器)也可用于二氧化锰与浓盐酸反应制备氯气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com